NeuroImage|EEG与行为证据表明:空间表征在时间判断中呈现“晚期补偿性”参与
人类普遍使用空间隐喻来表征时间,从指示过去和未来的手势到诸如时空弯曲之类的科学概念。然而,空间表征是否是大脑计时方式的基础仍未得到解决。通过将行为测量与实时脑记录相结合,我们证明了时间的空间编码仅在缓慢、费力的决策过程中出现,而不是在快速、准确的决策中。脑电图特征揭示了一个级联过程:计时所需的神经资源不足会触发补偿性的空间机制。计算模型将这种变异性与优化认知控制的神经调节系统波动联系起来。这些发现从根本上修正了我们对心理计时的理解,表明空间表征是当主要计时机制失效时被招募的认知启发式策略,而非时间认知的内在特征。
摘要
为补偿时间在感官层面的不可触性,人类常常依赖空间隐喻、手势与视觉工具来表征时间的流逝。这些空间工具,即启发式机制,既包括日常实践(例如用具有方向性的手势指示过去或未来事件),也包括更抽象的科学概念化(例如相对论中的“时空弯曲”)。尽管时间的空间化如此普遍,但空间在大脑时间表征中是否具有内在成分,以及其在监测时间长度中的作用程度,仍不清楚。在本研究中,我们结合 EEG 与行为实验,通过一项任务检验上述问题:30 名健康青年志愿者在任务中需要区分短(1 秒)与长(3 秒)时间间隔。在相容条件下,“短”判断与左侧按键反应相对应,“长”判断与右侧按键反应相对应;在不相容条件下,时间长度与左右侧反应的对应关系被反转。与不相容条件相比,相容条件下更快的反应时(RT)这一时间空间表征的特征,仅在较慢 RT 时出现。该结果指出:空间是一种时间表征的晚期补偿机制,当更快且非空间化的计时机制未能得到充分动员时,空间机制才会被招募。EEG 分析揭示了一个级联式过程:在非空间化时间间隔编码不足之后,时间加工中才出现空间机制的介入,并进一步导致对时间长度的决策延迟与反应选择变慢。基于元强化学习的计算模型表明,RT 速度的试次间波动及其对应的时间空间化,可能由多巴胺/去甲肾上腺素系统活动的随机波动及其与前扣带皮层的相互作用所解释。这些发现首次清晰地提供了空间机制在何时、为何以及如何服务于时间加工的证据,并表明非空间化与空间化的计时系统在行为与电生理层面均可被区分。
引言
人类使用空间隐喻、手势与视觉工具来表征并交流时间的流动。这些空间表征既植根于生物学约束,也源自文化塑造的感觉运动习惯。作为向前行走的生物,人类几乎普遍倾向于将过去表征为“留在身后”,将未来表征为“在身体前方等待”。此外,与阅读与观察习惯相关的时间空间化经验,也会塑造相应的时间流逝的空间表征。例如,在从左到右阅读的文化中,人们在心理上将短时间长度与过去事件放置在空间左侧,而将长时间长度与未来事件放置在空间右侧;相反,在从右到左阅读的文化中,人们采用从右到左的时间方向表征。
关于人类时间空间表征的主要实验证据来自 STEARC 效应(Space Time Association of Response Codes)。STEARC 显示:在从左到右阅读者中,当需要将时间间隔分类为“短”时,如果反应位于空间左侧则更快;当分类为“长”时,如果反应位于空间右侧则更快。该相容条件与不相容条件形成对照:在不相容条件下,“短”映射到右侧、“长”映射到左侧,RT 更慢。时间间隔长度与侧化运动反应位置之间的空间相容性效应提示:时间在心理上可能沿着文化习得的观察与阅读方向展开。STEARC 效应常被视为表明大脑计时机制中存在一种内在的空间成分。然而,与这种广泛观点不同,我们近期发现:STEARC 主要在决策较慢时出现,而在决策较快时并不出现,并且慢反应实际上更不准确。这表明:最早期的计时判断依赖非空间化机制,而空间编码是更慢的附加过程,会逐步叠加到主要机制之上。该结果提出一种可能性:在行为与脑活动层面,将快速的非空间化时间知觉机制与较慢的空间化机制分离开来。本 EEG 研究在此基础上进一步考察:时间编码与运动准备的神经特征如何随反应速度而变化。
既往 EEG 研究已识别出 STEARC 的神经相关指标,即在选择相容与不相容手部反应时所涉及的半球间竞争。具体而言,与不相容映射(左–长、右–短)相比,相容指令(左–短、右–长)与更大的侧化准备电位(LRP)相关,反映了对侧运动皮层(相对于反应手)相较于非反应手对侧运动皮层的更强激活。在 STEARC 情境中,LRP 研究显示:在预期短时长起点附近,右侧运动皮层首先被激活,提示左手反应的早期预激活;随着时间向长时长推进,该运动激活逐渐转向左半球,提示右手反应对长时长的延迟激活。值得注意的是,当“长”时长与左手“不相容”反应相联系时,上述 LRP 活动模式不再出现,即在预期短时长起点附近并不存在对右手反应的预激活。基于这些证据,本研究检验:STEARC 随反应速度变化而在强度与出现上产生的差异,是否会反映在 LRP 振幅的相应变化中。例如,可以预测:在较慢反应中更充分发展的 STEARC,可能伴随更显著的 LRP。此外,为进一步刻画空间相容性效应如何从决策形成传播到动作执行,我们还分析了中央侧化导联上的头皮负波,即准备电位(Bereitschaftspotential),其反映与反应准备相关的皮层兴奋性。
更重要的是,我们旨在检验:较慢 RT 时出现的 STEARC 是否在时间间隔编码阶段之前就已有 EEG 活动的调制,即在运动选择过程尚未充分启动之前。发生在时间间隔起点或终点的 EEG 成分不太可能直接受到刺激–反应相容性效应的影响,因为此时与运动输出相关的决策要么尚未形成,要么刚开始展开。然而,如果这些时间编码成分的振幅或潜伏期会随随后反应速度发生系统性变化,则可能揭示:在慢反应试次中观察到的 STEARC 存在更早期的神经前兆。
在这一视角下,我们聚焦于一组成熟的 ERP 成分,它们分别指示时间加工与决策形成的连续阶段。随时间间隔起点到终点发展、位于额中央的缓慢负向成分 CNV,反映计时过程中认知资源的投入与优化。在时间间隔终点,额区的 N1/P2 复合成分与时间信息的知觉评估相关,而中央–后部的 P300 通常与时间长度的决策相关加工相关。此外,计时的晚期正成分 LPCt(常见于额区与后部导联)被认为反映了支持“短”与“长”判断的证据累积。由于这些成分发生在外显反应执行之前,它们若随反应速度发生调制,将表明时间的空间编码能够在相对早期的认知阶段影响计时决策,而非仅在运动准备阶段产生。
综上,这一多阶段 EEG 路径使我们不仅能够确定 STEARC 如何随反应速度出现,还能够定位时间的空间表征首次显现的加工阶段。最后,基于行为与电生理结果,我们提出一个神经–计算框架,用以解释从快速非空间化时间表征向较慢空间化时间表征转变的机制。
材料与方法
参与者
参与者数量通过先验功效分析(G*Power)确定,效应量 f(U)=0.568 来自既往研究。分析结果显示:在采用双侧 0.05 的显著性标准、并使用重复测量的组内因素方差分析时,需要 28 名参与者以获得 0.80 的检验效能。因此,我们招募并测试了 30 名健康成人志愿者(22 名女性、8 名男性;平均年龄:23.3 岁;标准差:2.6)。所有参与者均为右利手(爱丁堡利手量表 > 80%),视力正常或矫正正常,阅读方向为从左到右。无参与者报告既往或当前的神经或精神疾病史。数据采集后,因 EEG 伪迹数量过多,有 1 名参与者被排除。最终样本包含 29 名参与者(21 名女性、8 名男性;平均年龄:23.3 岁;标准差:2.7)。
实验流程与任务
设备与刺激
实验使用 E-Prime 软件(v.2.2)实施。每个试次开始呈现 500 ms 的白色中央注视十字(2.3° × 2.3°)。随后,一个白色圆点目标刺激(直径 = 2.3°)在屏幕中央替代注视十字,作为计时刺激。该刺激呈现短(1000 ms)或长(3000 ms)时间间隔。目标刺激结束后,给予 1500 ms 进行快速反应。试次间间隔(ITI)从参与者反应后开始,持续 500–700 ms(see Fig. 1)。参与者被要求尽可能快速判断目标时间间隔为短或长,并用左手食指按键盘左侧“X”键,或用右手食指按键盘右侧“M”键作答(see Fig. 1)。
整个实验共包含 1024 个试次,分为 8 个实验区组,每区组 128 个试次。在其中 4 个区组中,短间隔对应左侧按键,长间隔对应右侧按键(相容条件:Comp)。在另外 4 个区组中,反应侧与时间长度的对应关系反转(不相容条件:Incomp)。Comp 与 Incomp 两组区组的呈现顺序在参与者间进行平衡。Comp 与 Incomp 各包含 512 个试次,其中每种时长各 256 个试次,并在行为与 EEG 分析所使用的每个 RT 分箱中各有 64 个试次(见下文)。在每个实验区组之前,都会呈现包含 20 个试次的练习区组。
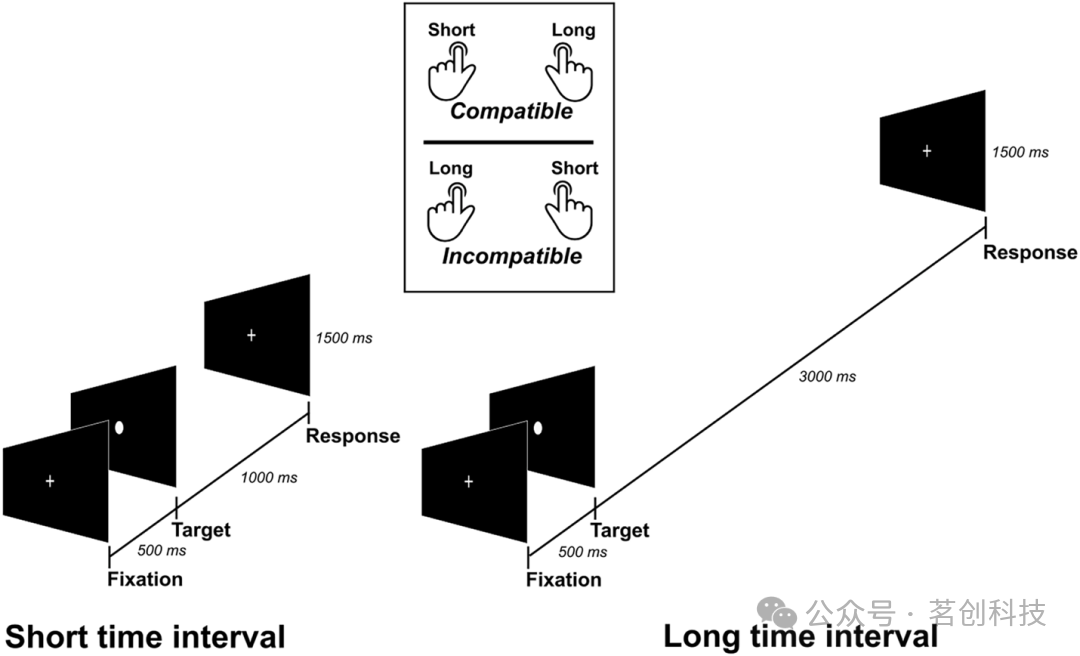
图 1. STEARC 任务中的试次事件与反应条件。
程序
参与者在电屏蔽、安静且隔离的房间中接受测试。头部位置通过下颌托固定,观看距离保持为 57.2 cm。所有参与者均不了解本研究的具体目的,并签署书面知情同意书。实验流程遵循《赫尔辛基宣言》原则,并在数据收集前获得罗马第一大学“萨皮恩扎”伦理委员会批准(Prot. n. 0002,619)。
电生理记录
EEG 采用 64 导电极按 10–10 系统布局记录(BrainVision 系统)。所有头皮通道在线参考为 Cz。水平眼动通过位于左右外眦的双极电极记录。眨眼与垂直眼动通过左眼下方电极记录,并在离线时参考到 Fp1。
各电极点 EEG 信号以 256 Hz 采样率数字化,放大器带通为 0.1–1000 Hz,并包含 50 Hz 陷波滤波,数据用于离线平均。EEG 首先以全通道平均为参考进行重参考,然后离线进行 0.1–30 Hz 带通滤波。随后,在以目标刺激起点锁定的分析中,连续 EEG 被分段为 [−200, +1000 ms](短间隔)与 [−200, +3000 ms](长间隔)。在以目标刺激终点锁定的分析中,短与长间隔的分段均为 [−200, +1500 ms]。所有情况下,目标刺激起点或终点之前的 200 ms 用作基线校正。最后,在以手动反应锁定的分析中,EEG 被分段为 [−1200, +300 ms],并同样以前 200 ms 作为基线。
在计算机化伪迹剔除之前,先使用 BrainVision Analyzer 2 软件中的独立成分分析(ICA)进行眼动校正。随后,在信号平均前进行伪迹剔除:剔除峰值振幅超过 ±100 μV 或电压阶跃超过 60 μV/ms 的分段。平均而言,有 3.4% 的分段因违反上述标准而被剔除。
统计分析
手动反应时(RTs)
低于或高于个体平均 RT 两个标准差的 RT 被排除,按此标准排除的试次少于 3%。STEARC 通过比较 Comp 与 Incomp 条件下的 RT 优势来衡量。为检验其时间发展过程,我们将 STEARC 作为 RT 速度的函数,沿四个四分位/分箱测量:从最快的 Bin1(B1)到最慢的 Bin4(B4)。为此我们使用 Vincentization 程序:对每位参与者,在 Comp 与 Incomp 条件下分别计算正确反应的 RT 分布(由快到慢),然后将每一分布划分为四个比例相等的四分位分箱,使每个分箱包含相同比例的试次(即四分之一)。Comp 与 Incomp 条件中对应分箱的平均 RT 差异,提供了逐分箱的 STEARC 时间进程测量。随后,将个体 RT 输入 2 × 2 × 4 重复测量方差分析,以检验空间–时间相容性(Comp vs Incomp)、时间间隔(Short vs Long)与 RT 分箱(B1、B2、B3、B4)的组内主效应与交互作用。错误分布同样通过 RT 分箱(B1、B2、B3、B4)× 空间–时间相容性(Comp vs Incomp)× 时间间隔(Short vs Long)的重复测量方差分析进行。显著主效应与交互作用均使用 Bonferroni 事后比较进一步检验。
电生理数据
以目标刺激起点锁定的分析:CNV 成分
与既往研究一致,与时间相关的 CNV 以额–中央导联池的平均活动测量,导联包括 FC1、FC2、FCz、C1、Cz、C2。我们关注 CNV 的早期与晚期阶段(见结果)。在短与长时间间隔中均识别出两个阶段:300–550 ms 的早期阶段与 550–900 ms 的晚期阶段。此外,在长时间间隔中还存在一个更晚的阶段,时间窗为 1700–2900 ms。个体平均振幅被输入空间–时间相容性(Comp vs Incomp)× 时间间隔(Short vs Long)× RT 分箱(B1、B2、B3、B4)的重复测量方差分析。显著主效应与交互作用在所有情况下均用 Bonferroni 事后比较进一步检验。
以目标刺激起点锁定的分析:侧化准备电位(C3 − C4)
在每一种实验条件组合下,即空间–时间相容性(Comp vs Incomp)、时间间隔(Short vs Long)与 RT 分箱(B1、B2、B3、B4),我们通过 C3 减去 C4 的振幅,计算左侧相对右侧手运动皮层区域的差异激活:短间隔的时间窗为 −200 至 1000 ms,长间隔为 −200 至 3000 ms。由于手部运动准备会在与运动手对侧的半球手运动皮层诱发运动相关负波,因此,正向的 C3−C4 差异波形表示左侧手运动皮层激活强于右侧,负向差异波形则表示右侧强于左侧。我们使用 Brainstorm 中实现的参数化连续双侧单样本 t 检验(与 0 比较),并在时域内采用 FDR 进行多重比较校正,以评估这些差异波形的统计显著性。
以目标刺激终点锁定的分析:N1/P2、P300 与 LPCt 成分
N1/P2 复合成分在额–中央导联池(FC1、FCz、FC2)上测量,N1 与 P2 的时间窗分别为 90–180 ms 与 180–290 ms。对每个成分,个体平均振幅被输入空间–时间相容性(Comp vs Incomp)× 时间间隔(Short vs Long)× RT 分箱(B1、B2、B3、B4)的重复测量方差分析,并用 Bonferroni 事后比较检验主效应或交互作用的显著性。
头皮地形图的目测显示:P300 与 LPCt 的起始与峰值时间会随时间间隔长度与 RT 分箱而变化。因此,我们在 Brain Analyzer 2 的半自动峰值检测算法下,测量这些成分的个体振幅与潜伏期。
对于 P300,我们选取中央–后部导联池(CP1、CP2、CPz、P1、Pz、P2):短间隔使用 300–700 ms 时间窗,长间隔使用 180–360 ms 时间窗。个体潜伏期与振幅数据输入空间–时间相容性(Comp vs Incomp)× 时间间隔(Short vs Long)× RT 分箱(B1、B2、B3、B4)的重复测量方差分析。
LPCt 从中央–额部导联池(FC1、FCz、FC2、F1、Fz、F2)提取:短间隔时间窗为 600–1300 ms,长间隔时间窗为 300–700 ms。个体振幅与潜伏期同样输入空间–时间相容性(Comp vs Incomp)× 时间间隔(Short vs Long)× RT 分箱(B1、B2、B3、B4)的重复测量方差分析。所有方差分析中,显著主效应与交互作用均通过 Bonferroni 事后比较进一步检验。
以目标刺激终点锁定的分析:侧化准备电位(C3 − C4)
与起点锁定分析相同,我们在每一种实验条件组合下(空间–时间相容性、时间间隔、RT 分箱),以 −200 至 1500 ms 的时间窗量化 C3−C4 的差异活动。差异波形的统计显著性同样通过连续双侧单样本 t 检验并以 FDR 校正,在 Brainstorm 中实现。
以手动反应锁定的分析:准备电位与侧化准备电位(C3 > C4)
准备电位(BP)按两部分计算:a)在 Cz 导联上 −600 至 −200 ms 的平均振幅,作为其负性子成分;b)在同一 Cz 导联上 −150 至 −10 ms 的平均振幅,作为其 pP1–2 复合子成分。两部分均通过手动反应(Left、Right)× 空间–时间相容性(Comp vs Incomp)× RT 分箱(B1、B2、B3、B4)的重复测量方差分析检验,并用 Bonferroni 事后比较解析显著主效应与交互作用。
由 C3 > C4 差异活动得到的 LRP 取自 −1200 至 +300 ms 的时间窗,并按与起点/终点锁定分析相同的程序进行统计评估。
结果
反应时
显著的 STEARC 仅在最慢 RT 的 B3 与 B4 中观察到(空间–时间相容性 × RT 分箱交互作用:F(3, 84)=5.3,p=.002,ƞp²=0.16;Fig. 2;B3:Comp=493.7 ms,Incomp=510.1 ms;B4:Comp=673.4 ms,Incomp=706.9 ms)。同时也观察到典型的前导期效应(ForEff):一旦时间间隔持续时间超过“短”间隔,参与者会在其终点到来前就准备将其分类为“长”。这会导致对“长”间隔的 RT 快于对“短”间隔的 RT,即 ForEff。本研究中 ForEff 体现为时间间隔主效应显著(F(1, 28)=290.7,p<.001,ƞp²=0.9;Fig. 2),对长间隔的 RT(427.1 ms)快于短间隔(557.6 ms)。一般而言,ForEff 表明:在 STEARC 任务中,参与者可以提前准备对可预测终点的“长”间隔的反应,但无法对“短”间隔的终点做同样准备。对短间隔而言,STEARC 在 B3 与 B4 的较慢 RT 中显著(空间–时间相容性 × RT 分箱交互作用:F(3, 84)=7.1,p=.0002,ƞp²=0.20;B3:Comp=564.3 ms,Incomp=590 ms;B4:Comp=727.6 ms,Incomp=763.7 ms)。对长间隔而言,STEARC 仅在最慢的 B4 中出现(空间–时间相容性 × RT 分箱交互作用:F(3, 84)=2.6,p=.05,ƞp²=0.08;Comp=619.1 ms,Incomp=650.1 ms;Fig. 2)。
反应准确性随 RT 速度而变化(F(3, 84)=18.935;p<.01;ƞp²=0.403)。Bonferroni 比较显示:与其他所有分箱相比,最慢的 B4 错误显著增加(B1=0.83;B2=0.43;B3=0.7;B4=3;p<.01)。RT 分箱 × 时间间隔交互作用显著(F(3, 84)=65.569;p<.01;ƞp²=0.200),该效应由 B4 中长时长反应准确性下降所驱动,而短时长在不同分箱间准确性无变化(Supplementary Fig. 1)。这些结果进一步确认:STEARC,即时间流逝的空间表征,仅在对时间间隔长度的决策较慢时发生,而在决策较快时不发生。
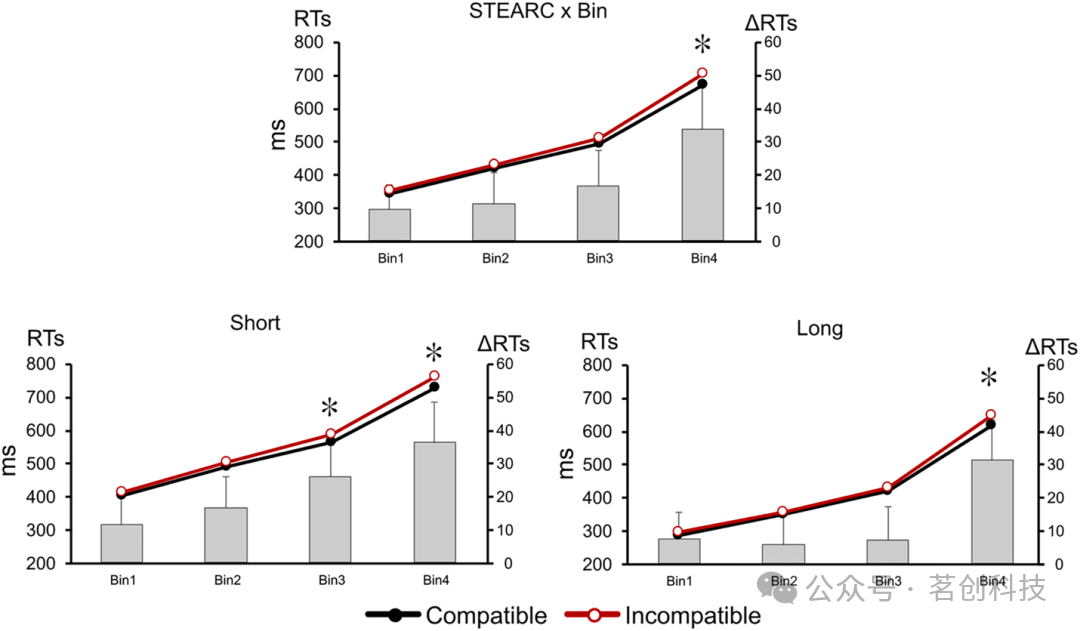
图 2. STEARC 效应随反应时(RT)速度变化的函数(短 1 秒 + 长 3 秒时间间隔:上方面板);Bin 1 为最快 RT,Bin 4 为最慢 RT。STEARC 效应在短时间间隔(下左面板)与长时间间隔(下右面板)中的表现。左侧 Y 轴:相容条件(黑线)与不相容条件(红线)的 RT。右侧 Y 轴:不相容减去相容的 RT 差值(灰色柱)。显著差异以星号标注。
EEG 结果
以时间间隔起点锁定的 EEG 活动
偶发负变(CNV)
CNV 是 EEG 中一种缓慢负向偏转,发生在第一个刺激之后,该刺激预示第二个与任务相关的刺激或动作。在时间间隔任务中,时间间隔的起点对应第一个刺激,而终点对应第二个刺激,此时 CNV 消退。最初,沿时间间隔展开的 CNV 振幅被认为反映主观计时。后续证据澄清:CNV 更可能反映用于时间计时的认知与运动资源的投入与优化;该过程受计时机制调制,但并不专门反映时间加工。在短与长时间间隔的最初 1000 ms 的晚期阶段(550–990 ms),CNV 在更快 RT 的分箱中显著更大(RT 分箱主效应:F(3, 84)=8.1,p<.001,ƞp²=0.22;Fig. 3A 与 Fig. 3B,事后比较见 Supplementary Table 1)。同样的效应也出现在长时间间隔的晚期阶段(1700–2900 ms;RT 分箱主效应:F(3, 84)=4.5,p=.005,ƞp²=0.14;Fig. 3B,事后比较见 Supplementary Table 2)。这些结果表明:在时间间隔呈现期间,CNV 的晚期成分在较慢反应试次中发展不足,而行为层面显著 STEARC 正是在这些试次中出现。
C3−C4 差异活动(LRP):时间间隔呈现期间的运动反应预激活
我们分析 C3−C4 差异活动,以评估时间间隔呈现期间,一只手相对于另一只手的预激活是否随随后反应速度而变化。未观察到显著的 C3−C4 差异活动。
以时间间隔终点锁定的 EEG 活动
N1/P2 复合成分:主观计时
N1/P2 成分的振幅反映时间间隔终点处的主观计时,此时在同一时间间隔期间发展起来的 CNV 消退。此外,N1/P2 的振幅也与目标间隔的主观时长与其比较参照之间的差异呈正相关。本研究中,N1 的振幅受 RT 速度与时间间隔长度共同调制(F(3, 84)=3.9,p=.01,ƞp²=0.11)。在短间隔中,B4 的较慢 RT 下 N1 更小(−0.22 μV),相比 B1(−0.47 μV)与 B2(−0.55 μV)更快 RT 下显著降低(Fig. 4A 与 4B)。在长间隔中,N1 振幅不随 RT 速度变化。P2 的振幅在短间隔(1.27 μV)高于长间隔(0.76 μV;F(1, 28)=4.2,p=.04,ƞp²=0.13)。时间间隔 × RT 分箱交互作用显著(F(3, 84)=3.1,p=.03,ƞp²=0.09;Fig. 4A 与 4B):在短间隔中,B1 的 P2 振幅(1.27 μV)显著大于其他所有分箱(B2=1.21 μV,B3=1.08 μV,B4=1.16 μV);长间隔中未见类似差异。
这些结果显示:在短间隔中,较浅的 N1 与 P2 反应(即主观计时更不充分)与较慢 RT 试次相关。长间隔中不存在类似效应,提示在该情形下 ForEff 有助于预测间隔终点,从而降低 N1 与 P2 对主观计时的敏感性。
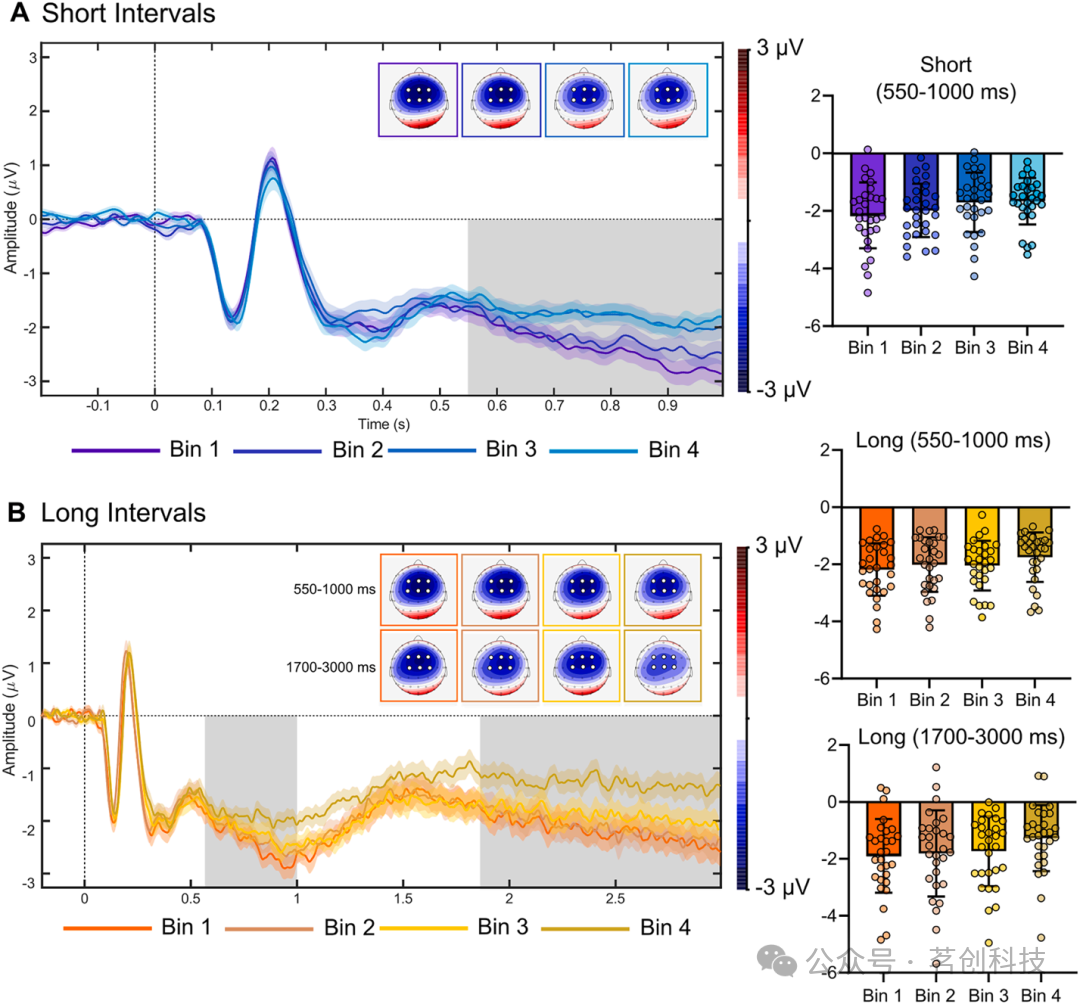
图 3. 锁定目标起始(横轴时间 0)的晚期 CNV 成分波形、头皮地形图及个体/平均振幅。时间窗:550–1000 ms(短与长时间间隔均适用),1700–3000 ms(仅适用于长时间间隔)。CNV 记录于额-中央导联(FC1、FC2、FCz、C1、Cz、C2)。图中给出了 RT 分箱 Bin 1、2、3、4 的颜色编码。(A)短 1 秒时间间隔;(B)长 3 秒时间间隔。灰色阴影表示分箱之间具有显著统计差异的时间段。
P300:比较时间间隔长度
在计时任务中,P300 标记由目标间隔与内部参照间隔的比较所激活的决策过程,因此,两者差异越大,P300 振幅越高。本研究中,P300 潜伏期在长间隔中总体短于短间隔(275.1 ms vs 479.2 ms;时间间隔主效应:F(1, 28)=244.2,p<.001,ƞp²=0.89;Fig. 5A),这很可能是 ForEff 使得长间隔终点可预测所致。在短间隔中,P300 潜伏期随 RT 变慢而增加(B1=395 ms;B2=458 ms;B3=504 ms;B4=561 ms;时间间隔 × RT 分箱交互作用:F(3, 84)=49.7,p<.001,ƞp²=0.63;Fig. 5A),而长间隔中潜伏期不随 RT 速度变化。P300 振幅在短间隔不可预测终点处更大(5.76 μV),在长间隔可预测终点处更小(3.79 μV;时间间隔主效应:F(1, 28)=26.7,p<.001,ƞp²=0.26;Fig. 5A)。同时,时间间隔 × RT 分箱交互作用显著(F(3, 84)=2.9,p=.04,ƞp²=0.09):在较慢 RT 的 B4 中(3.19 μV),P300 振幅小于较快 RT 的 B1(4.41 μV)与 B2(3.96 μV)。这些结果表明:在较慢 RT 的试次中(同时观察到显著 STEARC),短间隔的 P300 潜伏期增加,长间隔的 P300 振幅降低。上述 EEG 标记提示:目标间隔与内部比较参照之间的比较过程变慢或效能降低。
计时的晚期正成分(LPCt):支持短/长决策的证据累积
在计时任务中,LPCt 标记向“短”或“长”决策边界的证据累积过程。与 P300 相似,ForEff 使得 LPCt 在长间隔中的潜伏期短于短间隔(462.5 ms vs 914.5 ms;时间间隔主效应:F(1, 28)=936.5,p<.001,ƞp²=0.92;Fig. 5B)。此外,长间隔中 LPCt 潜伏期在不同 RT 分箱间无差异,而短间隔中 LPCt 潜伏期随 RT 变慢而逐步延长(B1=708 ms;B2=851 ms;B3=946 ms;B4=1151 ms;时间间隔 × RT 分箱交互作用:F(3, 84)=41.1,p<.001,ƞp²=0.59;Fig. 5B)。最后,无论短或长间隔,LPCt 振幅在较快 RT 时更高(B1=3.32,B2=2.49,B3=1.69,B4=−0.25;RT 分箱主效应:F(3, 84)=272.5,p<.001,ƞp²=.7;Fig. 5B)。与 P300 的结果一致,这些发现表明:较慢 RT 的试次表现为支持短/长决策的证据累积变慢或效能降低。
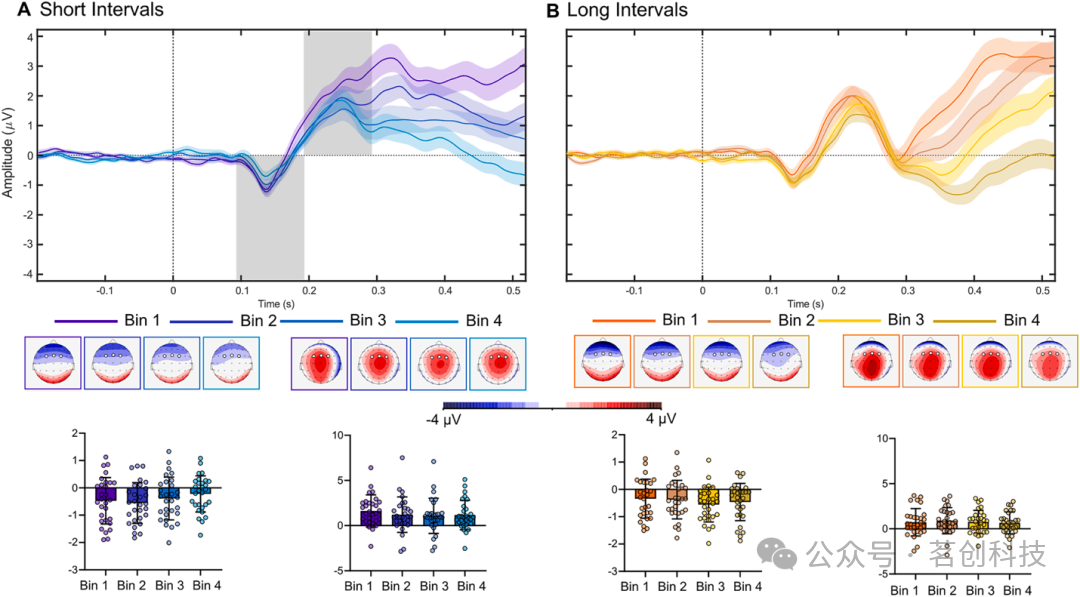
图 4. 锁定目标结束(横轴时间 0)的 N1(时间窗 90–180 ms)与 P2(时间窗 180–290 ms)成分波形、头皮地形图及个体/平均振幅。两种成分均记录于额部导联(FC1、FC2、FCz)。图中给出了 RT 分箱 Bin 1、2、3、4 的颜色编码。(A)短 1 秒时间间隔;(B)长 3 秒时间间隔。灰色阴影表示分箱之间具有显著统计差异的时间段。
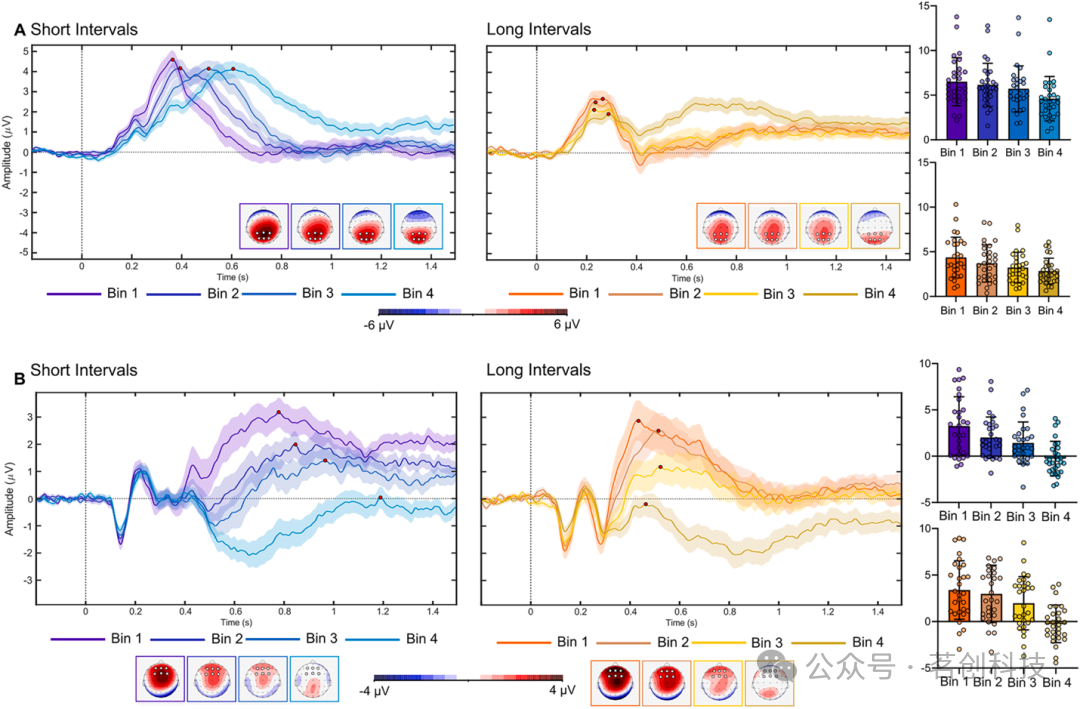
图 5. A)锁定目标结束(横轴时间 0)的 P300 成分波形、头皮地形图及个体/峰值振幅,记录于中央-顶叶导联(CP1、CP2、CPz、P1、Pz、P2)。图中给出了 RT 分箱 Bin 1、2、3、4 的颜色编码。(A)短 1 秒时间间隔;(B)长 3 秒时间间隔。红点表示平均峰值潜伏期与振幅。B)锁定目标结束(横轴时间 0)的 LPCt 成分波形、头皮地形图及个体/峰值振幅,记录于额部导联(FC1、FCz、FC2、F1、Fz、F2)。图中给出了 RT 分箱 Bin 1、2、3、4 的颜色编码。(A)短 1 秒时间间隔;(B)长 3 秒时间间隔。红点表示平均峰值潜伏期与振幅。
C3−C4 差异活动(LRP):时间间隔终点处的运动反应预激活
以时间间隔终点锁定的 LRP 捕捉从时间间隔编码到选择时长反应之间的过程持续时间。本研究中,在短间隔 Comp 与 Incomp 条件下,目标终点后 180–240 ms 观察到初始左手激活(Fig. 6A)。在 Incomp 试次中(例如“间隔短时按左键”),该初始左手激活在目标终点后 260–500 ms 被右手激活所取代(Fig. 6A)。在长间隔 Comp 试次中,目标终点后 240–350 ms 出现右手激活(Fig. 6A)。在长间隔 Incomp 试次中,目标终点后 180–240 ms 出现显著左手激活。
此外,我们通过一系列配对 t 检验,在显示显著 C3−C4 差异活动的时间窗内,进一步考察 LRP 振幅随 RT 速度的变化。在所有类型试次中,反应手相对于非反应手的预激活在较慢 RT 分箱中降低(见 Fig. 6B 与 Supplementary Tables 3 和 4)。这表明:从时间间隔结束到选择并激活运动反应这一阶段,较慢 RT 的试次(即出现 STEARC 的试次)表现为反应手相对非反应手的运动预激活界定不清。
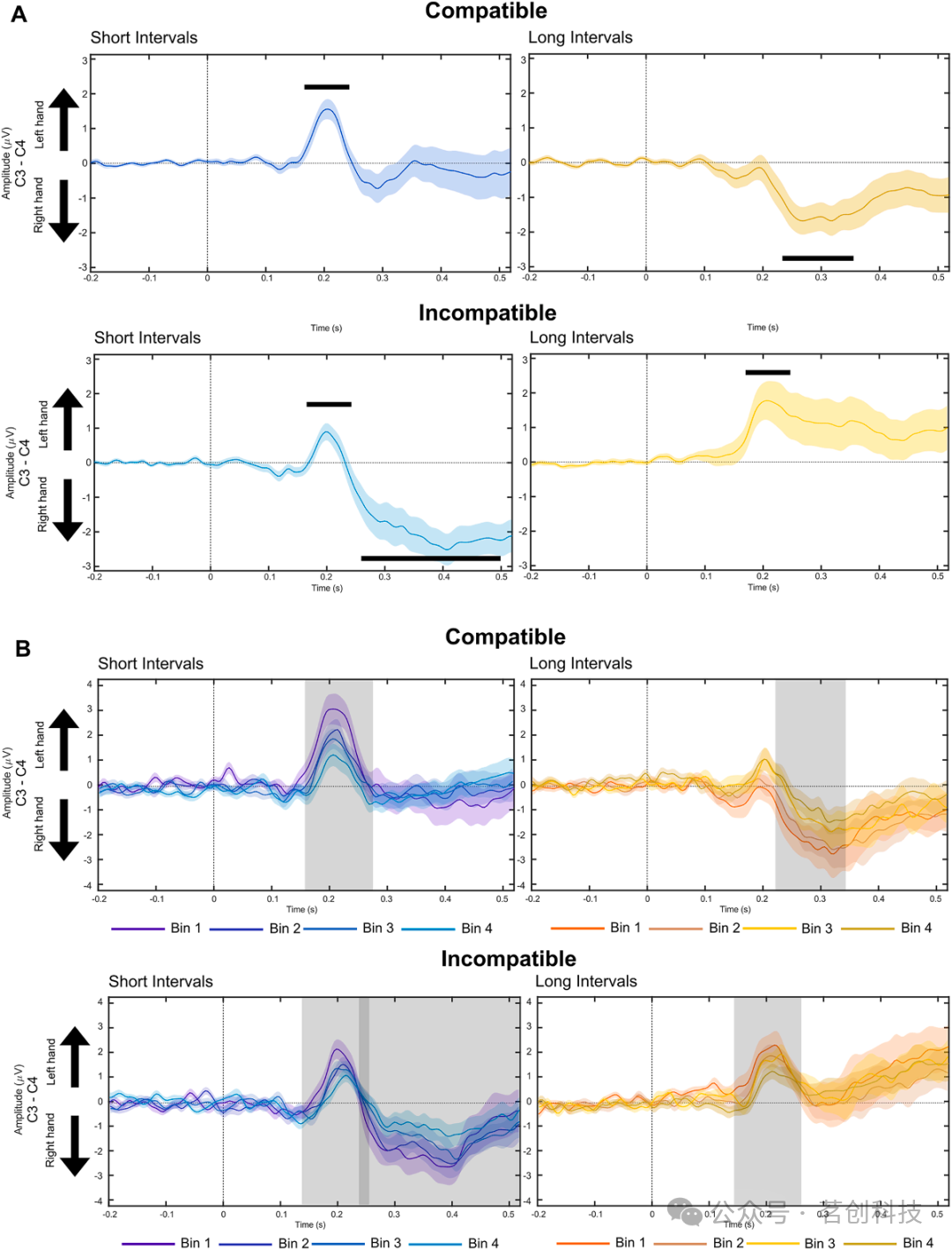
图 6. A)锁定目标结束(横轴时间 0)的差异性 C3 > C4 LRP 波形:在相容与不相容条件下,短 1 秒(蓝线)与长 3 秒(黄线)时间间隔。B)锁定目标结束(横轴时间 0)的差异性 C3 > C4 LRP 波形:在相容与不相容条件下,短 1 秒(蓝线)与长 3 秒(黄线)时间间隔随 RT 分箱的变化。图中给出了 RT 分箱 Bin 1、2、3、4 的颜色编码。灰色阴影表示分箱之间具有显著统计差异的时间段。
以手动反应锁定的 EEG 活动
准备电位(BP):反应准备与激活
BP 反映与运动准备相关的皮层兴奋性,并起源于扣带皮层与辅助运动皮层。BP 的特征是一个在运动开始前 1–2 秒启动的长前导负性成分。该负性成分之后,在运动开始前 100–150 ms 出现一个短暂的 pP2 正波,其起源于前岛叶,并反映用于对目标刺激进行分类的感觉证据累积。本实验中,长前导负性成分的振幅随时间间隔长度与 RT 速度变化(F(3, 84)=11.4,p<.001,ƞp²=0.36)。在短间隔中,B1 的该成分更强(−1.2 μV),显著大于其他分箱(B2=−0.29 μV;B3=0.16 μV;B4=0.37 μV)。表面上相反,在长间隔中,该成分在 B4 的较慢 RT 时更大(−0.55 μV),并显著大于其他所有分箱(B1=−0.13 μV;B2=−0.04 μV;B3=−0.02 μV;见 Fig. 7)。这一看似悖论的结果可由对短暂 pP2 子成分的分析澄清。pP2 在短间隔中更大(1.4 μV),在长间隔中更小(0.1 μV;F(1, 28)=10.6,p=.002,ƞp²=0.27),并随间隔长度与 RT 速度共同变化(F(3, 84)=3.03,p=.03,ƞp²=0.09)。在短间隔中,pP2 在最慢的 B4 中选择性降低(0.67 μV),低于其他所有分箱(B1=1.45 μV;B2=1.69 μV;B3=1.77 μV)。在长间隔中,pP2 在 B2(0.41 μV)小于 B1(0.92 μV),在 B3 变为接近 0(−0.11 μV),在 B4 则转为负向下陷,该下陷延长了此前的长负性成分,从而造成其振幅与持续时间看似“增强”(−1.16 μV;见 Fig. 7)。综合而言,BP 的分析表明:较慢 RT 的试次对应于运动反应准备阶段皮层兴奋性的缺陷与延迟。
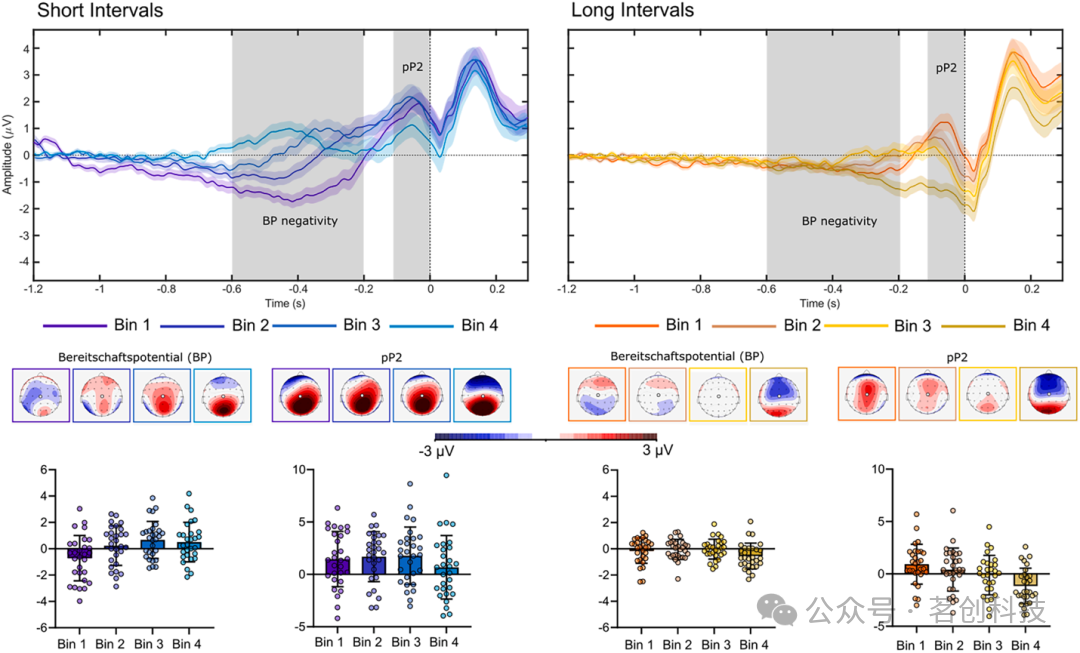
图 7. 锁定手动反应(横轴时间 0)的 Bereitschaftspotential(准备电位)负成分与 pP1 成分的波形、头皮地形图及个体/平均振幅(时间窗 600–200 ms 与 150–10 ms;Cz 导联),分别对应短(A)与长(B)时间间隔。图中给出了 RT 分箱 Bin 1、2、3、4 的颜色编码。灰色阴影表示分箱之间具有显著统计差异的时间段。
C3−C4 差异活动(LRP):反应起点处的运动反应预激活
以反应锁定的 LRP 反映反应激活与外周运动过程的持续时间。在短间隔 Comp 试次中,左手激活在反应前 170 ms 开始;在长间隔 Incomp 试次中,左手激活在反应前 185 ms 开始(Fig. 8A)。与左手反应相比,右手反应显示更长的准备过程。在长间隔 Comp 试次中,可能由于 ForEff 使“长”判断可被提前预期,右手激活在反应前约 280 ms 就开始;相反,在短间隔不相容试次中,由于时间间隔终点不可提前预期,右手预激活更短,仅在反应前 210 ms 开始(Fig. 8A)。
随后,我们在显示显著 C3−C4 差异活动的时间窗内,通过一系列 t 检验进一步考察 LRP 随 RT 速度的变化。对于右手反应,B4 的 LRP 起始早于其他所有分箱;对于左手反应,B4 的 LRP 更大(见 Fig. 8B)。这些结果表明:较慢 RT 出现 STEARC 的同时,反应锁定的 LRP 更大且持续更久。这种更长的反应准备持续时间反过来补偿了同一试次中在时间间隔终点处观察到的 LRP 发展不足(见上一节结果)。
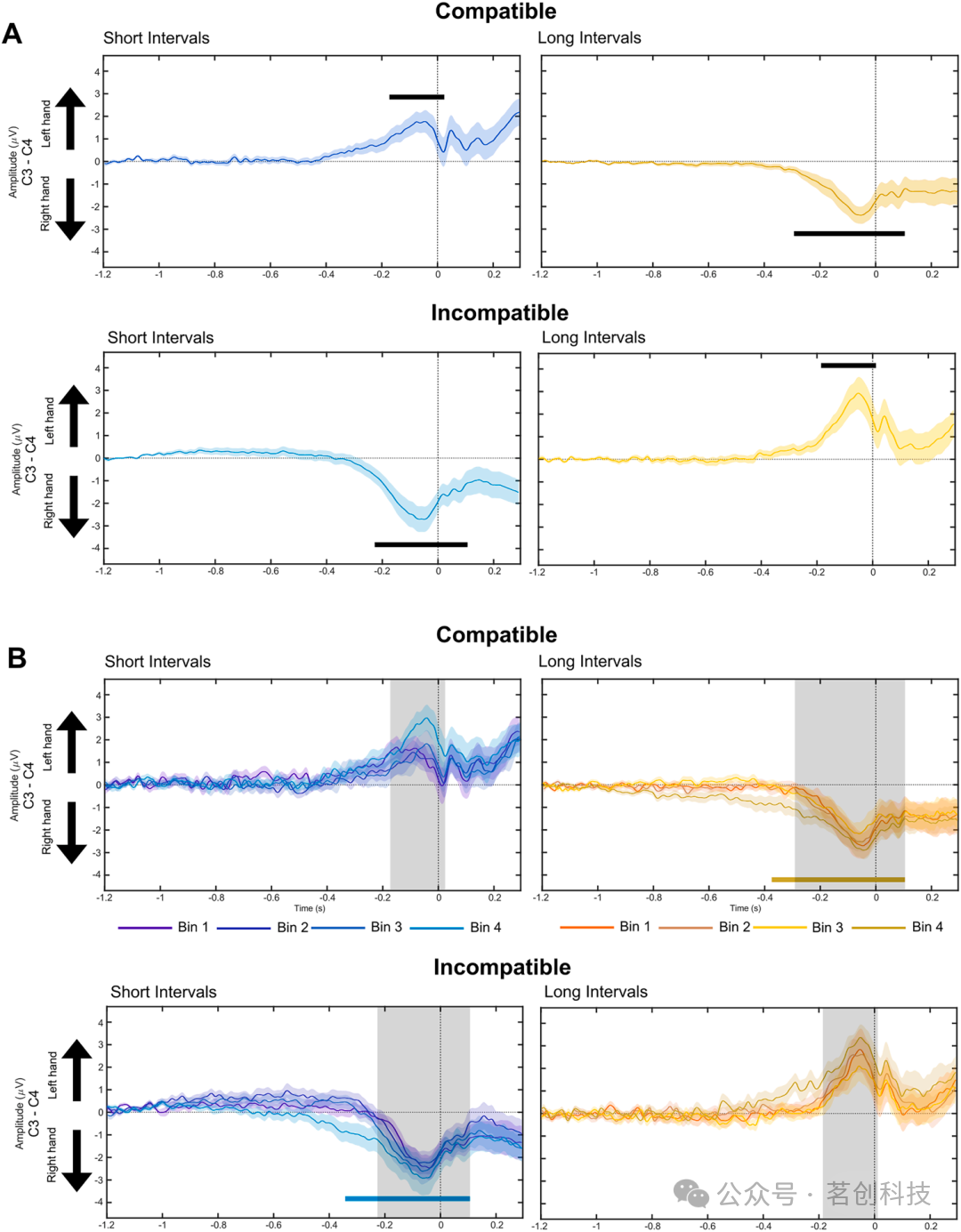
图 8. A)锁定手动反应(横轴时间 0)的差异性 C3 > C4 LRP 波形:在相容与不相容条件下,短 1 秒(蓝线)与长 3 秒(黄线)时间间隔。B)锁定手动反应(横轴时间 0)的差异性 C3 > C4 LRP 波形:在相容与不相容条件下,短 1 秒(蓝线)与长 3 秒(黄线)时间间隔随 RT 分箱的变化。图中给出了 RT 分箱 Bin 1、2、3、4 的颜色编码。灰色阴影表示分箱之间具有显著统计差异的时间段。蓝色与黄色粗条表示 C3 > C4 振幅差异具有统计显著性的时间段。正差值 = 左手相对右手的预激活更强;负差值 = 右手相对左手的预激活更强。
讨论
本研究表明,由 STEARC 效应揭示的时间空间表征与多种 EEG 反应的变化相对应。更具体而言,手动 RT 中观察到的 STEARC 是一个级联式过程的结果,该过程从时间间隔的编码阶段开始。首先,时间间隔终点前的 CNV 晚期阶段振幅更浅,与较慢 RT 以及 STEARC 的出现相关。对于长时间间隔,CNV 在第一秒末(即预期短间隔可能结束的时点)形成平台,随后减弱并在间隔结束前再次上升。这种双相趋势提示:1 秒的“短”时长被作为准备“长”判断的锚点。这进一步说明:CNV 与其说反映时间脉冲的累积(若如此,长间隔中 CNV 振幅应沿时长线性增长),不如说反映在间隔终点到来前对认知与资源的优化。最后,CNV 的早期 N1/P2 成分(标记启动计时的精确性)与后续长负性成分之间,并未随 RT 速度呈现关联。
在短间隔的终点处,N1/P2 复合成分的较大振幅与较快 RT(未出现 STEARC)相关。由于 N1/P2 反映目标间隔时长与其比较参照之间的主观差异,该结果表明:更快的短间隔分类与其主观时长的缩短相关。相反,在长间隔中,N1/P2 振幅不随 RT 速度变化,这很可能源于 ForEff 使参与者能在终点到来前就作出“长”判断,同时也表明策略性因素可降低 N1/P2 的振幅及其对主观计时的敏感性。
顶叶晚期 P300 与额部计时晚期正成分(LPCt)与证据累积过程相关,它们共同参与确定时间间隔长度的决策边界。当时间间隔短于边界时,这些成分更大,因为决策过程必须持续到间隔结束;而对长间隔而言,由于可以在终点之前就做出决策,这些成分更浅。在本研究中,较慢 RT 的试次(即行为层面出现 STEARC 的试次)表现为:短间隔的 P300 潜伏期更长,以及长间隔的 P300 振幅更小。P300 源自一个包含多个脑区的网络,其中一个关键节点是颞顶联合区(TPJ),该区域用于指示预期与实际感觉运动及认知事件之间的匹配/不匹配信号。这提示:在计时任务中,P300 标记目标间隔与比较参照之间的主观匹配/不匹配;对短间隔而言,当出现 STEARC 且 P300 潜伏期更长时,匹配/不匹配信号的释放被延迟;对长间隔而言,ForEff 削弱了终点处匹配/不匹配信号的重要性,从而降低相应 P300 的振幅。
无论短或长间隔,在 STEARC 出现的最慢 RT 中均未观察到 LPCt。该下降与短间隔中 P300 的晚期发展、以及长间隔中 P300 的持续活动相对应,仿佛 P300 的发展干扰了随后的 LPCt。鉴于 LPCt 的功能定位,该下降提示刺激–反应规则的选择发生在更晚且存在缺陷。这一推断与另一个发现一致:STEARC 也出现在运动反应晚期动员的试次中,表现为准备电位(BP)降低或缺失。这种降低同时影响了 BP 的长负性成分(起源于扣带与辅助运动皮层)以及较晚的短暂 pP2 成分(起源于前岛叶)。
既往研究曾将 STEARC 与时间间隔呈现期间及之后的 LRP(C3−C4 差异活动)振幅变化联系起来。基于此,一个可能的预期是:LRP 越大,STEARC 越强。然而,与这一预期相反,我们发现:随着较慢 RT 中 STEARC 的逐步建立,反映相容反应激活的 LRP 振幅相对于反映不相容反应的 LRP 振幅并非增加,而是降低(Fig. 9)。该结果提示:当相容反应手的准备有效且非反应手的反应受到良好抑制时,反应更快且 STEARC 不发生。这个新且看似反直觉的发现值得进一步研究,因为 LRP 在 STEARC 中具有重要作用。举例而言,近期有研究考察了对时间间隔的“短/长”反应的运动准备,但其未在被试内平衡相容与不相容的时间–空间反应映射,因此目前无法从其数据中提取干净的 STEARC 运动准备相关指标,并与本研究结果直接对照。
STEARC 的 EEG 相关指标的统一解释
应如何理解 STEARC 多方面的 EEG 相关指标?在此我们提出:一种统一解释可能基于内侧前额叶皮层(MPFC)与儿茶酚胺系统(多巴胺 DA 与去甲肾上腺素 NE)的相互作用在动机、注意、认知控制与计时中的作用。近期的神经–计算模型提出:MPFC 与脑干核团之间的环路会根据任务需求、动机与认知投入的期望价值来优化儿茶酚胺释放;这种优化基于学习去控制受儿茶酚胺影响的内部变量(如努力、神经可塑性与注意),即元学习。这些模型提示:在 STEARC 这类任务中,MPFC 向儿茶酚胺脑干核团发出的控制信号增强,会导致更高的 DA 与 NE 释放,从而改善时间间隔编码、加快对其长度的决策与反应选择,并产生更短 RT。关键在于,儿茶酚胺释放的优化是随机过程,即在环境变量保持恒定时,优化会在试次间波动,从而决定 RT 与 EEG 反应的变异性。这些波动可能反映在源自 MPFC 的 CNV 振幅上,因为 MPFC 是驱动元学习优化的神经模块(see Fig. 10)。概括而言,该解释提出一个形式化假设:MPFC 控制信号的试次间变异与儿茶酚胺释放的变异以及 RT 的变异相关联。
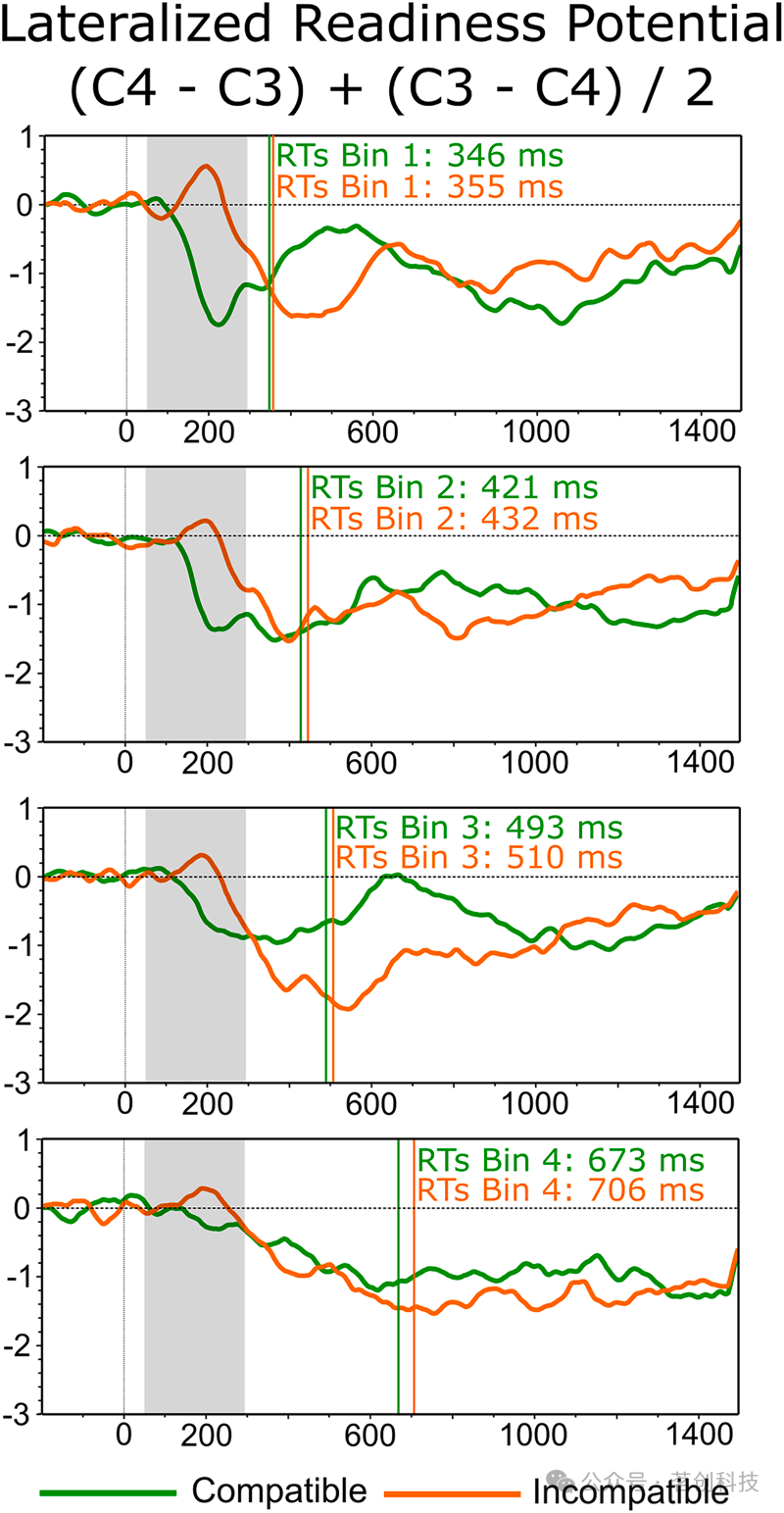
图 9. 差异性 C3 > C4 LRP 波形:在 Bin 1(上排)至 Bin 4(下排)中,将左右手平均后,锁定时间间隔结束(横轴时间 0),相容条件(绿线)与不相容条件(橙线)的比较。灰色阴影表示具有显著统计差异的时间段。垂直线表示各分箱的平均手动 RT。
与这一解释一致,我们发现:与 STEARC 同时出现的计时决策变慢的最初标记,是 CNV 振幅下降,即 MPFC 向脑干控制信号下降的 EEG 指标(Fig. 10)。由于 DA 水平与 CNV 振幅相关,可以推断:在 CNV 较浅、RT 较慢且 STEARC 显著的试次中,存在 DA 活动的相位性下降以及认知资源优化不足。DA 的下降也会减慢时间脉冲的累积,导致对时间长度的低估。本研究发现:较慢 RT 与 STEARC 与 N1/P2 复合成分振幅降低相关,而 N1/P2 指示时间间隔的主观时长。这提示:在 CNV 编码阶段 DA 活动的下降影响了 N1/P2 所反映的时间间隔主观时长。最后,DA 与 NE 也共同调制 P300 成分;在多种情况下,较低的 DA 或 NE 活动会降低 P300 振幅,而对潜伏期的影响仍不明确。本研究中,与 STEARC 相匹配的计时决策变慢与短间隔的 P300 潜伏期延长、以及长间隔的 P300 振幅降低相关,这同样与 STEARC 对应儿茶酚胺能活动降低的假设相容。
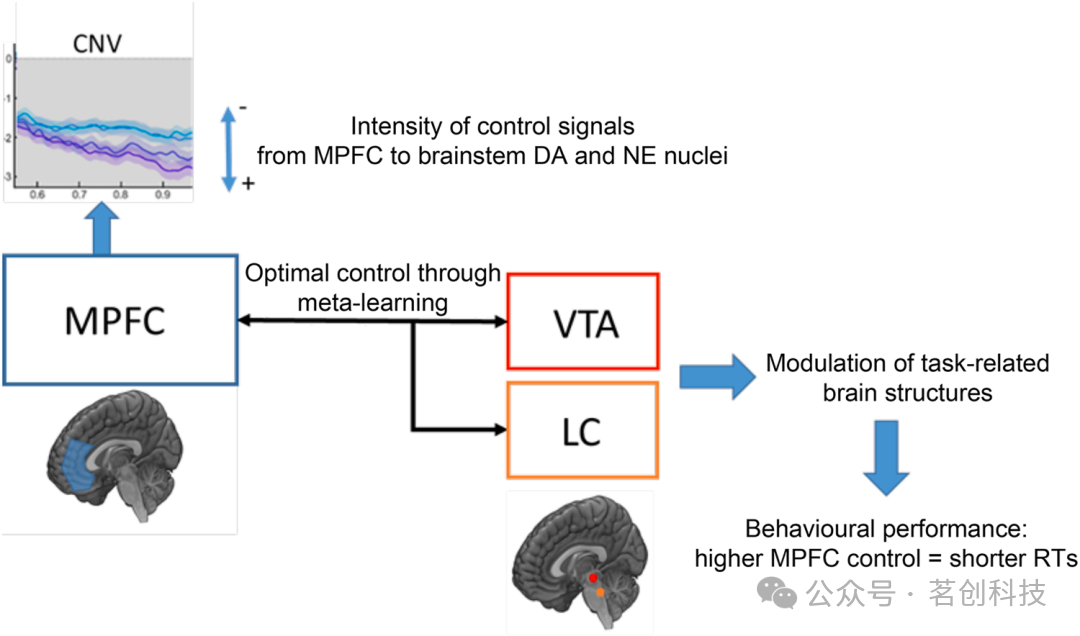
图 10. MPFC-儿茶酚胺系统模型及其在行为表现中的作用。MPFC(内侧前额叶皮层,Medial Prefrontal Cortex),VTA(腹侧被盖区,Ventral Tegmental Area,多巴胺发放核团),LC(蓝斑核,Locus Coeruleus,去甲肾上腺素发放核团),DA(多巴胺,Dopamine),NE(去甲肾上腺素,Norepinephrine)。
结论
阅读、书写与环境观察等文化实践,会对感觉运动与认知事件施加序列化与空间化的排序,不仅影响一系列时间事件的编码,也影响数列的学习。这些学习经历通过纳入视觉–空间特征来增强大脑对时间与数字的表征。人类文化与科学史提供了大量例证,说明视觉–空间表征的时间与数字如何帮助并塑造人类理解、解释并赋予环境意义的能力;相对论中“时空弯曲”就是著名例子。尽管如此,近期行为证据显示:沿从左到右组织的心理时间线对连续时间刻度的心理排列,以及沿心理数字线对数字的排列,并非大脑对时间或数字的内在表征。相反,这类排列更可能由以下因素触发:a)在当前任务中使用空间化反应编码;b)存在侧化的空间可供性,例如左右手臂挥动以指示过去与未来;c)出现操作符号(例如“+”“−”),从而重新激活对加减运算的过度学习的从左到右心理表征。本研究结果进一步强化这一结论:即便在任务中使用左/右空间反应编码来分类时间间隔长度,当计时决策足够快时,对应的从左到右心理时间表征仍会被绕开。最后,我们提出:基于元学习的注意资源部署优化,并由包含 MPFC 与儿茶酚胺核团的皮层–皮层下环路实现,可能构成 STEARC 神经特征的基础。这些发现为理解支撑人类广泛使用时间流动的心理空间表征的大脑机制提供了新线索,并可能为分别研究非空间化与空间化的计时脑机制提供新工具。
参考文献
Doricchi, F., Scozia, G., Pinto, M., Lozito, S., Lo Presti, S., Pazzaglia, M., Silvetti, M., & Lasaponara, S. (2026). EEG reveals how space acts as a late heuristic of time. NeuroImage, 326, 121710.

AtomGit 是由开放原子开源基金会联合 CSDN 等生态伙伴共同推出的新一代开源与人工智能协作平台。平台坚持“开放、中立、公益”的理念,把代码托管、模型共享、数据集托管、智能体开发体验和算力服务整合在一起,为开发者提供从开发、训练到部署的一站式体验。
更多推荐
 已为社区贡献1条内容
已为社区贡献1条内容







所有评论(0)