Acad Radiol(IF=3.9)深圳市人民医院超声科董发进等团队:基于纵向超声Delta放射组学的乳腺癌新辅助化疗肿瘤反应早期分层预测研究
01
文献学习

今天分享的文献是由深圳市人民医院超声科董发进等团队于2025年12月在《Academic Radiology》(中科院2区,IF=3.9)上发表的研究“Longitudinal Ultrasound Delta Radiomics for Early Stratified Prediction of Tumor Response to Neoadjuvant Chemotherapy in Breast Cancer”即基于纵向超声Delta放射组学的乳腺癌新辅助化疗肿瘤反应早期分层预测研究,该研究基于233例接受新辅助化疗的乳腺癌患者,提取治疗前和第二周期后的超声图像中的放射组学特征,构建了两个Delta模型(Delta_resistance 和 Delta_PCR),分别用于预测化疗抵抗和病理完全反应。模型在测试集中的AUC分别达到0.917和0.936,显著优于单时间点模型。SHAP分析增强了模型的可解释性。研究结果表明,纵向超声Delta放射组学可用于早期分层预测乳腺癌NAC反应,指导个体化治疗。
创新点:①双任务分层预测框架:首次同时构建化疗抵抗与病理完全缓解两个Delta模型,实现精细化风险分层,超越单一二分类预测。②纵向超声Delta特征:基于治疗前与第二周期后超声图像的相对变化特征,动态捕捉肿瘤异质性演变,显著优于单时间点模型。③SHAP可解释性集成:应用博弈论SHAP方法实现全局与个体预测的透明解释,破解黑箱问题,增强临床信任度。
临床价值:①早期识别耐药患者:Delta_resistance模型AUC达0.917,助力及时调整无效化疗,避免毒性暴露与疾病进展风险。②精准预测病理完全缓解:Delta_PCR模型AUC达0.936,为保乳手术及降阶梯治疗提供客观依据,优化个体化方案。③无创动态监测工具:基于常规超声影像,低成本、无辐射、可重复,在早期治疗窗口实现疗效动态评估。
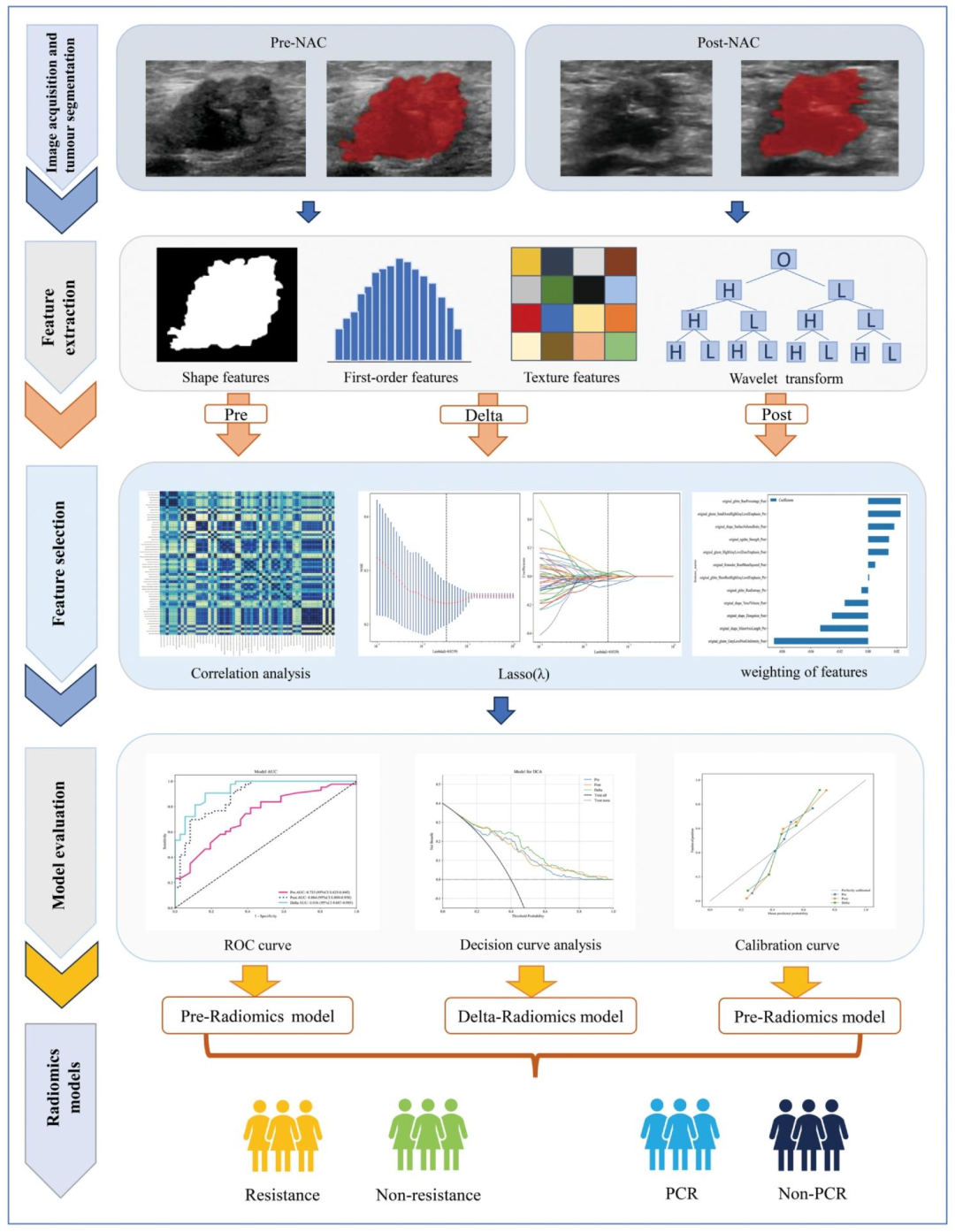
图 2:Delta影像组学模型构建流程概览
图像输入:分为Pre-NAC(治疗前)、Post-NAC(2周期后)两个时间点的超声图像。
特征提取
提取类型:形状特征、一阶特征、纹理特征、小波变换特征;
单时间点提取:Pre组学特征、Post组学特征;
Delta特征计算:RF_Delta=(RF_Pre–RF_Post)/RF_Pre(核心:量化治疗前后特征的相对变化)。
特征筛选:Pearson相关性分析去共线性→LASSO回归加权降维(10折交叉验证)。
模型构建:同步构建3类模型
Pre模型:仅用治疗前特征;
Post模型:仅用2周期后特征;
Delta模型:融合前后特征的变化值(研究核心模型)。
模型评估:ROC曲线、决策曲线分析(DCA)、校准曲线。
输出结果:化疗耐药/非耐药、pCR/非pCR分层预测。
02
研究背景和目的
研究背景
乳腺癌是全球女性癌症相关发病率和死亡率的主要原因之一。新辅助化疗(NAC)作为乳腺癌的重要治疗策略,能够显著缩小肿瘤、降低分期并提高保乳手术的成功率。然而,由于乳腺肿瘤存在显著的遗传异质性,不同患者对NAC的反应差异极大,部分患者获益有限,甚至面临治疗延迟、疾病进展和治疗相关毒性增加的风险。因此,早期、准确地评估NAC疗效对于实现个体化治疗、及时调整化疗方案、避免无效治疗至关重要。目前临床常用的评估方法包括基于形态学变化的RECIST标准和基于术后标本的病理学评估(如Miller-Payne分级系统)。RECIST易受观察者变异影响,且难以捕捉肿瘤内部的异质性和多样化的消退模式;病理评估虽准确,但需在化疗结束后进行,无法用于早期监测。影像学技术中,乳腺X线摄影对致密型乳腺敏感性有限,磁共振成像(MRI)成本高且存在禁忌,而超声检查虽具有低成本、无辐射、实时成像等优势,但其评估主要依赖于二维形态特征,同样面临观察者变异和无法反映肿瘤动态变化的局限。近年来,放射组学作为一种非侵入性图像分析方法,能够从医学图像中提取大量定量特征,捕捉常规影像解读无法识别的肿瘤异质性。然而,多数现有放射组学研究基于单时间点成像,忽略了治疗过程中肿瘤特征的动态变化。因此,基于治疗前和早期治疗(第二个周期后)的纵向超声图像,构建Delta放射组学模型,有望更全面地反映肿瘤生物学演变,从而提高NAC反应预测的准确性。
研究目的
本研究旨在开发和评估基于纵向超声图像的Delta放射组学模型,用于乳腺癌患者新辅助化疗(NAC)反应的早期分层预测,从而支持个体化治疗决策。具体而言,研究构建了两个独立的预测模型:一是Delta_resistance模型,用于预测化疗抵抗(即对NAC不敏感的患者);二是Delta_PCR模型,用于预测病理完全缓解(PCR),即识别有望达到PCR的患者。通过比较Delta模型与单时间点模型(仅治疗前或仅早期治疗后)的预测性能,验证整合治疗前后动态变化的放射组学特征能否显著提高预测准确性。研究纳入233例接受NAC的乳腺癌患者,提取治疗前和第二个周期后的超声图像中的放射组学特征,计算Delta特征(定义为RF_Pre - RF_Post)/ RF_Pre,并采用LASSO回归进行特征选择,结合多种机器学习分类器(如随机森林、逻辑回归等)构建模型。模型的判别性能通过曲线下面积(AUC)、敏感性、特异性等指标评估,同时引入SHAP可解释性分析,量化各特征对预测结果的边际贡献,增强模型的透明度和临床可信度。最终目标是:一方面帮助临床医生早期识别化疗抵抗患者,及时调整治疗方案,避免不必要的毒性暴露;另一方面精准筛选可能达到PCR的患者,为实施降阶梯治疗和优化手术策略提供依据,从而推动乳腺癌新辅助化疗管理的精准化和个体化。
03
数据和方法
研究数据
样本量:333例乳腺癌患者(训练集233,测试集100)
影像数据:治疗前 + 第2周期NAC后超声图像
病理数据:ER、PR、HER2、Ki-67、分子分型、MP分级
标签定义:
抵抗:MP G1–G3
pCR:MP G5
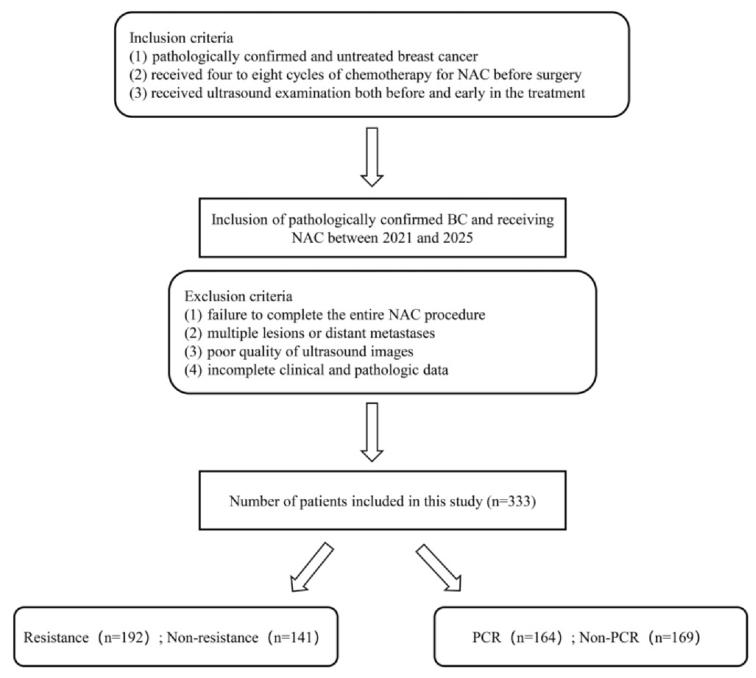
图 1:患者纳入与排除流程图
技术方法
图像分割:ITK-SNAP手动勾画ROI
特征提取:PyRadiomics,共214个特征(形状、一阶、纹理等)
特征筛选:
ICC > 0.8(一致性)
统计检验(P < 0.05)
Pearson相关系数 > 0.9 去冗余
LASSO回归 + 10折交叉验证
Delta特征计算:(RF_Pre - RF_Post) / RF_Pre
模型构建:6种机器学习分类器,最终选用RandomForest
模型评估:AUC、ACC、SEN、SPE、PPV、NPV、DCA
可解释性分析:SHAP(全局 + 局部)
04
实验结果
Delta_resistance模型(RandomForest):
测试集AUC = 0.917,SEN = 0.854,SPE = 0.846
优于Pre和Post模型
Delta_PCR模型(RandomForest):
测试集AUC = 0.936,SEN = 0.884,SPE = 0.833
优于Pre和Post模型
SHAP分析显示,关键特征如GrayLevelNonUniformity_Post、SurfaceVolumeRatio_Post等对预测贡献最大
亚组分析显示模型在不同分子分型中表现稳定
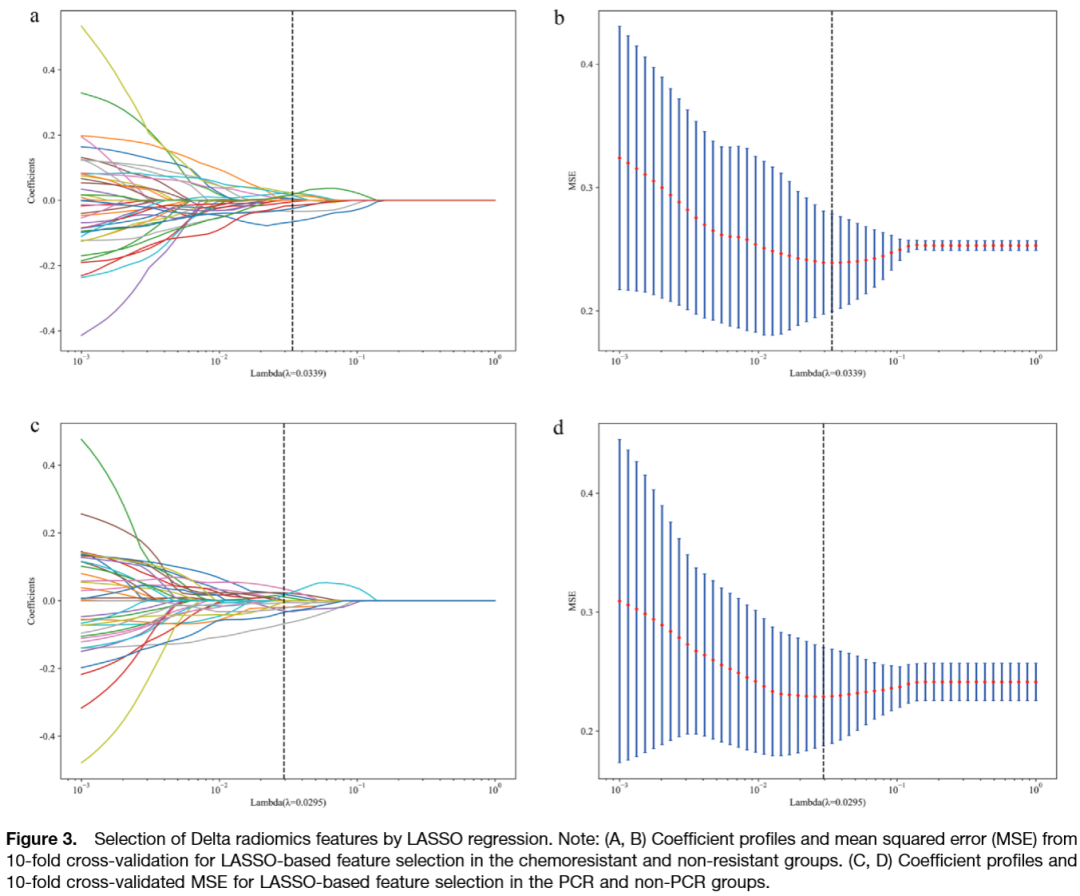
图 3:LASSO回归筛选Delta影像组学特征
该图包含A、B、C、D四个子图。A和B对应耐药预测任务:A图为系数随惩罚参数λ变化的路径图,随着λ增大,部分特征系数被压缩至零;B图为10折交叉验证的均方误差随λ变化曲线,红色虚线标出最佳λ值。C和D对应病理完全缓解预测任务,同样展示系数路径和交叉验证误差曲线。最终耐药模型筛选出10个Delta特征,pCR模型筛选出14个Delta特征,有效控制了过拟合风险。
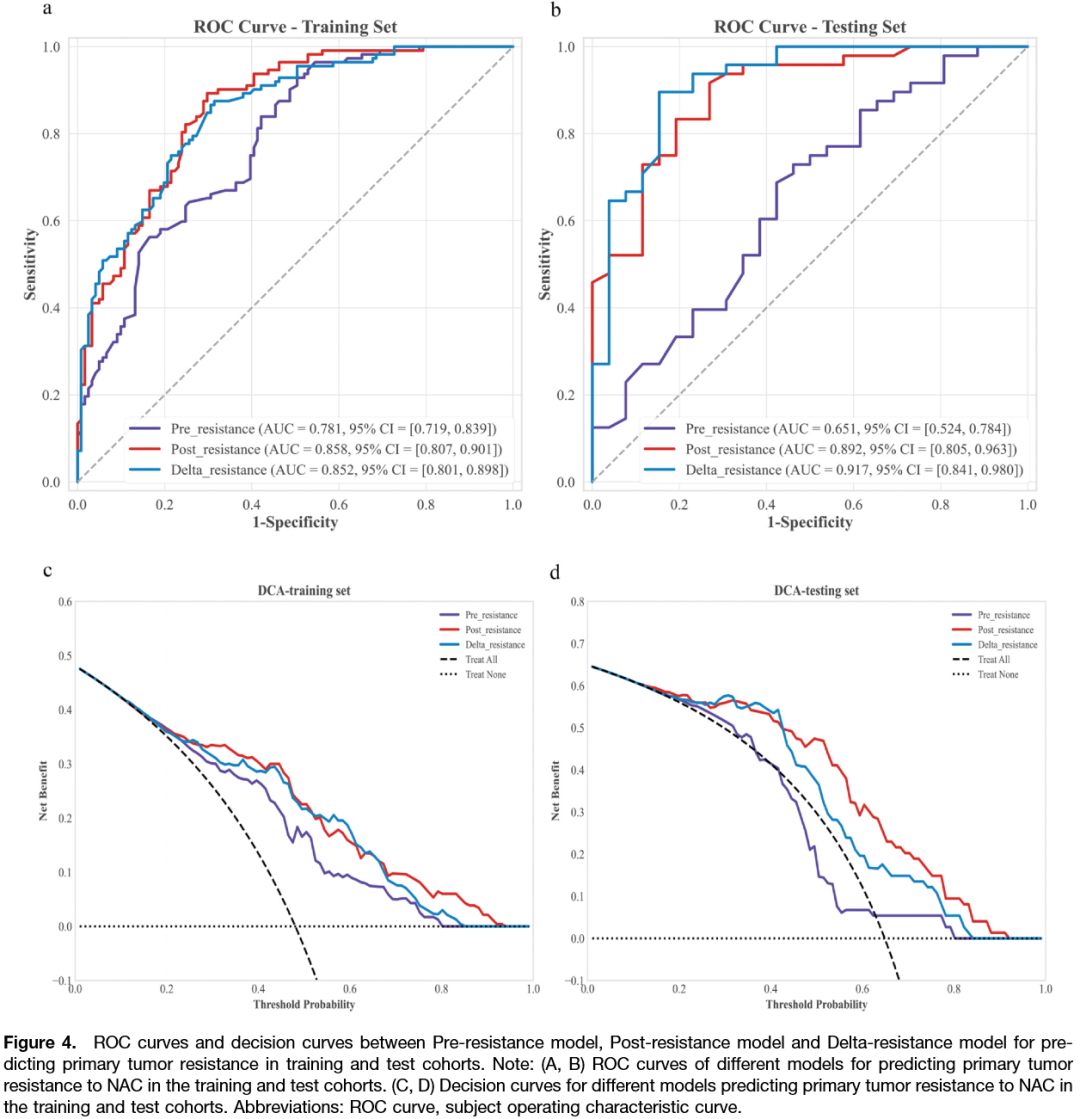
图 4:Delta耐药模型的ROC曲线与决策曲线
该图对比了三种模型(仅治疗前特征、仅早期治疗后特征、Delta联合特征)在预测化疗耐药中的表现。A和B为训练集和测试集的ROC曲线:Delta模型在测试集中AUC达0.917,显著优于Pre模型的0.651和Post模型的0.892。C和D为决策曲线分析,纵轴表示净获益,横轴为阈值概率。Delta模型(红色曲线)在较宽阈值范围内均高于其他两条曲线,表明其具有最佳的临床净获益,可作为识别耐药患者的可靠工具。
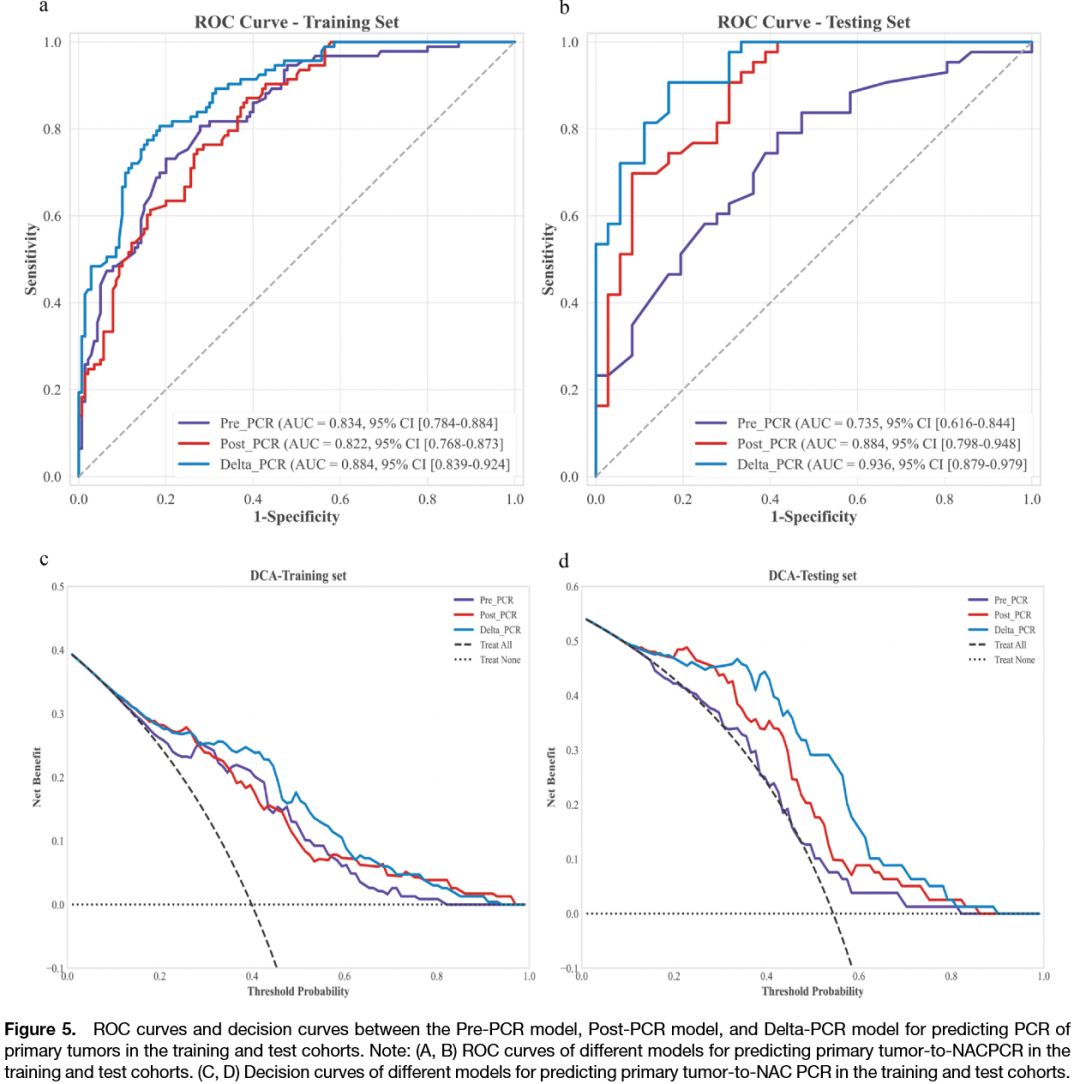
图 5:Delta pCR模型的ROC曲线与决策曲线
该图比较了三个模型预测病理完全缓解的能力。A和B为ROC曲线:Delta模型在测试集中AUC达0.936,灵敏度0.884、特异度0.833,显著优于Pre模型(AUC 0.735)和Post模型(AUC 0.884)。C和D为决策曲线:Delta模型(红色)在大部分阈值概率下净获益最高,尤其在高阈值区域优势更明显。这表明联合治疗前后动态特征的Delta模型不仅能有效区分pCR与非pCR患者,还能为降阶梯治疗和手术方案优化提供影像学依据。
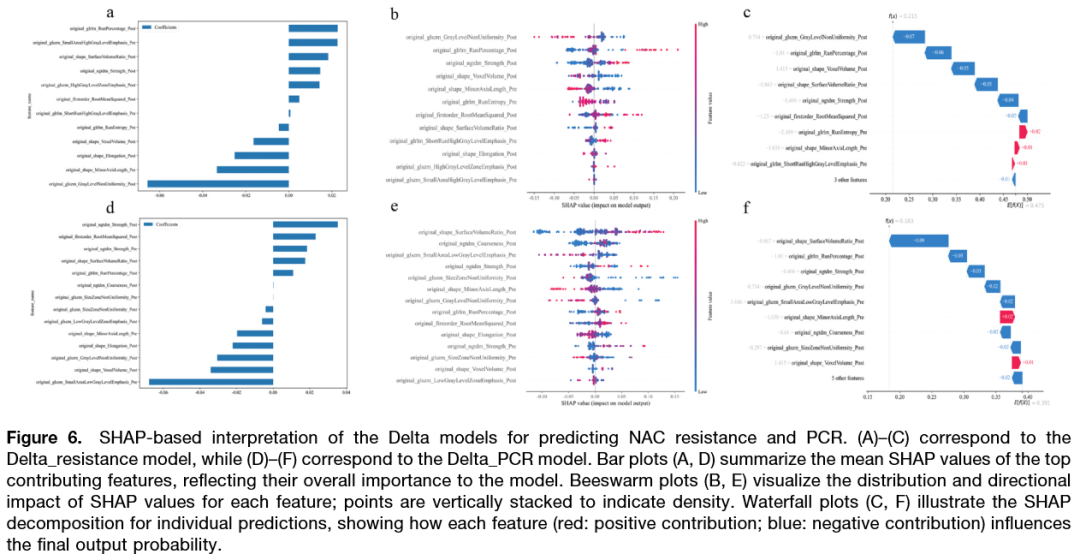
图 6:SHAP模型可解释性分析
该图分为左右两部分:左列(A-C)对应耐药模型,右列(D-F)对应pCR模型。A和D为条形图,展示全局特征重要性排序,耐药模型中贡献最大的特征是“_Post”后缀的治疗后特征(如GrayLevelNonUniformity)。B和E为蜂群图,显示每个特征SHAP值的分布及与预测结果的正负相关方向。C和F为瀑布图,针对单个患者展示各特征如何将基线预测概率(E[f(x)])逐步推高或拉低至最终输出值,实现了个体化预测逻辑的可视化,增强了“黑箱”模型的临床可信度。
05
研究结论
基于超声影像的Delta放射组学模型能够在新辅助化疗(NAC)早期(第二个化疗周期后)对乳腺癌患者的治疗反应进行精准分层预测。研究构建了两个主要模型:Delta_resistance模型用于预测化疗耐药性,在测试集中AUC达0.917,敏感性和特异性分别为0.854和0.846;Delta_PCR模型用于预测病理完全缓解(PCR),AUC达0.936,敏感性0.884、特异性0.833。两个模型均显著优于单时间点(治疗前或治疗后)模型,证明了动态影像特征变化在反映肿瘤生物学演变中的关键价值。此外,研究引入SHAP可解释性分析,揭示了如GrayLevelNonUniformity、SurfaceVolumeRatio等关键放射组学特征对预测结果的贡献,增强了模型的临床透明度和可信度。尽管模型在测试集中表现出色,但存在一定过拟合风险,且为单中心研究,样本量有限。总体而言,Delta超声放射组学具备早期识别耐药患者、指导个体化治疗和优化手术策略的潜力,为乳腺癌NAC疗效的精准评估与分层管理提供了有力工具。
06
讨论
局限性:①单中心小样本:研究为单中心回顾性,样本量有限,可能存在选择偏倚,泛化能力受限。②手动分割依赖经验:ROI由人工勾画,虽由高年资医生操作,仍存在主观变异性。③潜在过拟合风险:测试集AUC略高于训练集,提示模型在小样本高维特征下可能过拟合。
未来展望:①多中心外部验证:需联合多中心、大样本队列验证模型鲁棒性与临床泛化能力。②自动化分割技术:探索深度学习自动勾画ROI,提升精度与可重复性,减少人工误差。③整合多模态数据:结合临床病理变量(如分子分型)构建联合模型,优化预测效能。
参考文献:Wang M, Huang Z, Tian H, Mo S, Wu H, Xu J, Dong F. Longitudinal Ultrasound Delta Radiomics for Early Stratified Prediction of Tumor Response to Neoadjuvant Chemotherapy in Breast Cancer. Acad Radiol. 2025 Dec;32(12):7119-7133. doi: 10.1016/j.acra.2025.09.011.

AtomGit 是由开放原子开源基金会联合 CSDN 等生态伙伴共同推出的新一代开源与人工智能协作平台。平台坚持“开放、中立、公益”的理念,把代码托管、模型共享、数据集托管、智能体开发体验和算力服务整合在一起,为开发者提供从开发、训练到部署的一站式体验。
更多推荐
 已为社区贡献75条内容
已为社区贡献75条内容






所有评论(0)