原代人肝细胞长期培养模型评估丨全人源肝细胞三培养体系(TCS)在CYP450酶诱导研究中的应用解析
摘要
在药物研发阶段,细胞色素P450(CYP450)酶诱导研究是体外药物代谢与药物相互作用(DDI)评估的重要组成部分。传统原代人肝细胞(PHH)虽广泛应用于CYP诱导评价,但在长期培养稳定性、部分CYP亚型表达维持等方面仍存在局限。本文围绕一种全人源肝细胞三培养体系(TCS, Tri-Culture System),系统介绍其在主要CYP酶诱导研究中的应用表现,包括基础表达水平、原型诱导剂刺激后的诱导能力以及EC₅₀与Emax分析结果。研究结果表明,TCS在维持肝细胞长期功能及CYP诱导能力方面表现稳定,尤其在CYP2C酶诱导研究中具有一定应用潜力,可为药物研发中的体外诱导模型选择提供参考。
关键词
全人源肝细胞;三培养体系;TCS;原代人肝细胞;PHH;CYP450;CYP酶诱导;CYP2C酶诱导检测;肝细胞诱导评估模型;药物代谢研究
一、引言
在药物研发阶段,新型化合物对主要细胞色素P450(CYP)酶的体外诱导潜能评估是关键环节,传统方法多采用三明治培养的原代人肝细胞(PHH)。尽管PHH结合监管指南往往能较合理地预测临床诱导风险,但对于新一代的肝细胞模型在CYP诱导评估中的表现,目前仍缺乏充分认知。
本研究评估了一种新型的全人源肝细胞三培养系统(TCS),用于检测主要CYP和核受体的基础表达水平,以及在原型诱导剂处理后CYP的诱导水平。这些结果将为TCS在体外诱导研究中的进一步应用提供基础数据支持,并为探索TCS能否克服PHH存在的相关挑战(如CYP2C酶诱导评估难题)提供重要参考。
二、材料与方法
1、4周培养期内基因基础表达水平的评估
- 将原代人肝细胞(PHH)和饲养细胞接种到24孔胶原包被板上,构建三培养体系(TCS);
- 在4周培养期内的特定时间点,向孔中加入Trizol试剂裂解细胞;
- 采用氯仿萃取法分离RNA,使用SuperScript IV VILO试剂盒合成cDNA;
- 使用QuantStudio7实时荧光定量PCR系统上的TaqMan芯片检测法评估基因表达。与第1天的表达量相比,使用ΔΔCt法计算倍数变化。
2、评估CYP表达对原型诱导剂的反应
-
将原代人肝细胞(PHH)和饲养细胞接种到96孔胶原包被板上,构建三培养体系(TCS);
-
培养至第10天,向孔中加入含不同浓度原型诱导剂(含0.1%二甲基亚砜)的培养基(表1);
-
细胞暴露于诱导剂48小时,前24小时后更换新鲜培养基和诱导剂;
-
48小时后,移除培养基,使用mRNA Catcher PLUS纯化试剂盒收集各孔中的RNA;
-
采用Super Script IV VILO试剂盒合成cDNA,通过QuantStudio7实时荧光定量PCR系统结合TaqMan探针检测法评估基因表达水平,采用ΔΔCt法计算相对于溶媒对照组的倍数变化;
-
使用GraphPad Prism软件,通过S型曲线拟合数据来确定Emax和EC₅₀值。
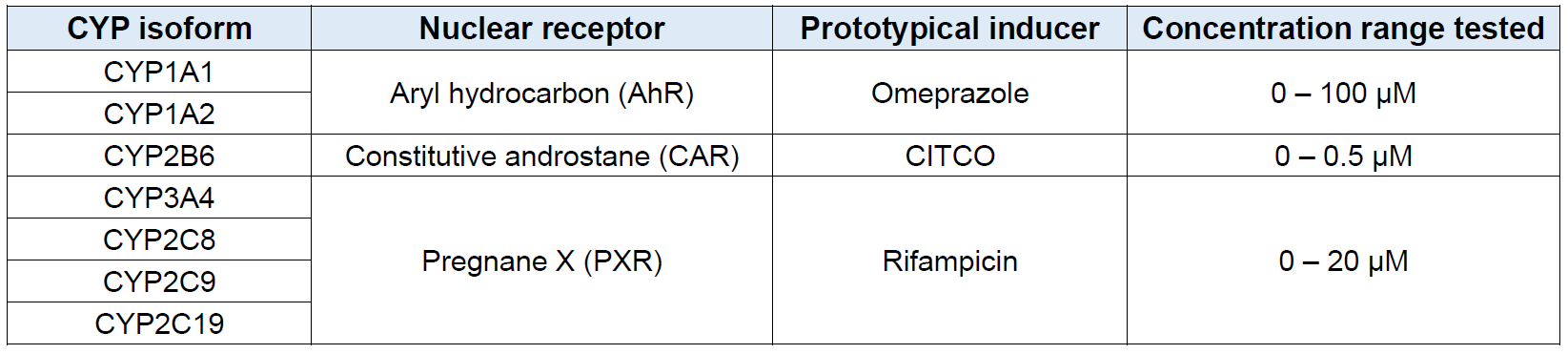
表1. 针对阳性诱导剂处理后诱导潜能评估的CYP酶列表
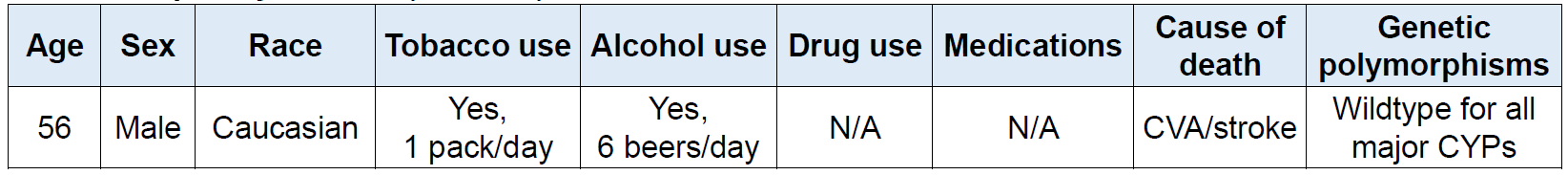
表2. 肝细胞供体(1921756)信息
三、结果
1、三培养体系(TCS)研究中内参基因的筛选
结果显示,各内参基因的Ct值存在差异(图1)。其中GAPDH在培养期间的Ct值具有良好的一致性,因此被选为理想的内参基因。
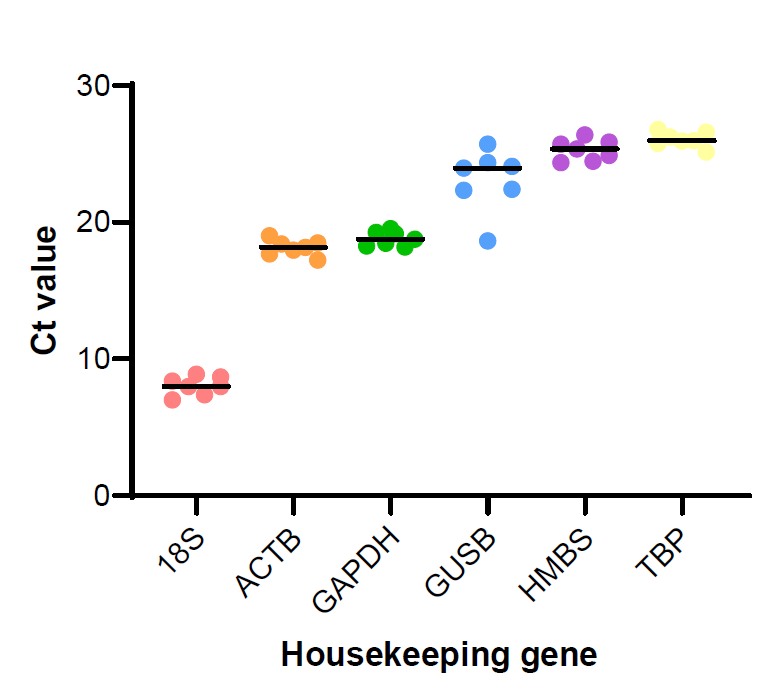
图1. 4周培养期内各内参基因表达水平的评估。每个圆点代表第1、4、7、12、17、23或30天的基因表达水平。
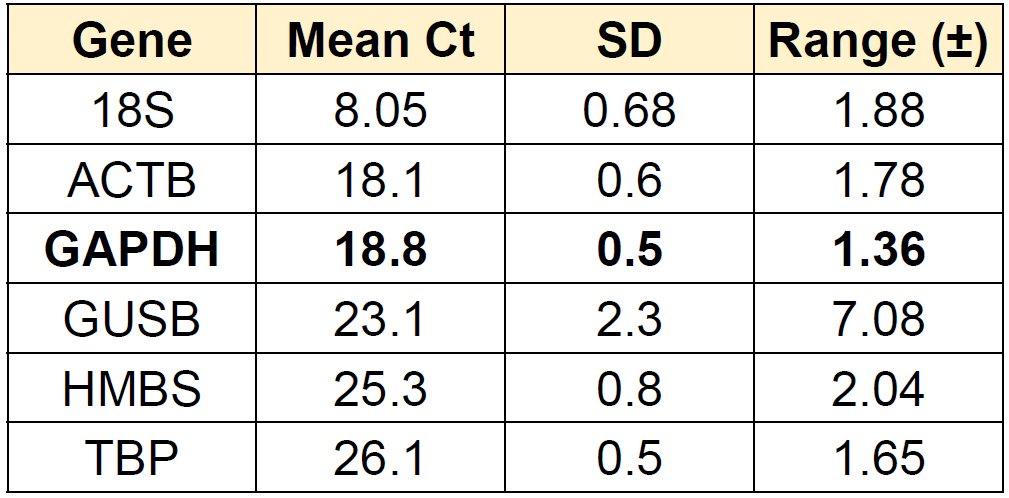
表3. 各内参基因的Ct值统计数据
2、4周培养期内TCS中CYP酶和核受体的基础表达水平
如图2所示,在TCS建立后的4-12天内,除CYP1A1和CYP2E1外,其余CYP酶和核受体的表达水平均明显升高。大多数受测基因的表达水平在培养第7-12天达到峰值,因此后续的诱导研究选择在培养第10天启动。
这一结果说明,TCS体系能够在较长培养周期内维持较稳定的肝细胞功能状态,并支持关键代谢酶与核受体的持续表达。
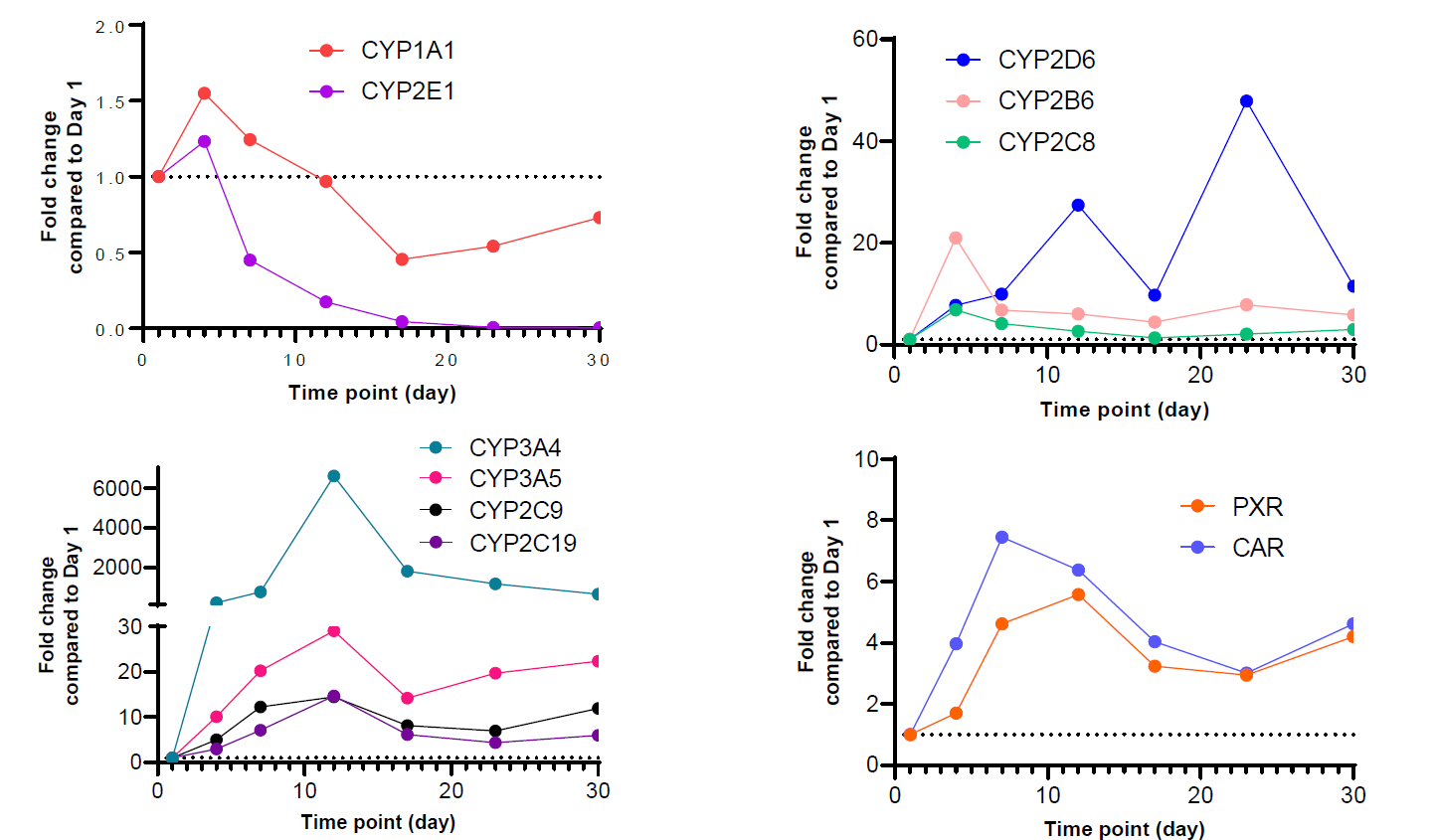
图2. 在基础培养条件下,于4周培养期内的不同时间点检测TCS中各CYP酶和核受体的基因表达水平。
3、原型诱导剂暴露48小时后主要CYP酶的诱导潜能
经不同浓度原型诱导剂处理48小时后,TCS中所有主要CYP酶均表现出明显的诱导潜能,包括CYP2C家族各亚型(图3)。
各酶的最大诱导倍数(Eₘₐₓ)和半数效应浓度(EC₅₀)数据见表4。此外,在所有主要CYP酶的测试中,当诱导剂浓度达到最高值时,诱导潜能均呈现下降趋势。
研究结果表明:
- TCS体系能够较好维持主要CYP酶的诱导响应能力;
- CYP2C相关诱导研究表现较好;
- TCS在长期培养模型中仍能维持较高代谢功能;
- 对于药物代谢与DDI研究具有一定参考意义。
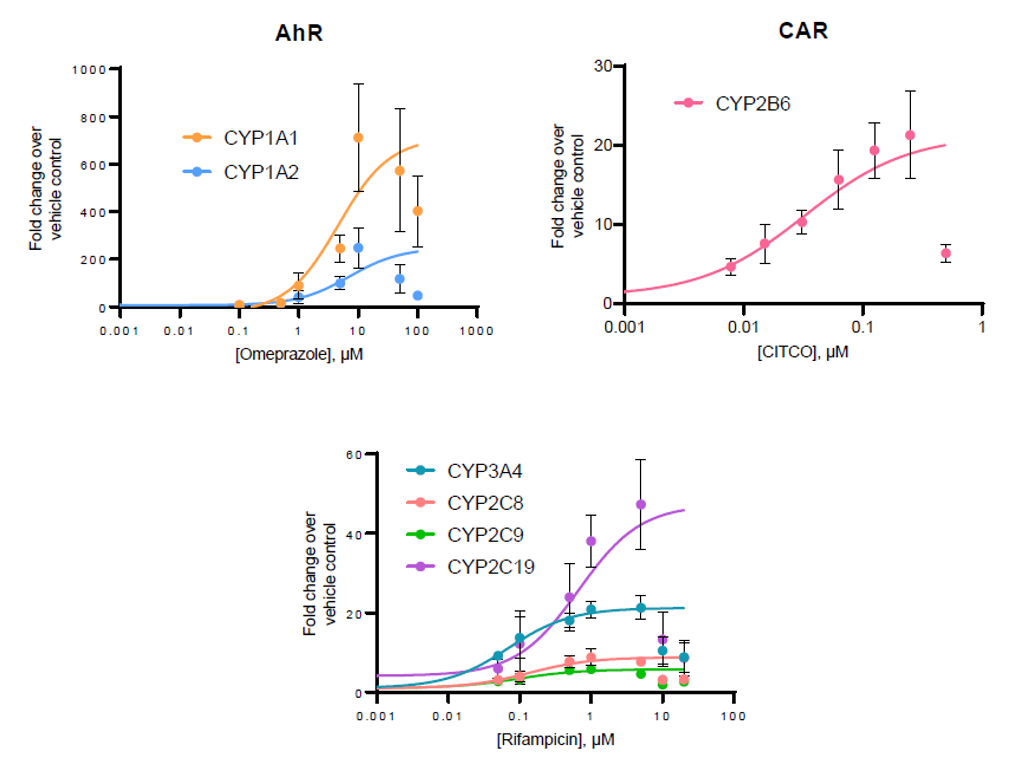
图3. 三培养体系(TCS)经不同浓度的多种原型诱导剂处理48小时后,检测各CYP酶的基因表达水平。表达水平以相对于溶媒对照组的倍数变化表示(n=4),通过将曲线限定在观察到的最高倍数变化值,确定各酶的最大诱导倍数(Eₘₐₓ)和半数效应浓度(EC₅₀)。
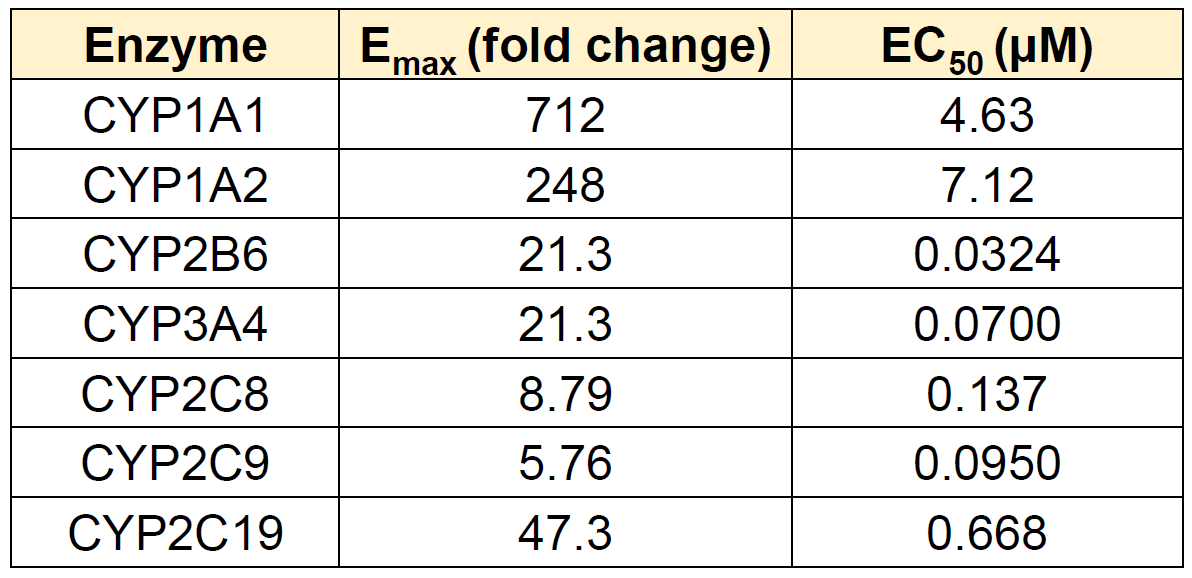
表4. 各CYP酶的最大诱导倍数(Eₘₐₓ)和半数效应浓度(EC₅₀)
四、研究讨论
传统PHH模型虽然被广泛用于CYP诱导研究,但在长期培养过程中,常会出现:
- 肝细胞功能下降;
- CYP表达水平降低;
- 细胞状态不稳定;
- 供体差异较大等问题。
而全人源TCS体系通过引入辅助饲养细胞与长期培养策略,在一定程度上改善了传统模型存在的问题。
从本研究结果来看:
- 大多数CYP酶表达可维持至培养后期;
- 核受体表达稳定;
- 对原型诱导剂具有明显响应;
- CYP2C家族诱导表现较好。
因此,该体系在:
- 药物代谢研究;
- CYP诱导评价;
- DDI风险预测;
- 长期肝毒性研究;
- 肝脏体外模型研究;
等方向具有一定应用潜力。
五、结论
-
TCS建立后的4-12天内,除CYP1A1和CYP2E1外,CYP酶和核受体的表达水平明显升高;
-
大多数受测基因在TCS中的表达水平于第7-12天达到峰值;
-
主要CYP酶在TCS中均对原型诱导剂具有高度诱导性,包括CYP2C酶;
-
在主要CYP酶的测试中,当诱导剂浓度达到最高值时,诱导潜能均有所下降。
总体来看,全人源肝细胞三培养体系(TCS)在长期培养稳定性与CYP450酶诱导研究中表现出良好应用潜力,可作为体外药物代谢与诱导评价的重要研究模型之一。
参考说明
本文基于原代人肝细胞、CYP450酶等公开研究资料、文献、应用文章整理,仅用于科研技术交流与行业信息分享。

AtomGit 是由开放原子开源基金会联合 CSDN 等生态伙伴共同推出的新一代开源与人工智能协作平台。平台坚持“开放、中立、公益”的理念,把代码托管、模型共享、数据集托管、智能体开发体验和算力服务整合在一起,为开发者提供从开发、训练到部署的一站式体验。
更多推荐
 已为社区贡献30条内容
已为社区贡献30条内容







所有评论(0)