原代人肝细胞长期培养模型研究:全人源三培养体系(TCS)对PHHs功能维持的影响
摘要:
原代人肝细胞(Primary Human Hepatocytes,PHHs)是药物代谢、药理学及毒理学研究中的核心模型,但传统培养体系难以长期维持其形态与代谢功能。本文基于全人源三培养体系(TCS)的公开研究资料,系统介绍原代人肝细胞长期培养方法、胆小管网络形成、白蛋白与尿素分泌、细胞色素P450(CYP)活性维持以及Ⅰ相与Ⅱ相代谢功能等关键结果,为药物研发、DILI研究及体外肝模型构建提供参考。
关键词:
原代人肝细胞;PHHs;三培养体系;TCS;肝细胞长期培养;肝细胞培养体系;细胞色素P450;CYP3A4;药物代谢;毒理学研究;肝脏模型;胆小管网络;药物筛选;DILI;体外肝模型
一、引言
原代人肝细胞(PHHs)在临床前药理学和毒理学研究中的应用受到一定限制,部分原因是缺乏便捷的合适培养体系。
理想的肝细胞培养体系通常需要满足以下条件:
- 操作简便
- 能支持不同供体来源细胞
- 可长期维持肝细胞结构与功能
- 适用于药物代谢与毒理学研究
- 维持细胞极性与CYP活性
传统三明治培养(Sandwich Culture,SC)体系与共培养体系虽然能够部分改善肝细胞状态,但依然存在一定局限性,例如:
- 肝细胞功能随时间下降
- CYP酶活性衰减
- 细胞极性难以长期维持
- 供体差异较明显
因此,研究人员开发了:
全人源三培养体系(Tri-Culture System,TCS)
用于长期维持原代人肝细胞的形态与代谢功能。
二、什么是全人源三培养体系(TCS)
TCS体系采用:
- 原代人肝细胞(PHHs)
- 两种原代人源饲养细胞(FCs)
共同构建培养环境。
与传统使用小鼠或大鼠来源饲养细胞的体系相比:
TCS具有:
- 全人源体系
- 更接近人体微环境
- 更适合药物代谢研究
- 更适合长期培养
等特点。
研究中:
将两种基质饲养细胞按照1:1比例混合后:
- 接种于24孔胶原包被板
- 再加入冻存原代人肝细胞
从而构建完整三培养体系。
三、TCS体系研究中的主要结果
在为期3周至6周的培养过程中:
研究人员重点评估了:
- 肝细胞形态
- 白蛋白分泌
- 尿素分泌
- 胆小管形成
- CYP酶活性
- 药物代谢能力
等指标。
结果显示:
1、PHHs在TCS中可长期维持稳定形态
来自多个成人供体的原代人肝细胞:
在TCS中能够:
- 长期保持健康形态
- 形成多细胞簇
- 稳定培养长达42天
相比传统SC体系:
TCS中肝细胞状态更加稳定。
2、胆小管网络形成稳定
培养初始5天内:
PHHs逐渐形成:
交织胆小管网络
并形成:
- 紧密连接
- 缝隙连接
这些结构对于:
- 肝细胞极性
- 药物转运
- 胆汁分泌
具有重要意义。
3、白蛋白与尿素分泌明显提高
研究显示:
与SC体系相比:
TCS中的PHHs:
白蛋白生成水平:
达到:
- 30–40 μg/天/10⁶细胞
尿素生成水平:
达到:
- 55–70 μg/天/10⁶细胞
说明:
TCS更有利于维持肝细胞功能。
4、CYP基因表达明显增强
培养第4天:
TCS中的:
- CYP1A2
- CYP2B6
- CYP3A4
- Alb
等基因表达:
平均高于SC体系约2倍。
说明:
TCS对于:
- 药物代谢功能
- 解毒功能
- CYP酶活性维持
具有明显优势。
5、Ⅰ相与Ⅱ相代谢长期稳定
第5天后:
TCS中:
- 咪达唑仑1-羟化
- 葡萄糖醛酸化
- 硫酸化
等功能:
可稳定维持至少2周。
说明:
TCS不仅维持肝细胞形态:
也能够长期维持:
代谢功能稳定性。
四、当前肝细胞培养体系面临的问题
目前:
肝细胞体外模型依然面临诸多挑战。
1、动物模型存在物种差异
动物模型虽然广泛应用于药理毒理研究:
但:
- CYP代谢差异
- 核受体差异
- 药物反应差异
会影响结果外推。
2、传统SC体系功能下降较快
传统单培养或三明治培养体系中:
PHHs通常会出现:
- 极性丢失
- CYP下降
- 代谢功能减弱
等问题。
3、非人源共培养体系局限明显
许多共培养体系:
使用:
- 小鼠细胞
- 大鼠细胞
作为饲养层。
这会带来:
- 物种干扰
- 信号差异
- 代谢偏差
等问题。
而TCS:
采用全人源体系:
因此更适合:
- 药物开发
- DILI研究
- 长期毒性研究
- ADME研究
等方向。
五、TCS体系搭建流程
实验流程

图1 三培养体系搭建步骤
具体步骤
1、培养基制备
包括:
- 过夜解冻
- 添加补充剂
- 37℃预热
整体耗时约30分钟。
2、饲养细胞接种
包括:
- 解冻
- 计数
- 接种FCs
耗时约60分钟。
3、原代人肝细胞接种
包括:
- 解冻PHHs
- 计数
- 接种
整体约需2–4小时。
4、培养基更换
每日更换培养基。
六、检测方法解析
研究中采用了多种检测方式:
用于评估:
- 肝细胞功能
- CYP活性
- 代谢稳定性
等指标。
七、蛋白表达检测
通过免疫细胞化学法:
检测:
- ZO-1
- Connexin-32
- CK18
- 白蛋白(Alb)
- CYP1A2
- Vimentin(VIM)
等蛋白表达。
同时:
使用CDFDA:
对胆小管进行染色。
胆小管与蛋白标志物表达

图3 三培养体系(TCS)中胆小管形成及蛋白标志物表达
结果显示:
- ZO-1阳性
- Connexin-32阳性
- CK18阳性
说明:
肝细胞维持了较好的:
- 极性
- 细胞连接
- 功能状态
八、白蛋白与尿素检测
通过:
- ELISA
- 比色法
分别测定:
- Alb
- 尿素
水平。
功能验证结果
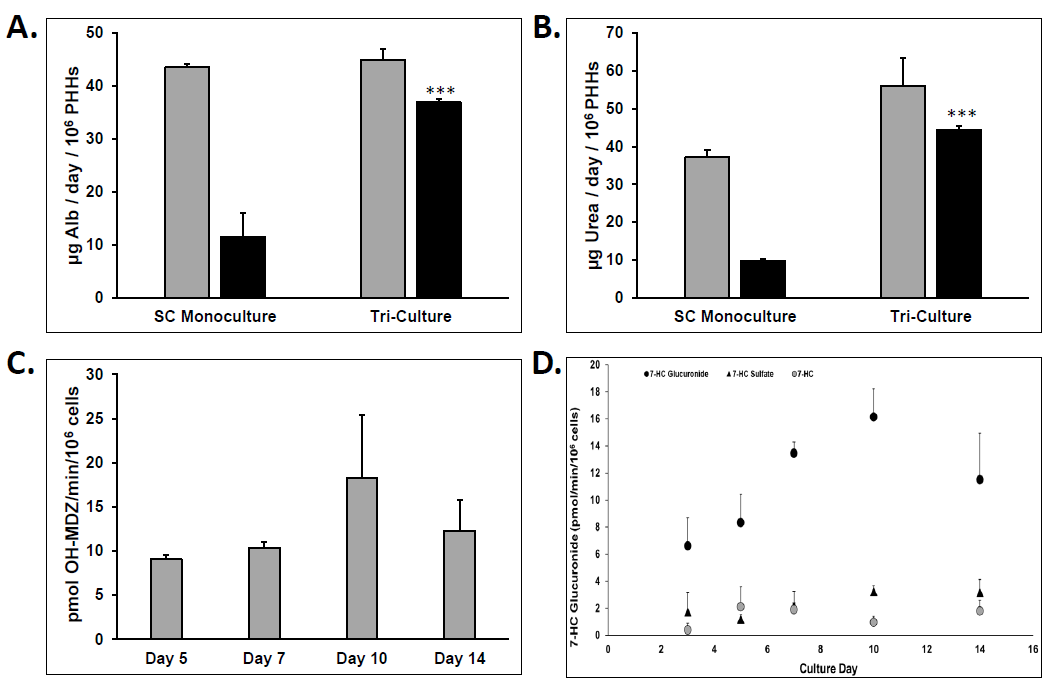
图5 三培养体系(TCS)中原代人肝细胞功能验证
结果显示:
相比SC体系:
TCS中:
- Alb生成更高
- 尿素水平更高
- 功能维持时间更长
九、CYP酶活性检测
研究采用:
- 奥美拉唑
- CITCO
- 利福平
等诱导剂:
检测:
- CYP1A2
- CYP2B6
- CYP3A4
活性。
CYP诱导结果
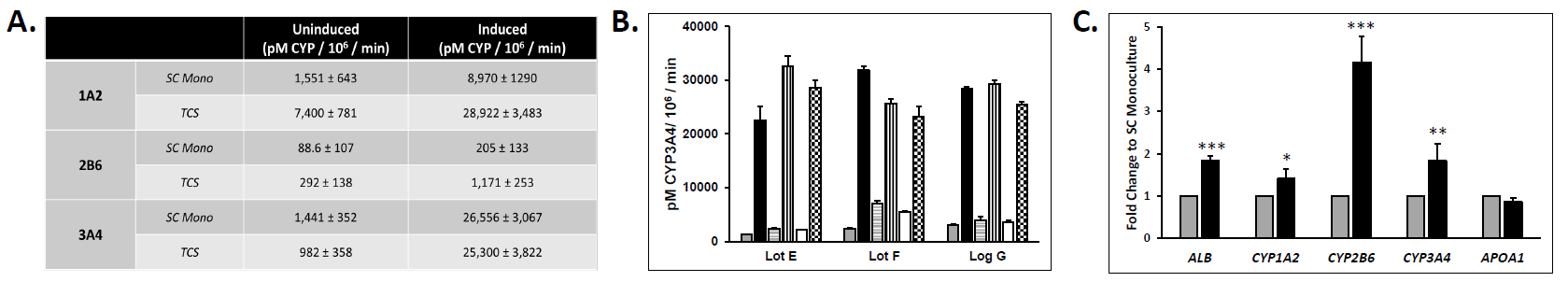
图6 三培养体系(TCS)中CYP1A2、CYP2B6及CYP3A4诱导情况
结果显示:
TCS中:
- CYP活性长期稳定
- 多供体间一致性较好
- 诱导能力明显优于SC体系
十、Ⅰ相与Ⅱ相代谢功能验证
Ⅰ相代谢
采用:
咪达唑仑(Midazolam)
作为探针。
检测:
- 1’-羟基咪达唑仑(OH-MDZ)
生成量。
Ⅱ相代谢
采用:
7-乙氧基香豆素(7-EC)
检测:
- 葡萄糖醛酸化
- 硫酸化
等功能。
结果显示:
TCS中:
Ⅰ相与Ⅱ相代谢功能:
可长期稳定维持。
十一、TCS长期稳定性分析
长期培养结果
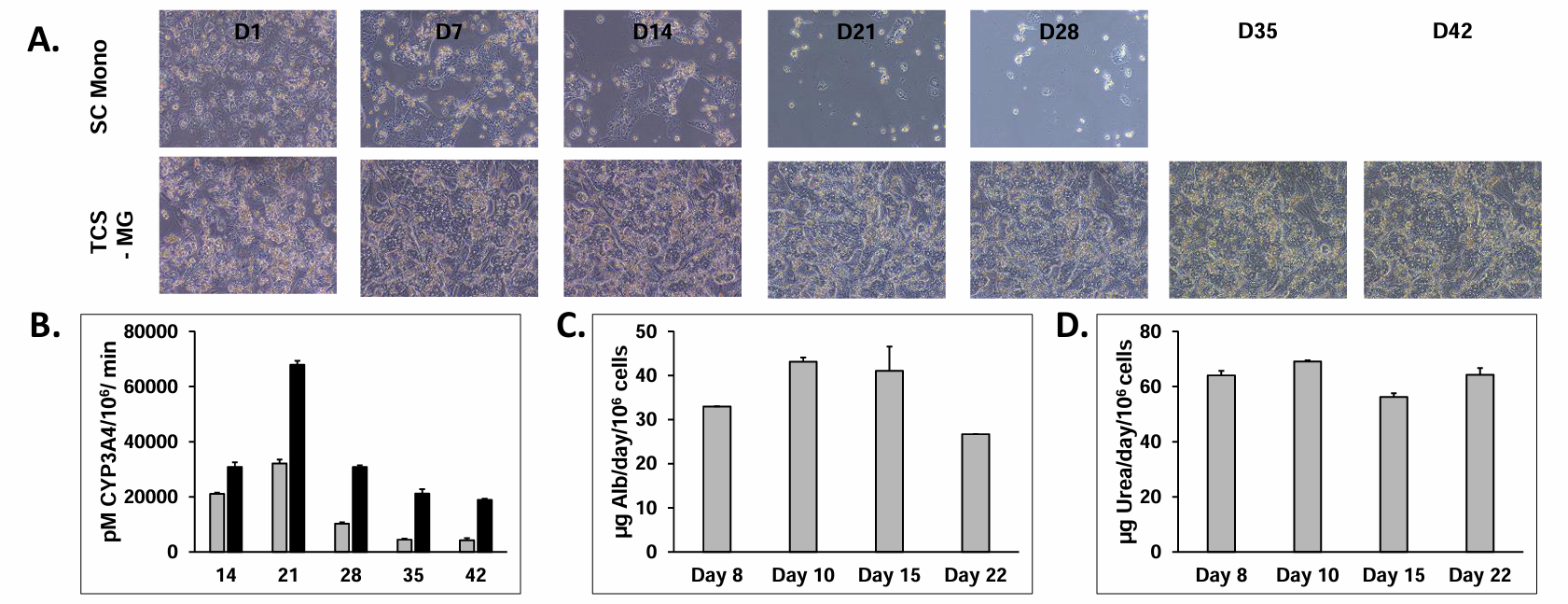
图4 三培养体系(TCS)的长期稳定性
研究中:
PHHs:
在无Matrigel条件下:
仍能够:
- 长期维持形态
- 长期维持CYP活性
- 长期维持Alb与尿素水平
时间可达42天。
十二、PHHs与FCs比例优化
研究还分析了:
PHHs与FCs不同接种比例。
最佳比例分析
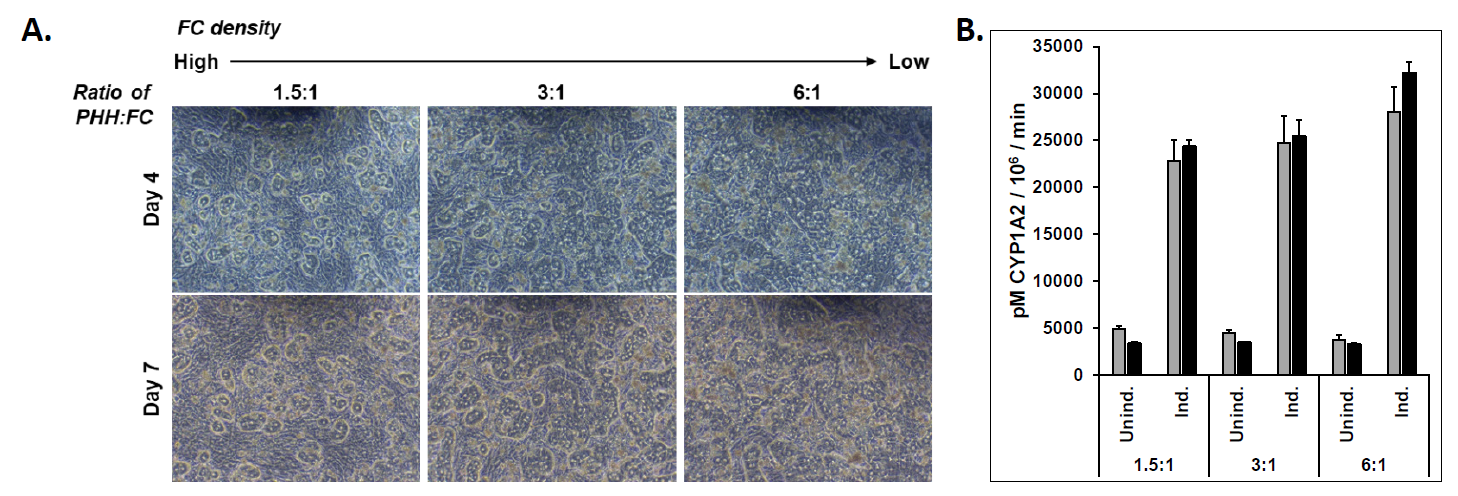
图2 三培养体系(TCS)中适宜PHHs与FCs比例
结果显示:
适宜比例有助于:
- 维持CYP活性
- 提高长期稳定性
- 提高功能维持能力
十三、供体适用性分析
研究中:
多个成人供体PHHs:
均能够在TCS中:
- 保持健康形态
- 保持代谢功能
- 长期维持CYP诱导能力
说明:
TCS具有:
较好的:
供体适用性与重复性。
十四、结论
综合研究结果:
全人源三培养体系(TCS)具有以下特点:
- 长期维持PHHs形态
- 长期维持Alb与尿素功能
- 稳定维持CYP活性
- 支持Ⅰ相与Ⅱ相代谢
- 维持胆小管网络结构
- 适用于多供体来源PHHs
因此:
TCS是一种:
便捷、稳定、可重复的原代人肝细胞长期培养体系
适用于:
- 药物研发
- DILI研究
- ADME研究
- 药物代谢
- 肝毒性评估
- 临床前毒理学
等方向。
参考文献
-
LeCluyse E.L., Witek R.P., Andersen M.E., Powers M.J., 2012. Organotypic liver culture models: Meeting current challenges in toxicity testing.
-
Olson H., Betton G., Robinson D., et al., 2000. Concordance of the toxicity of pharmaceuticals in humans and animals.
-
Khetani S.R., Bhatia S.N., 2008. Microscale culture of human liver cells for drug development.
-
Ware B.R., Durham M.J., Monckton C.P., Khetani S.R., 2017. A Cell Culture Platform to Maintain Long-Term Phenotype of Primary Human Hepatocytes and Endothelial Cells.
本文基于公开研究资料整理,仅用于科研信息分享。本文关于人肝细胞(PHHs)、肝细胞培养基、长期培养体系及相关药物代谢与毒理学研究解决方案,支持DILI研究、ADME研究及肝脏体外模型构建应用。

AtomGit 是由开放原子开源基金会联合 CSDN 等生态伙伴共同推出的新一代开源与人工智能协作平台。平台坚持“开放、中立、公益”的理念,把代码托管、模型共享、数据集托管、智能体开发体验和算力服务整合在一起,为开发者提供从开发、训练到部署的一站式体验。
更多推荐
 已为社区贡献30条内容
已为社区贡献30条内容







所有评论(0)