如何将影像组学特征与骨肉瘤免疫微环境中的关键生物学指标建立关联,并进一步解释其与无病生存期预后及免疫治疗响应的机制联系
01
导语
各位同学,大家好。现在做影像组学,如果还只停留在“提取特征—建个模型—算个AUC”,那就有点像算命算得挺准,但为啥准,自己也说不明白。别人一问:你这特征到底代表啥?背后有啥道理?瞬间就成了黑箱本箱。而真正能打高分、站得住脚的研究,都在干一件事——给影像组学找“生物学娘家”,让宏观图像和微观病理、细胞、基因、通路对上话。今天咱们就通过一篇骨肉瘤预后预测的最新文献,看看作者如何优雅、合理、不硬凑地将MRI影像特征与肿瘤免疫微环境中的CD3⁺ T细胞、CD8⁺ T细胞及CD8/FOXP3比值挂上钩,并进一步解释其与无病生存期、免疫治疗响应的机制联系。从“只会算分的工具人”,升级成能讲清疾病故事的研究者。

★题目:Pathology-interpretable radiomic model for predicting clinical outcome in patients with osteosarcoma: a retrospective, multicenter study
(基于病理可解释的影像组学模型预测骨肉瘤患者临床预后)
★期刊:《BMC Medicine》(中科院1区,IF=8.3)
★研究疾病:骨肉瘤
★生物学机制:肿瘤微环境中的免疫状态
★发表时间:2025年10月
02
研究背景-从 “临床问题” 落到 “生物学问题”
骨肉瘤是儿童和青少年中最常见的原发性恶性骨肿瘤,其高度侵袭性和早期转移倾向导致患者预后不佳,即使接受规范化新辅助化疗和手术,仍有相当比例的患者出现复发,5年生存率仅为23%–29%。因此,早期识别高复发风险患者、实现个体化治疗成为临床迫切需求。磁共振成像(MRI)是骨肉瘤诊疗中不可或缺的工具,但传统影像评估主要依赖放射科医生的主观经验,难以全面捕捉肿瘤内部的异质性。近年来,影像组学通过高通量提取定量影像特征,在预测骨肉瘤化疗反应和预后方面展现出潜力。然而,现有影像组学模型普遍存在一个核心瓶颈:缺乏生物学可解释性。模型依赖于大量计算特征,但这些特征与肿瘤的潜在病理生物学过程之间缺乏明确联系,导致临床医生难以理解和信任其预测结果。为解决这一问题,研究者开始尝试将影像组学特征与基因组学、蛋白质组学或病理图像进行关联。其中,病理图像(H&E和IHC)在临床中易于获取,能够提供关于细胞核形态、免疫微环境和缺氧状态等丰富信息,且与影像数据在生物学上更为接近。因此,建立影像组学特征与病理微环境特征之间的跨尺度关联,不仅能够赋予影像组学模型以生物学意义,还能为骨肉瘤的预后评估提供更透明、更可靠的决策支持。
03
研究目的(明确写出“三层目的”)
本研究旨在开发并验证一个基于MRI的影像组学模型,用于预测骨肉瘤患者的无病生存期(DFS),并系统性地揭示该模型背后的病理生物学机制。具体而言,研究目的分为三个层次:第一层,构建一个高性能的影像组学预测模型,采用多中心数据训练,并在两个独立的外部测试集中验证其泛化能力,同时与传统的临床预后指标(如T分期、肿瘤体积)进行比较;第二层,通过H&E染色全切片图像提取肿瘤细胞核的形态特征(包括核面积、轴长比、与邻核的距离等),并通过免疫组织化学(IHC)量化肿瘤微环境中的关键生物标志物,包括CD3、CD8、CD68、FOXP3(免疫相关)和CAIX(缺氧相关),从而建立从宏观影像到微观病理的多维度数据体系;第三层,采用相关性分析(Spearman和Pearson)探索影像组学特征与细胞核形态特征、免疫/缺氧标志物之间的关联,明确哪些影像特征能够反映肿瘤的核异质性或免疫浸润状态,最终实现从“黑箱预测”到“机制可解释”的跨越,为影像组学模型的临床转化奠定生物学基础。
04
研究思路(最核心:怎么挂靠机制)
本研究的核心思路是以病理图像为桥梁,将宏观影像组学特征与微观肿瘤生物学机制进行跨尺度关联。首先,从14个中心的骨肉瘤患者中收集治疗前的增强MRI(CE-FS-T1WI),手动分割肿瘤区域并提取1130个影像组学特征(包括形状、一阶统计量、纹理和小波特征)。经过降维和机器学习算法(AdaBoost)筛选,构建由12个关键特征组成的预后模型,预测无病生存期。其次,为了回答“这些影像特征究竟反映了什么生物学本质”,研究者收集了外部测试集中患者的H&E和IHC病理切片。在H&E切片上,采用无监督分割算法识别每个细胞核,提取10种核形态特征(面积、主轴/次轴长度、RGB均值、与邻核的Delaunay距离等),并通过直方图和统计量聚合为150个患者级特征。在IHC切片上,定量评估五种免疫/缺氧标志物(CD3、CD8、CD68、FOXP3、CAIX)的密度。最后,将12个影像组学特征分别与150个核形态特征和5个IHC标志物进行相关性分析(Spearman或Pearson,FDR校正),筛选出|r|>0.3的显著关联对,并区分弱、中、强相关。通过这一思路,研究不仅验证了模型的预测性能,更明确了哪些影像特征与核异质性相关、哪些与免疫激活(如CD8/FOXP3比值)高度相关,从而为影像组学提供了具体的病理学解释。
05
数据和方法(机制部分怎么设计)
数据:本研究共纳入270例经手术和病理确诊的骨肉瘤患者,来自14个中心。其中训练集166例(中心1-3,用于模型开发),外部测试集1共56例(中心4,用于独立验证),外部测试集2共48例(中心5-14,用于再次验证)。此外,机制分析中分别使用了41例患者的H&E切片(提取核形态特征)和40例患者的IHC切片(检测CD3、CD8、CD68、FOXP3、CAIX)。
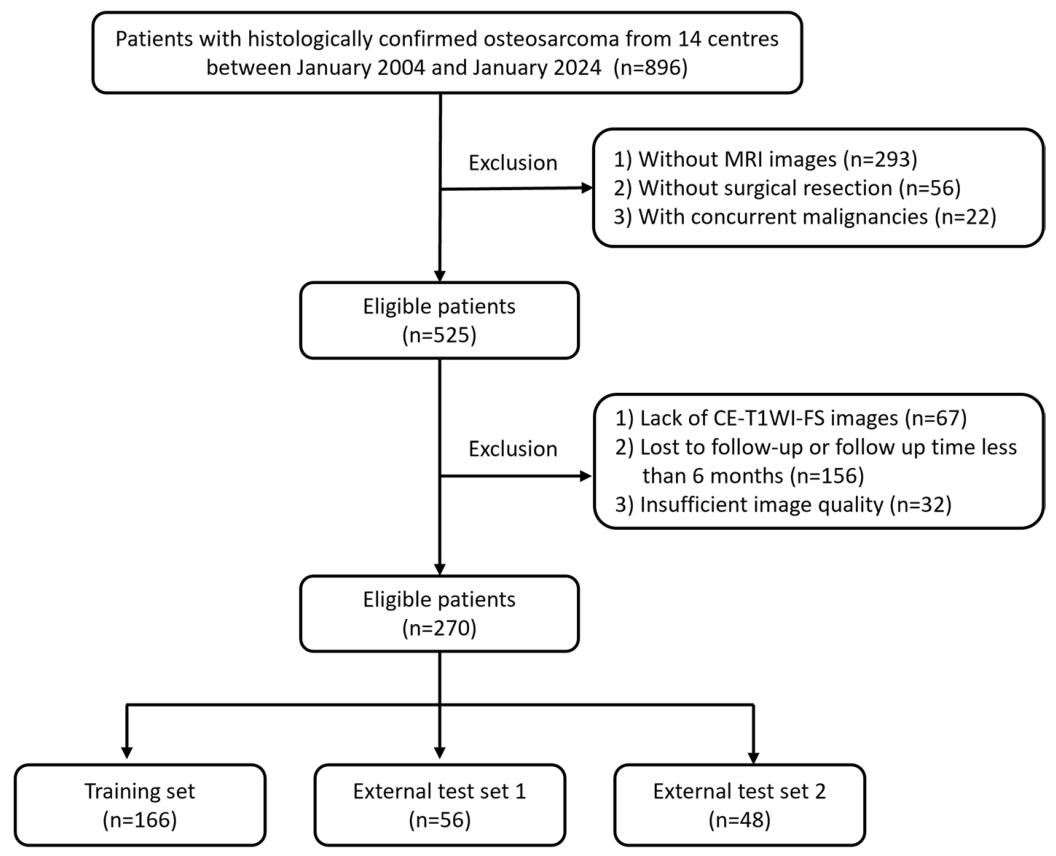
图 2:患者筛选流程图
方法:MRI预处理(N4偏置校正、灰度归一化、重采样至1×1×1 mm³)→肿瘤分割(手动逐层勾画ROI)→提取1130个影像组学特征(形状、一阶、纹理、小波)→特征降维(Pearson相关+Relief算法)→模型构建(六种分类器比较,选定AdaBoost,五折交叉验证)→性能评估(时间依赖AUC、校准曲线、决策曲线、SHAP值)→病理机制挂靠:从H&E切片中分割细胞核并提取10种形态特征(聚合为150个患者级特征),从IHC切片中定量免疫/缺氧标志物密度,最后用Spearman/Pearson相关分析评估影像特征与病理特征的关联(FDR校正)。
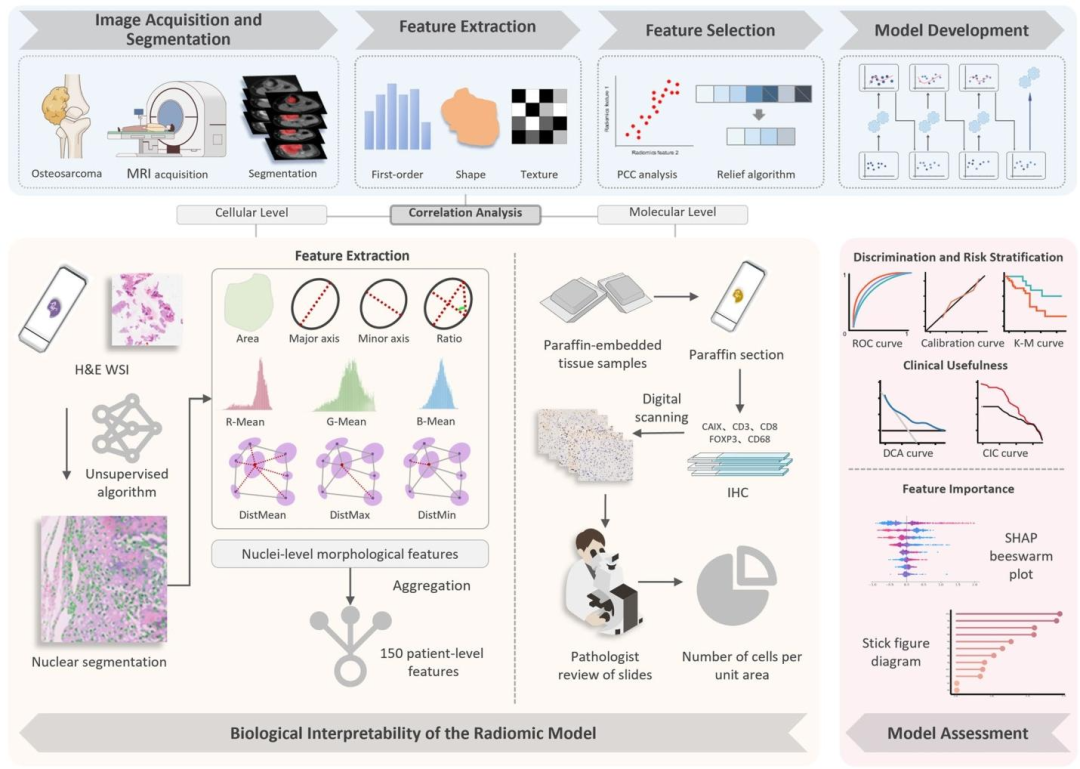
图 1:研究整体工作流程图
06
研究结果(“从表型到机制”)
1、表型层面(预测性能)
基于12个影像组学特征的AdaBoost模型在训练集中AUC为0.916,在两个外部测试集中分别为0.802和0.895,显著优于T分期和肿瘤体积(Delong检验,P<0.05)。校准曲线和决策曲线证实模型预测可靠、净获益高,可将患者准确划分为高、低风险组。
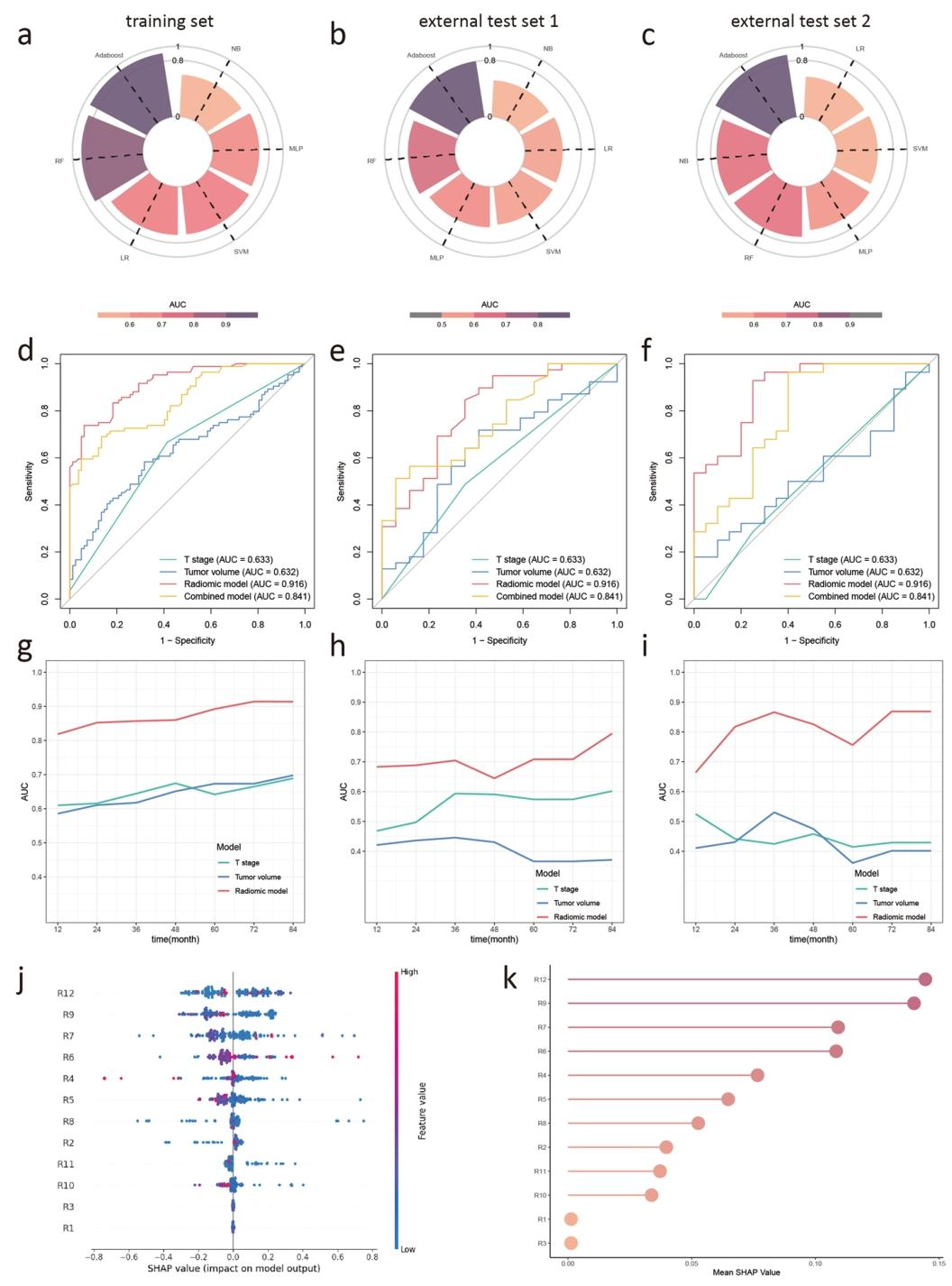
图 3(模型性能与SHAP特征重要性):该图分三部分:a-c比较六种机器学习算法的AUC,确认AdaBoost最优;d-f展示影像组学模型、T分期、肿瘤体积的ROC曲线,影像组学模型AUC显著更高;g-i显示时间依赖性AUC,影像组学模型长期保持优势;j-k为SHAP值条形图和蜂群图,其中wavelet_LLL_glszm_LargeAreaHighGrayLevelEmphasis等特征贡献最大,这些特征反映坏死/致密区或异质性,将影像特征与肿瘤生物学行为(侵袭性、坏死)直接挂钩。
2、机制层面(关联分析)
①与H&E核形态的关联
9个影像特征与17种核形态特征显著相关,共32对。68.8%为中等相关(|r|=0.4–0.5),18.8%为强相关(|r|>0.5),提示影像特征部分反映细胞核异质性。
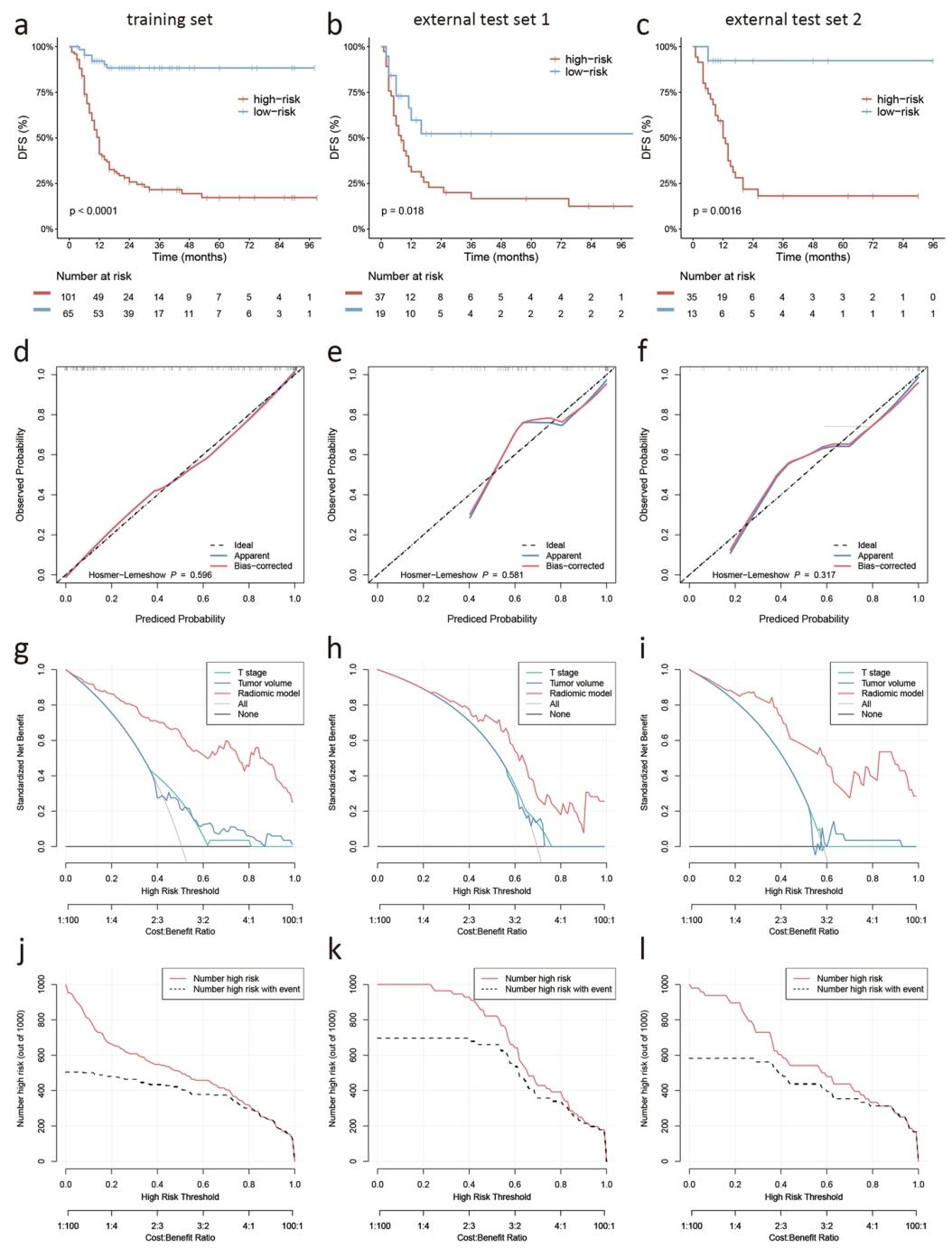
图 4(生存分层与临床决策曲线):该图包含三组:a-c Kaplan‑Meier曲线显示基于Radscore(阈值0.49)可将患者显著分为高、低风险组,验证模型预后分层能力;d-f校准曲线显示预测概率与实际生存一致;g-i决策曲线证明影像组学模型在较宽阈值范围内净获益最高;j-l临床影响曲线表明模型识别高风险患者的效率优越。这些分析从临床效用角度证实影像组学模型可指导个体化治疗,而分层能力的生物学基础正是图5揭示的免疫微环境差异。
②与IHC免疫标志物的关联
影像特征与CD3(r=0.50–0.76)、CD8(r=0.46–0.60)及CD8/FOXP3比值(r=0.69–0.81)显著相关,3对为强相关(r>0.7),表明影像组学可反映肿瘤免疫微环境状态。
③与缺氧标志物CAIX的关联
未发现显著相关性。原因可能包括骨肉瘤血供丰富、CAIX表达局灶且病理取样易避开坏死区,而影像覆盖全肿瘤,存在尺度与取样偏差。
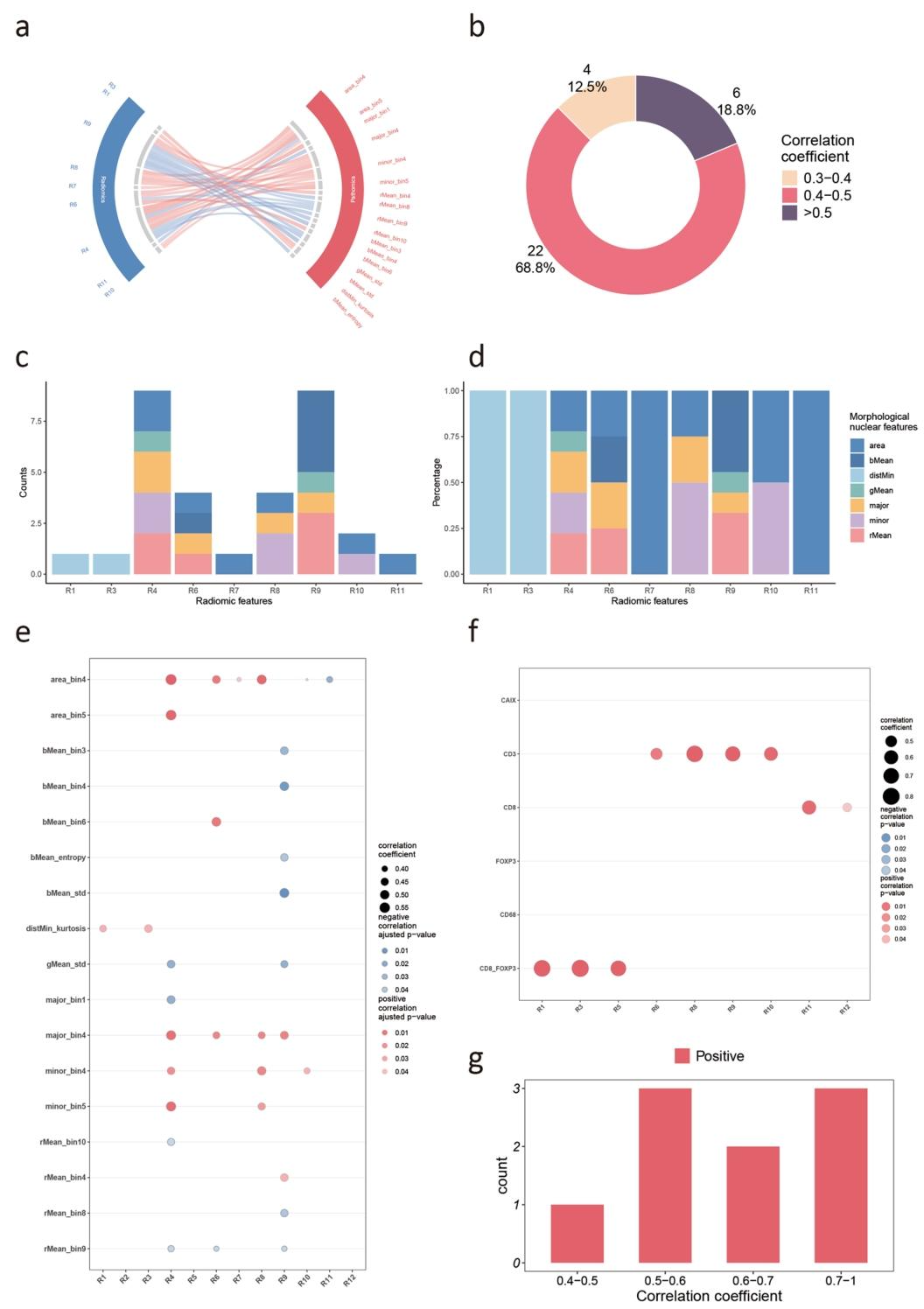
图 5(影像-病理关联分析):该图是机制挂靠的核心。a弦图显示9个影像特征与17种核形态特征存在32对显著相关(|r|>0.3);b显示68.8%为中等相关(|r|=0.4–0.5),18.8%为强相关(|r|>0.5);c-d堆叠条形图展示核形态特征在各影像特征中的分布;e气泡图展示影像-核形态相关强度;f气泡图展示影像特征与IHC标志物的关联,其中CD3、CD8、CD8/FOXP3比值呈中到强正相关(r最高0.81);g双向条形图总结相关系数分布。该图直观证明:影像组学特征主要反映肿瘤免疫微环境状态,而非单纯的核异质性。
07
讨论(把机制故事讲圆)
本研究的核心发现是:基于MRI的影像组学模型能够高精度预测骨肉瘤患者的无病生存期,且其预测性能显著优于传统的T分期和肿瘤体积。更重要的是,通过将影像特征与H&E衍生的细胞核形态特征以及IHC检测的免疫微环境标志物进行关联分析,我们首次系统揭示了影像组学特征的潜在生物学基础。结果显示,影像组学特征与CD3、CD8及CD8/FOXP3比值之间存在中到强相关性(最高r=0.81),而与缺氧标志物CAIX无显著相关。这一差异可能源于:骨肉瘤血供相对丰富、CAIX表达呈局灶性且病理采样常避开坏死区,而影像分析覆盖全肿瘤,存在尺度与取样偏差。与既往仅关注预测性能的研究相比,我们的工作将“黑箱”模型向“病理可解释”模型推进了一大步,增强了临床医生对模型输出的信任。从临床意义看,该模型可识别高复发风险患者,指导个体化辅助治疗(如免疫治疗或减量化疗),并有望整合到现有分期系统中。尽管如此,本研究仍存在局限性:回顾性设计、不同中心MRI扫描协议的异质性、病理图像与影像图像缺乏精确的空间配准(未做严格的组织-影像“病理组学”配准),以及免疫标志物仅采用平均密度而未考虑空间分布。未来需开展前瞻性研究,并引入多模态配准技术和空间转录组,进一步验证模型的生物学可解释性。
08
这篇文献的可借鉴思路
本研究的最核心借鉴价值在于“以病理为桥梁,将宏观影像特征与微观生物学机制进行跨尺度关联”。具体可迁移的思路如下:第一,病理特征的工程化量化。作者没有简单使用病理医生的半定量评分,而是从H&E切片中自动分割每个细胞核,提取10种形态特征(面积、轴长比、与邻核的Delaunay距离等),再通过直方图和统计量聚合为150个患者级特征。这一策略将主观病理描述转化为可计算、可复现的特征向量,适用于任何实体瘤的影像-病理关联研究。第二,分层递进的机制验证。研究分别从核形态(细胞内在特征)和免疫/缺氧微环境(细胞外环境)两个维度进行关联分析,发现影像特征与免疫标志物的相关性更强。这种分层设计有助于精准定位影像特征到底反映哪一层生物学信息,避免笼统的“影像-生物学相关”结论。第三,阴性结果的有效解释。CAIX无显著相关并未被忽视,而是从肿瘤血供、CAIX表达局灶性、病理取样偏差等角度给出合理解释,这反而增强了研究结论的严谨性。第四,模型解释工具SHAP的运用。通过SHAP值识别出对预测贡献最大的影像特征(如wavelet_LLL_glszm_LargeAreaHighGrayLevelEmphasis),并尝试赋予其生物学意义(坏死/致密肿瘤区),为后续机制验证提供具体靶点。第五,多中心外部验证。模型在两个独立测试集中均表现稳健,说明关联模式具有跨人群普适性,增强了机制结论的可靠性。以上思路可被直接迁移至其他癌症(如肺癌、乳腺癌、胶质瘤)的影像组学机制研究中,也可用于影像-基因组学、影像-蛋白质组学的跨尺度分析设计。
09
结语
总而言之,做影像组学不只是拼AUC、堆模型,更要学会给特征找意义、给模型讲道理。这篇文献告诉我们:以病理为桥梁,从H&E核形态到IHC免疫标志物,分层递进地做相关性分析,即使相关性中等也能讲出生物学故事;即使CAIX阴性结果,也能从取样偏差、肿瘤血供角度合理解释。只有把宏观影像和微观机制真正打通,我们的研究才不是“玄学算命”,而是有根有据、有血有肉、能讲好疾病故事的真科研。希望大家以后都能少走弯路,轻松写出有机制、有深度、能发高分的好文章!
参考文献:Ren Q, Zhang X, Wu X, Zhao H, Zhang Y, Yao Y, Leng Y, Zhang X, Liu Y, Xiao J, Liu W, Xie X, Pei N, He R, Tang N, Wen G, Zhang X, Zhang S, Zhang B. Pathology-interpretable radiomic model for predicting clinical outcome in patients with osteosarcoma: a retrospective, multicenter study. BMC Med. 2025 Oct 29;23(1):594. doi: 10.1186/s12916-025-04424-0.

AtomGit 是由开放原子开源基金会联合 CSDN 等生态伙伴共同推出的新一代开源与人工智能协作平台。平台坚持“开放、中立、公益”的理念,把代码托管、模型共享、数据集托管、智能体开发体验和算力服务整合在一起,为开发者提供从开发、训练到部署的一站式体验。
更多推荐
 已为社区贡献76条内容
已为社区贡献76条内容







所有评论(0)