细胞“时钟”可逆转?人类离延缓衰老的临床试验仅一步之遥
细胞“时钟”可逆转?人类离延缓衰老的临床试验仅一步之遥
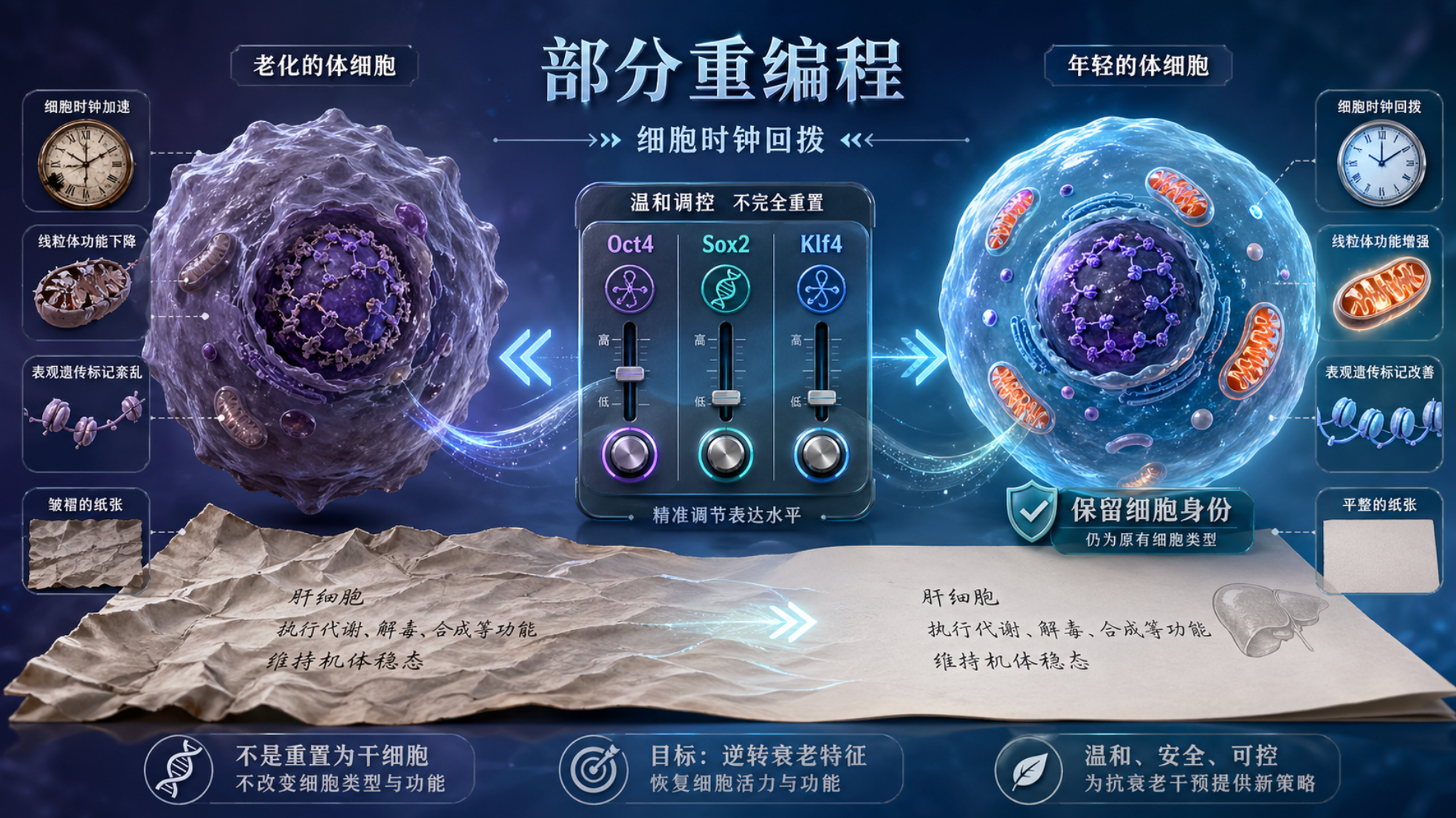
2006年,日本科学家山中伸弥找到了四个关键转录因子——Oct4、Sox2、Klf4和c-Myc,这四个“山中因子”组合在一起,能把一个成熟的体细胞硬生生拉回类似胚胎干细胞的初始状态。这相当于把一张写满人生经历的纸,重新变回一张白纸。
这项获得诺贝尔奖的突破,让再生医学沸腾了。但很快,所有人都意识到一个致命问题:一张白纸固然有无限可能,但它也可能变成任何东西——包括肿瘤。 当细胞被完全重置,它就失去了原有的身份和功能。你想让它修复视网膜,它可能长成一团混乱的组织。这就是再生医学的核心悖论:重置得越彻底,潜力越大,但失控的风险也越高。
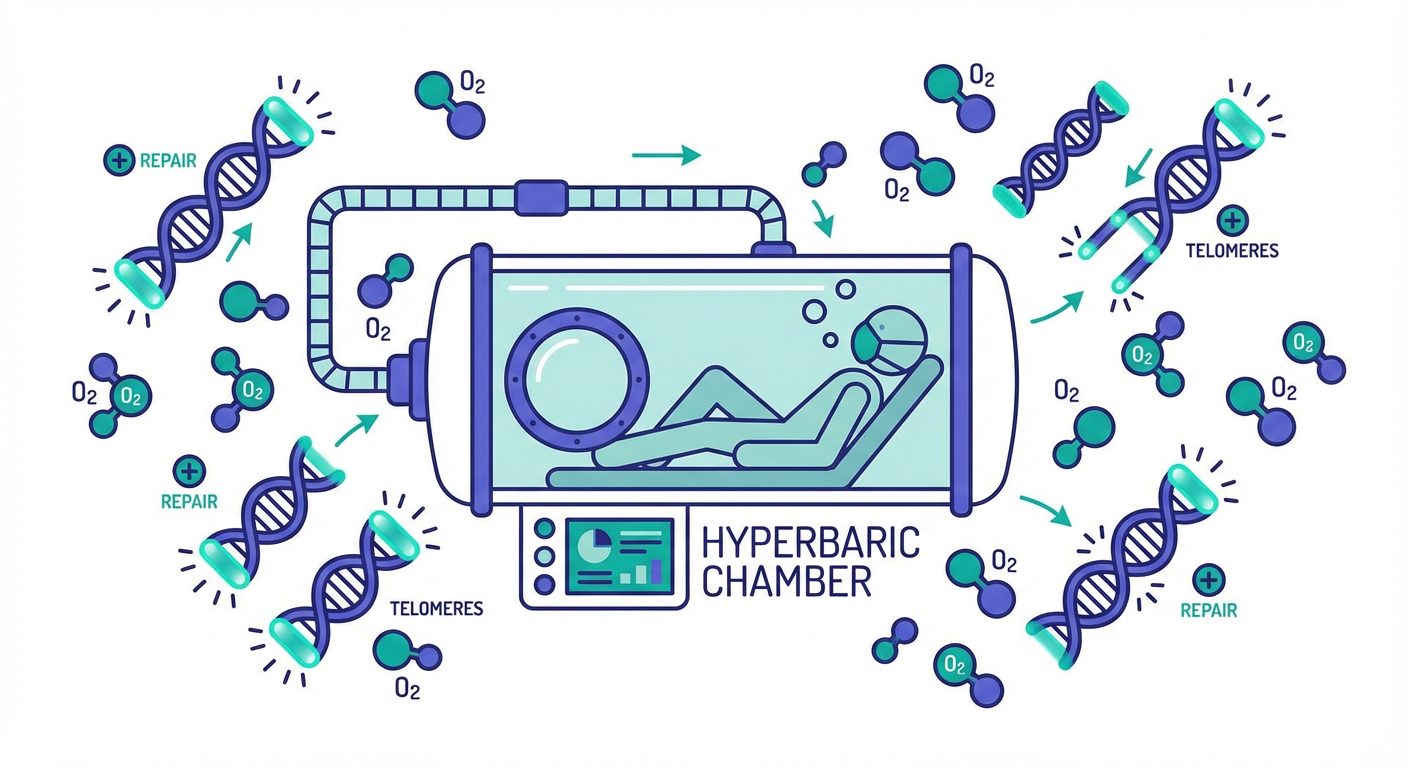
于是,一种更聪明的思路浮出水面。既然完全归零代价太大,那能不能只让细胞“年轻一点”?研究人员开始尝试缩短山中因子的作用时间,不完全抹去细胞的记忆,只是让它的表观遗传时钟往回拨几圈。这就是“部分重编程”的核心逻辑。
它追求的不是一张白纸,而是一张被擦去几道皱纹、但字迹依然清晰的旧纸。细胞保留着原有身份——皮肤细胞还是皮肤细胞,神经细胞还是神经细胞——但它的再生能力、代谢水平回到了更年轻的状态。这种“减龄不重置”的策略,本质上是在年轻化与癌变风险之间走钢丝。重编程程度太浅,效果不明显;重编程过度,细胞可能滑向未分化状态,甚至具备异常增殖能力。
2016年,索尔克研究所的团队率先在小鼠体内实现了这种动态控制:他们周期性开启和关闭山中因子,成功延长了早衰小鼠的寿命,还改善了肌肉和胰腺的再生能力。这证明了一件事:细胞的“年龄”状态,并非不可逆。 关键在于找到那个微妙的平衡点——让细胞变年轻,但不让它忘记自己是谁。
这个平衡点,正是所有“逆转衰老”技术想要攻克的核心。它不是简单的技术问题,而是一场关于“度”的精密艺术:如何让细胞重返青春,却不打开潘多拉魔盒。

二、从概念到人体:首次临床试验为何选择在眼睛里“动刀”?
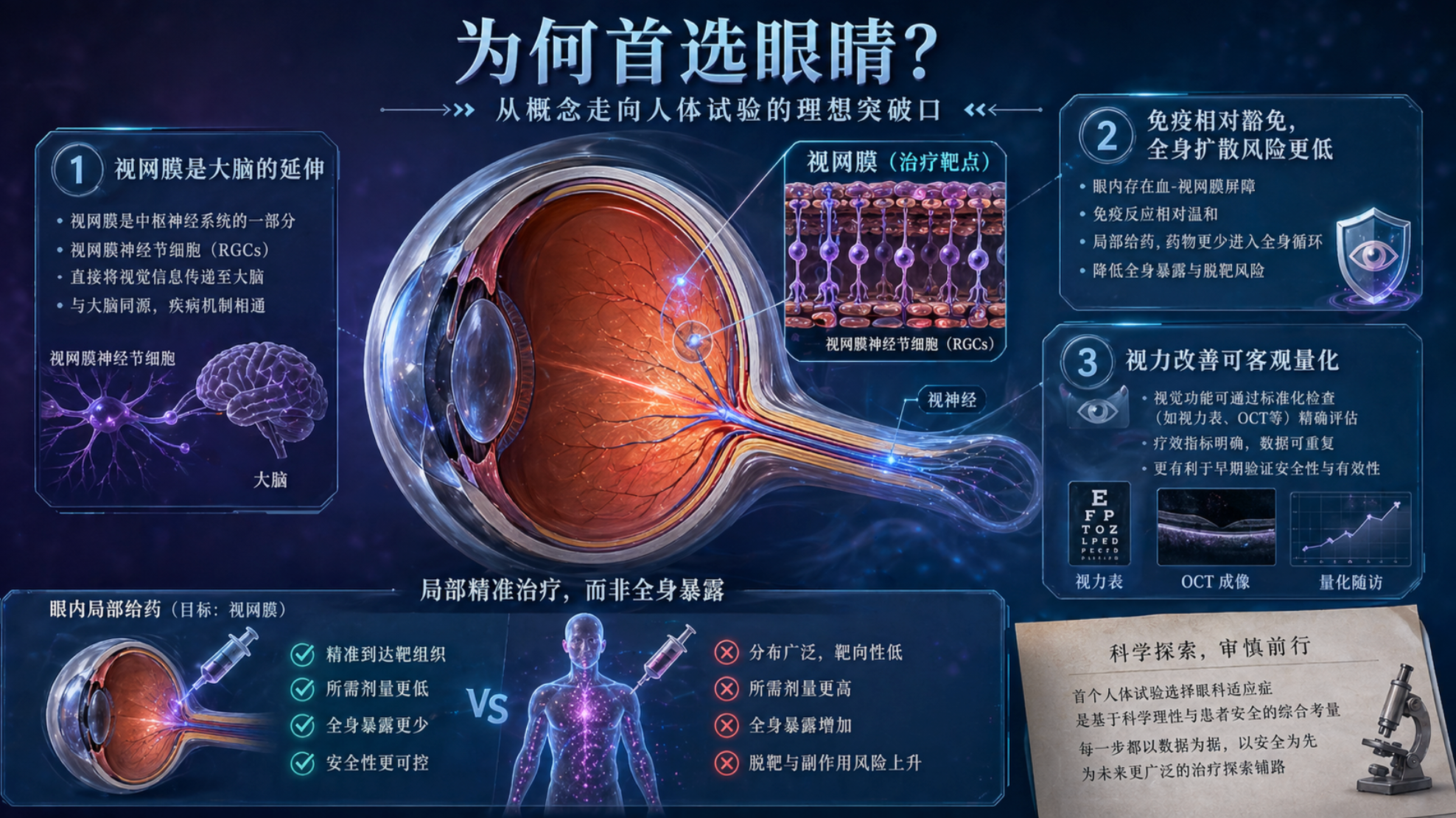
当“逆转衰老”从实验室概念走向人体试验,科学界选择了一个看似保守却极其精明的突破口:眼睛。
这不是偶然。Life Biosciences公司获批的临床试验,目标锁定在两种与年龄相关的视神经病变——开角型青光眼和非动脉炎性前部缺血性视神经病变(NAION)。选择视网膜作为“首战之地”,背后是三重精密考量:视网膜是大脑的延伸,却拥有相对独立的免疫豁免环境,一旦出现意外,全身扩散的风险远低于其他器官;其次,视神经损伤的功能终点明确——视力是否改善,可以客观量化;最重要的是,MIT科学家在小鼠模型中已证实,向视网膜神经节细胞导入三种山中因子,成功让受损的视神经功能恢复,这为人体试验提供了直接的概念验证。
但真正让这场试验成为可能的,是一个精巧的“开关设计”。
精准可控的“基因开关”:8周口服药物如何调控细胞变年轻的程度
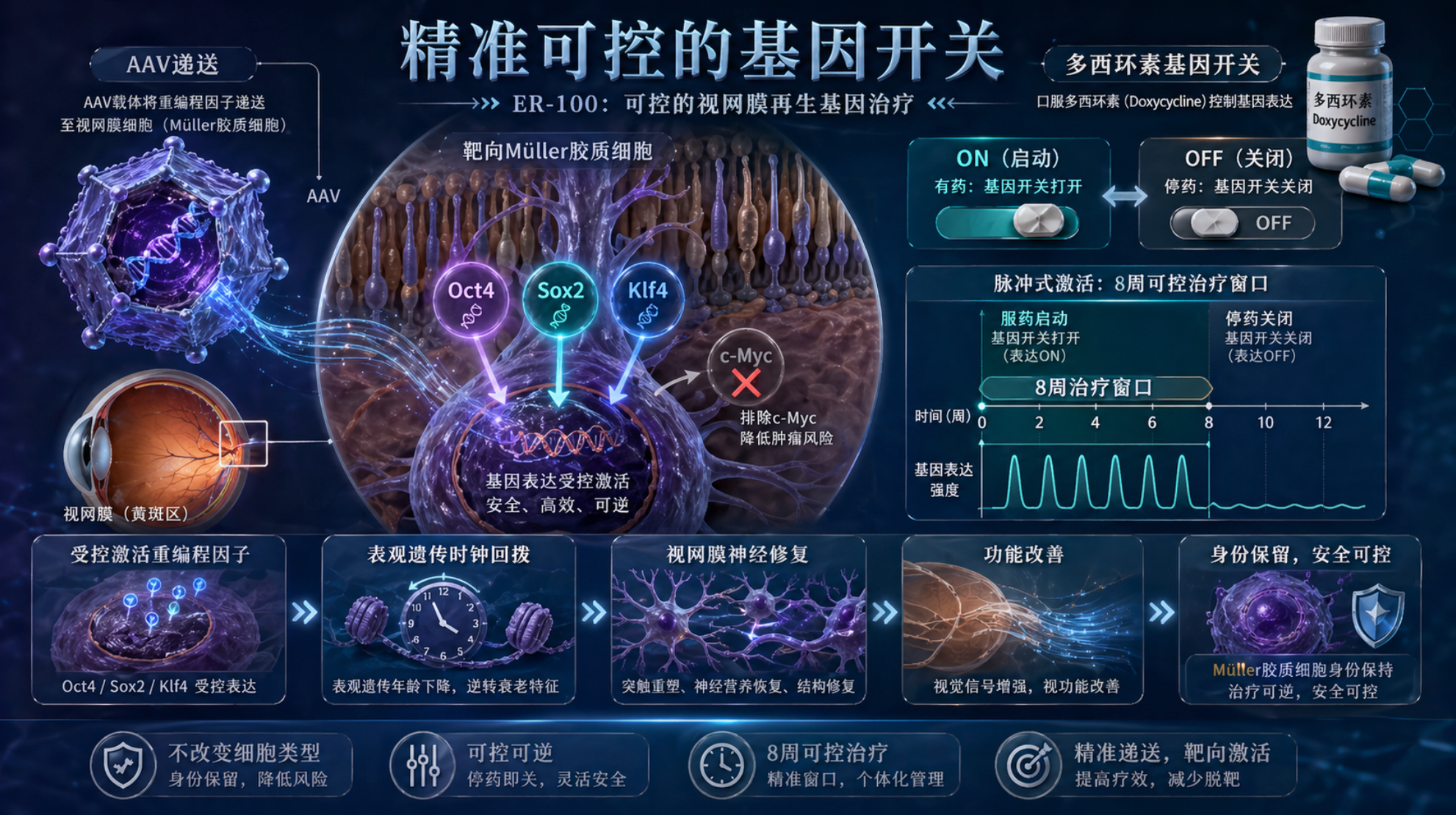
细胞重编程最危险的敌人,是失控。一旦细胞在“变年轻”的路上刹不住车,它们可能退回到完全未分化的干细胞状态,甚至演变为肿瘤。因此,如何精准控制重编程的“剂量”和“时间”,成为临床应用的核心难题。
此次试验采用的基因疗法ER-100,给出了一个巧妙的解决方案。研究人员利用改造后的腺相关病毒(AAV)作为载体,将三种山中因子(Oct4、Sox2、Klf4)送入视网膜细胞。但这三种因子并非“常开”状态——它们被设计成只有在外源药物存在时才会被激活。
这个“开关”就是口服多西环素。患者每天服药,重编程程序启动;停药,程序关闭。试验设计将治疗窗口限定在8周,这意味着细胞的“年轻化”过程被严格限制在可控的时间范围内。相比让重编程因子在体内长期表达,这种“脉冲式”激活策略大幅降低了过度重编程的风险。
在动物实验中,这种策略已展现出诱人的平衡能力:视网膜神经节细胞在保留原有身份的前提下,表观遗传时钟被重置,轴突再生,功能恢复。但动物实验的成功,距离人体安全应用之间,仍横亘着巨大的不确定性。
风险与希望的博弈:12名患者的试验如何权衡视力修复与长期安全

第一阶段的临床试验规模极小——仅招募12名患者,分为两组进行剂量递增。一组是青光眼患者,用于确定安全剂量;另一组是NAION患者,在安全基础上扩展效果验证。试验的首要终点不是“逆转衰老”,而是安全性和耐受性。
这种设计透露着审慎。视神经一旦受损,传统治疗手段极为有限。对于面临失明风险的患者而言,参与试验本身是一场风险与希望的博弈:如果重编程程度不足,可能毫无效果;如果过度,细胞可能丧失功能甚至发生癌变转化。研究团队必须在这条狭窄的安全带上,找到那个“既有效又不危险”的精确剂量。
更棘手的问题在于长期监测。即便8周治疗期内未出现肿瘤,重编程带来的表观遗传改变是否会埋下远期癌变的种子?试验方案要求对参与者进行长期随访,持续监测潜在不良反应。但某些风险可能需要数年甚至更久才会显现。
这场仅有12人的试验,承载的远不止12双眼睛的命运。它是对整个“细胞重编程”长寿赛道的首次人体检验。如果数据证明安全且有效,未来可能推广到肾脏、肝脏、心脏甚至大脑;如果失败,这个领域的资本热潮或将遭遇冰点。科学界对此保持冷静:即便试验成功实现神经再生,这更接近“功能修复”,而非严格意义上的“逆转衰老”。从修复一根视神经到逆转全身衰老,中间隔着至少10-20年的研究鸿沟。

三、潘多拉魔盒开启前:无法忽视的癌变风险与科学界冷思考
如果说“部分重编程”是精准调校细胞时钟的艺术,那么失控便是其硬币的另一面。在细胞“返老还童”的诱惑面前,一个根本性的恐惧始终挥之不去:我们唤醒的,究竟是再生的力量,还是癌变的幽灵?
被剔除的致癌因子:去除c-Myc蛋白是安全保证吗?
在最初的“山中因子”组合中,c-Myc蛋白是公认的致癌元凶。它能强力驱动细胞增殖,但一旦失控,便直接导向肿瘤。因此,Life Biosciences的ER-100疗法做了看似顺理成章的“减法”——将c-Myc剔除,只保留Oct4、Sox2和Klf4三种因子。

小鼠实验中,这种“三因子”方案似乎交出了不错的答卷:全身性导入后数月未观察到明显肿瘤,多项健康指标反而改善。但这张安全证书,真的足够坚实吗?
答案远非如此。去除c-Myc不等于根除癌变风险。重编程过程本身会引发剧烈的表观遗传波动,细胞在“年轻化”的路径上可能滑向任何一种非预期的命运。更关键的是,不同细胞类型对重编程的敏感度天差地别——对视网膜细胞安全的剂量,对肝脏、乳腺或血液细胞可能是过度刺激。这意味着,不存在“一刀切”的安全阈值。
剔除c-Myc只是排除了最显眼的引信,潘多拉魔盒里,还藏着更隐蔽的风险。

富豪的豪赌与科学的审慎:我们离安全地逆转衰老还有多远?
这项技术的商业前景已让硅谷为之沸腾。Altos Labs、Retro Biosciences、NewLimit等公司已吸纳数十亿美元投资,贝索斯、彼得·蒂尔等科技富豪纷纷押注。在他们眼中,细胞重编程是通往“长寿逃逸速度”的终极船票。
然而,科学界的语调要冷静得多。即便此次眼病临床试验获得积极结果,它所证明的也更接近 “功能修复”而非“系统性逆转衰老” 。从修复视神经到逆转全身衰老,中间横亘着巨大的科学鸿沟。专家们列出了一长串必须回答的问题:重编程的精确剂量与频率如何确定?长期癌变风险是否在可接受范围?多器官干预的安全边界在哪里?
更为根本的挑战在于,我们尚未完全理解重编程的作用机制。表观遗传时钟的“回拨”究竟意味着什么?是细胞真正获得了新生,还是仅仅擦除了衰老的表面标记?这些问题没有答案之前,每一次重编程尝试,都是对生命底层代码的试探性修改。
这场豪赌的结局,或许需要10到20年才能揭晓。在资本狂欢与技术憧憬之外,严谨的临床试验和长期随访,才是唯一的判官。

AtomGit 是由开放原子开源基金会联合 CSDN 等生态伙伴共同推出的新一代开源与人工智能协作平台。平台坚持“开放、中立、公益”的理念,把代码托管、模型共享、数据集托管、智能体开发体验和算力服务整合在一起,为开发者提供从开发、训练到部署的一站式体验。
更多推荐
 已为社区贡献10条内容
已为社区贡献10条内容






所有评论(0)