Science 突破!CAR 疗法跨界阿尔茨海默病,星形胶质细胞变身“清道夫”,精准清除 Aβ 斑块
核心看点
-
现有靶向 Aβ 的单抗疗法(如仑卡奈单抗)需高剂量、重复给药,且存在淀粉样蛋白相关影像学异常(ARIA)风险,亟需新型治疗策略。
-
华盛顿大学团队首次将 CAR 技术应用于星形胶质细胞,开发出 CAR-A 疗法,通过单次静脉注射即可在全脑范围高效清除 Aβ 斑块。
-
在 AD 模型小鼠中,CAR-A 既能显著减少已形成的老年斑(晚期治疗),也能从源头预防 Aβ 沉积(早期干预),并重塑胶质细胞稳态。
-
CAR-A 重编程星形胶质细胞直接吞噬 Aβ,同时通过旁分泌信号逆转小胶质细胞耗竭状态,形成星形-小胶质细胞协同抗炎网络。
摘要
阿尔茨海默病(Alzheimer's disease, AD)是一种与年龄相关的中枢神经退行性疾病,是痴呆症最常见的形式。其主要病理特征包括β-淀粉样蛋白(Amyloid-β peptide, Aβ) 聚集形成的老年斑(Senile plaques, SPs)、Tau蛋白异常聚集形成的神经原纤维缠结 (Neurofibrillary tangles, NFTs) 以及大量神经元丢失。近年来,靶向 Aβ 的单克隆抗体疗法(如仑卡奈单抗、多奈单抗)已获 FDA 临床批准,但这类疗法仍存在无法回避的核心局限,如需要高剂量、需重复给药、治疗窗口窄、存在淀粉样蛋白相关影像学异常(ARIA)的风险等。这些挑战凸显了开发新治疗方法的迫切需求。
2026 年 3 月 5 日,华盛顿大学医学院Marco Colonna 团队在国际顶刊Science发表了题为Targeting amyloid-β pathology by chimeric antigen receptor astrocyte (CAR-A) therapy的重磅研究。该研究首次将嵌合抗原受体(CAR)技术创新性应用于大脑星形胶质细胞,开发出靶向 β 淀粉样蛋白(Aβ)的 CAR-A 疗法,仅需单次非侵入式静脉给药,即可在阿尔茨海默病(AD)模型小鼠中实现全脑范围的 Aβ 斑块高效清除,同时重塑神经胶质细胞稳态,为 AD 这一 “绝症” 带来了全新的疾病修饰治疗策略。
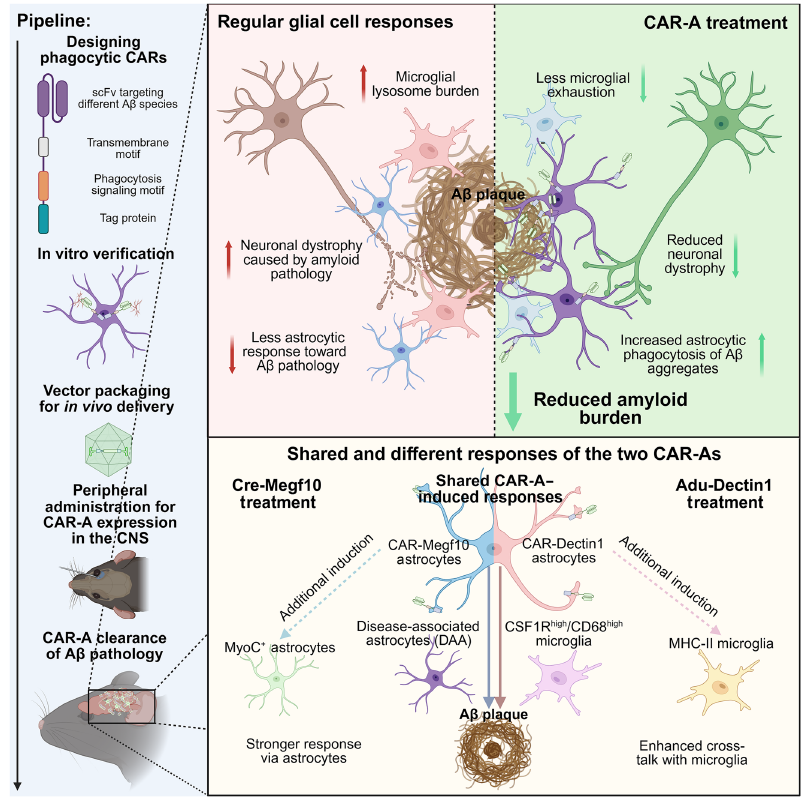
研究结果
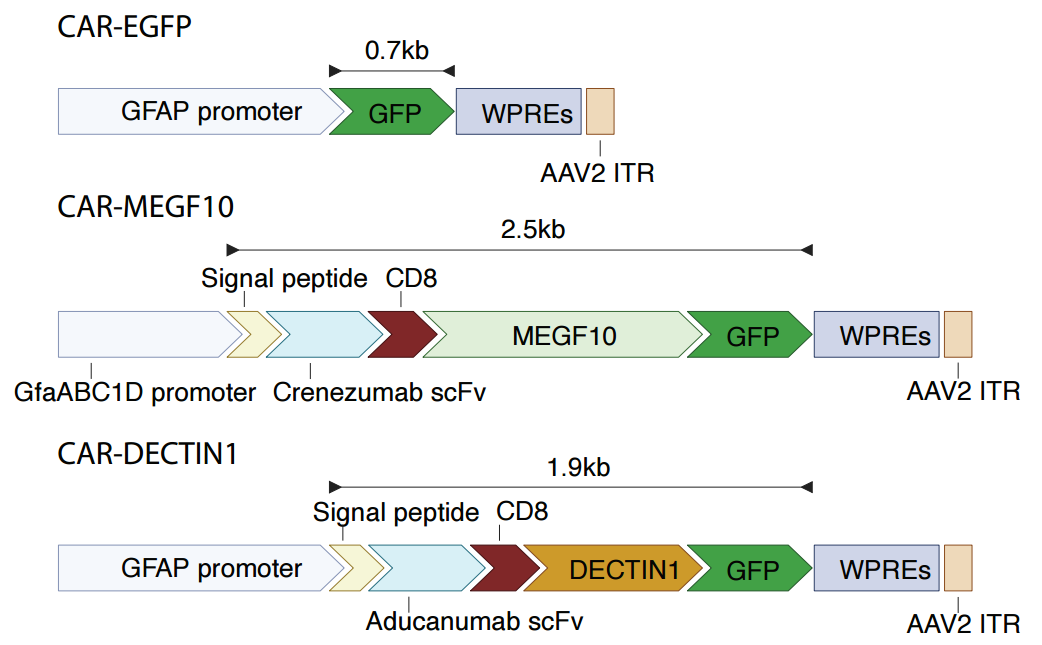
1. CAR模块化设计
首先,研究团队设计了一个工程化CAR系统的框架,将抗Aβ单链可变片段(scFv)与吞噬受体的胞内结构域融合。作者选择了三种在中枢神经系统吞噬细胞中表达并具有直接吞噬能力的受体:MEGF10(星形胶质细胞表达)、Dectin1(小胶质细胞表达)和MERTK(两种胶质细胞均表达),以及一个CAR-T经典信号结构域CD3ζ。
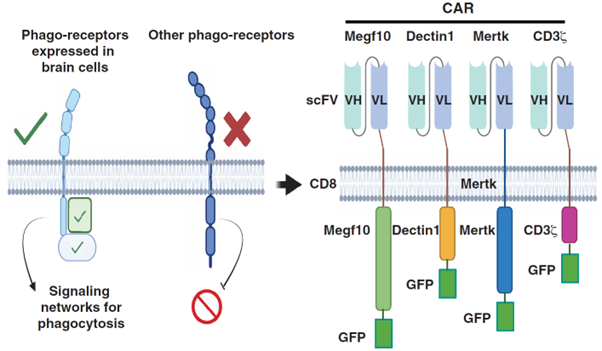
随后,研究团队使用抗Aβ单克隆抗体(crenezumab,Cre)的scFv序列进行初步筛选,发现这4 种 CAR 均能在永生化和原代星形胶质细胞中稳定表达,显著增强细胞对 Aβ42 的吞噬与降解能力,且吞噬作用具有严格的抗原特异性 —— 仅靶向 Aβ,不会非特异性吞噬 tau 蛋白、α- 突触核蛋白、髓鞘碎片等 AD 相关病理分子。
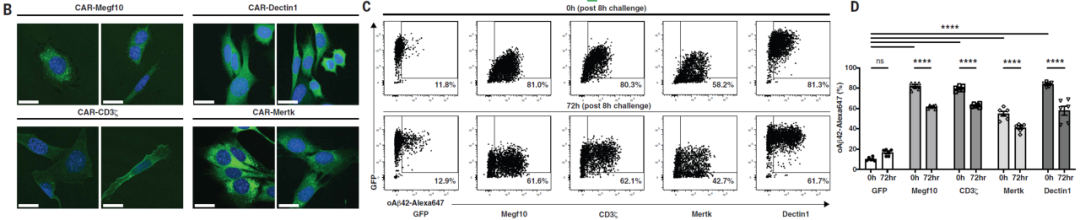
2. CAR-A筛选优化
既往临床试验表明,抗Aβ单克隆抗体清除斑块的疗效取决于其对纤维状而非可溶性Aβ的优先结合能力。因此 ,研究团队筛选了不同的scFv组件来优化Megf10和Dectin1-CAR的应用效果。他们选择了两种scFv:crenezumab(Cre,可结合多种形式的Aβ,如可溶性、寡聚体和纤维状)和aducanumab(Adu,优先结合Aβ寡聚体)。借助慢病毒载体转导原代星形胶质细胞,结果显示,Cre-Megf10表达导致星形胶质细胞对Aβ吞噬能力较其他载体更强,而Cre-Dectin1和Adu-Dectin1显示出相似的Aβ吞噬增强效果。基于这些数据,研究团队优先选择了两种CAR载体——Cre-Megf10和Adu-Dectin1用于体内验证。
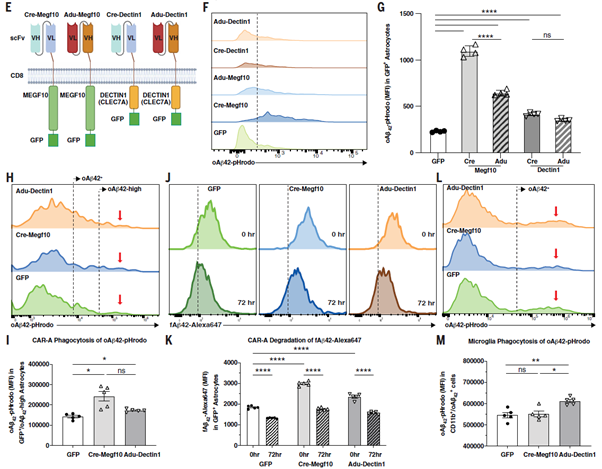
3. CAR-A 高效清除 Aβ,兼具治疗与预防双重潜力
接下来,为了体内验证CAR-A的效果,研究团队借助AAV-PHP.eB(可跨血脑屏障的AAV血清型)搭配GFAP(星形胶质细胞特异性启动子)策略,通过静脉注射实现在全脑星形胶质细胞中表达CAR。作者在5xFAD AD模型小鼠中,分别验证了CAR-A 疗法的晚期治疗效果与早期预防潜力。
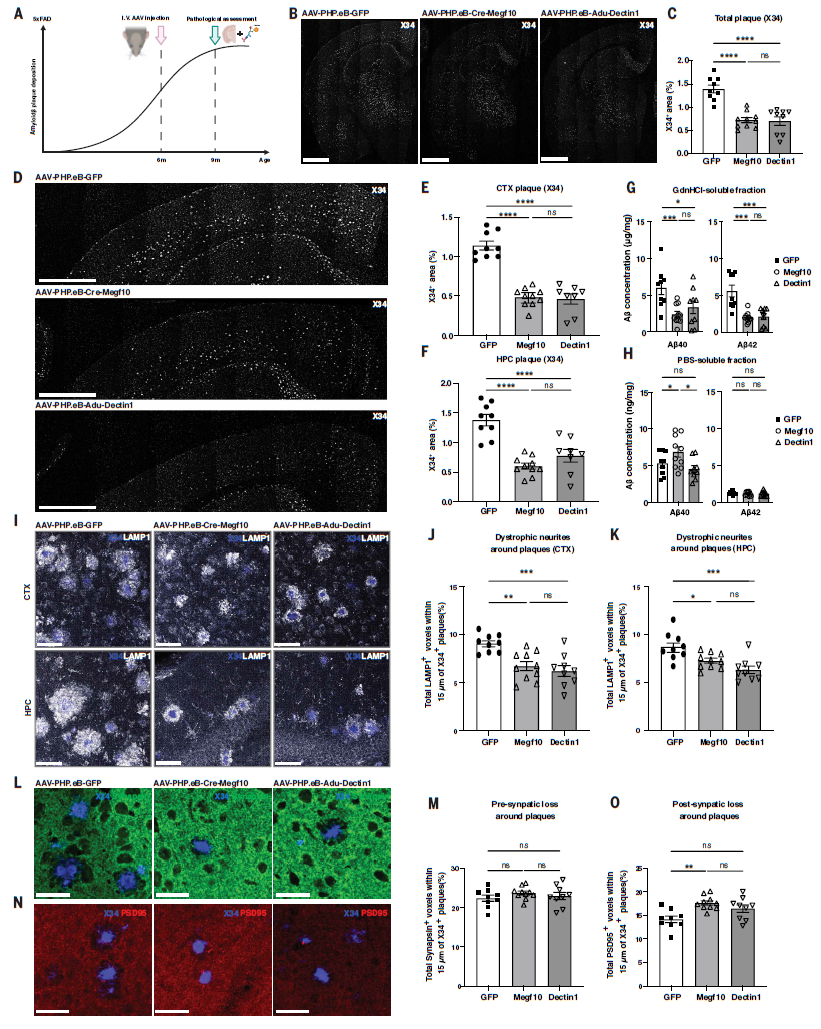
晚期治疗:单次注射显著减少淀粉样斑块负荷
研究团队在6月龄5xFAD小鼠中静脉注射AAV-PHP.eB-CAR-A(AAV-PHP.eB-Cre-Megf10和AAV-PHP.eB-Adu-Dectin1), 3个月后评估Aβ斑块变化。结果显示,两种CAR-A均促使小鼠全脑总 Aβ 斑块下降约 50%,其中大脑皮层和海马区的Aβ斑块显著减少,不溶性Aβ1-42寡聚体显著降低。此外,LAMP1染色结果显示,斑块周围的营养不良神经突体积显著降低,其中 Cre-Megf10 治疗组还显著改善了突触后的丢失表型,改善了突触完整性。
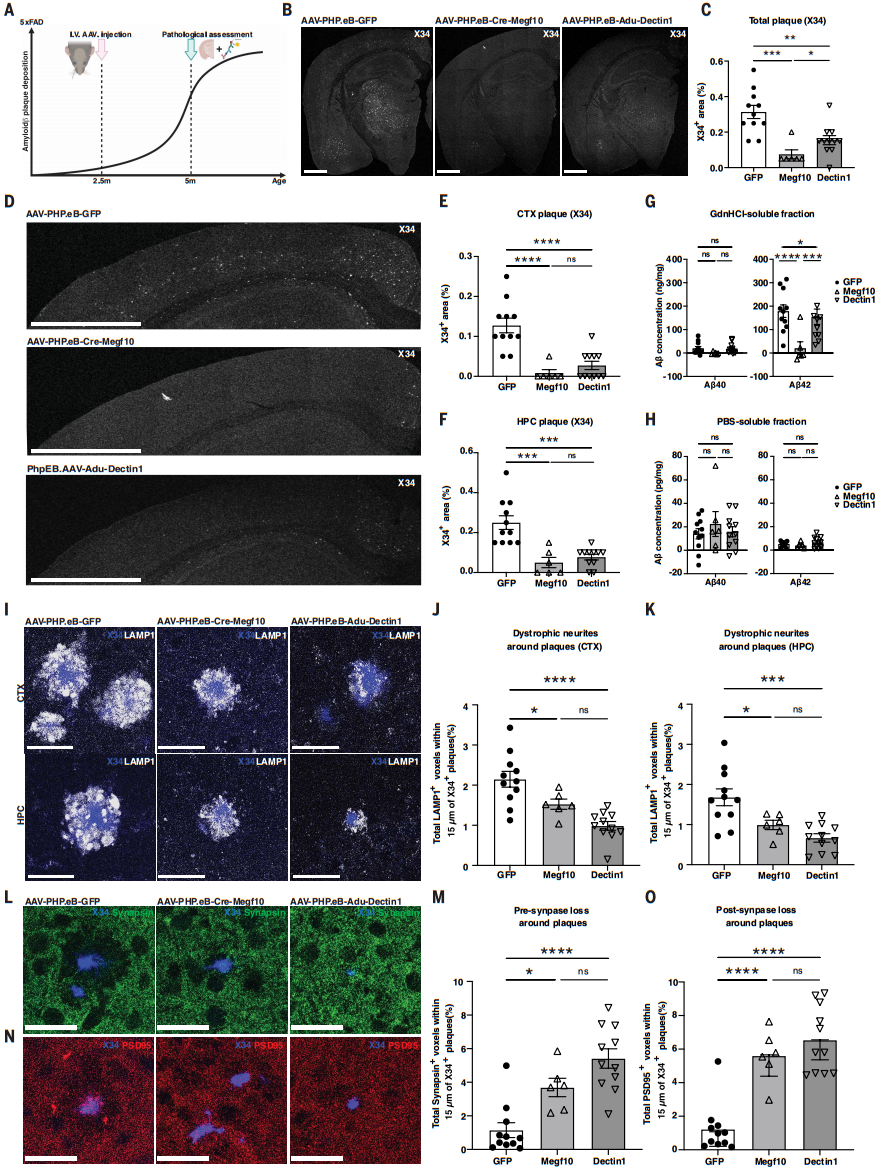
早期干预:预防淀粉样蛋白沉积效果更佳
进一步,研究团队探索了两种CAR-A疗法作为预防策略的潜力。他们在2.5月龄5xFAD 小鼠(尚未出现Aβ斑块)中静脉注射AAV-PHP.eB-CAR-A,2.5个月后检测发现,AAV-PHP.eB-Cre-Megf10组小鼠大脑几乎检测不到Aβ斑块,AAV-PHP.eB-Adu-Dectin1组也显著抑制斑块的形成。此外,两种CAR-A均有效改善了突触丢失,从源头阻断了 Aβ 引发的神经退行性级联反应。
尽管 CAR-A 疗法实现了显著的病理改善,然而行为学结果显示,在不同月龄的小鼠中,均未观察到记忆相关行为学的显著提升。这他们对此提出了几种可能的解释:首先,AAV 载体本身引发了小鼠轻微的运动行为改变,对认知行为学检测结果造成了干扰;其次,CAR-A 增强的吞噬活性可能意外促进了突触修剪,部分抵消了 Aβ 清除带来的获益;以及5xFAD 模型本身存在行为学表型异质性的固有局限,需在更多模型中通过更全面的行为学测试验证。
4.机制研究:CAR-A 重塑神经胶质细胞网络,协同对抗 AD 病理
为进一步解析CAR-A 疗法的分子和细胞机制,作者借助单细胞核 RNA 测序(snRNA-seq)、免疫荧光等技术发现星形胶质细胞与小胶质细胞的协同调控网络。
CAR-A 重编程星形胶质细胞,激活其吞噬与保护功能
结果显示,两种CAR-A 均显著激活了疾病相关星形胶质细胞(DAA,具有病理作用) 亚群,这些DAA积极地向斑块周围聚集,并上调了LRP1这种能结合并清除淀粉样蛋白受体的表达。此外,Cre-Megf10 还特异性激活了TA2 过渡态星形胶质细胞→MyoC + 星形胶质细胞的分化轨迹,该亚群富集突触调控与脂质代谢相关通路,与突触完整性的维持密切相关,这也解释了为何仅 Cre-Megf10 组实现了突触丢失的挽救。

CAR-A 逆转小胶质细胞耗竭,重塑其稳态表型
不仅如此,CAR-A疗法可通过星形胶质细胞 - 小胶质细胞的交互作用,间接影响小胶质细胞的状态。在AD 病理中,小胶质细胞会进入持续活化的疾病相关小胶质细胞(DAM)状态,最终发生功能耗竭,无法有效清除 Aβ。而经过CAR-A治疗后,这些耗竭的小胶质细胞比例显著下降,取而代之的是一类全新的、高表达CSF1R/CD68小胶质细胞亚群,该亚群同时表达稳态标志物与吞噬相关基因,是一种介于稳态与活化之间的中间态,既保留了强大的吞噬功能,又避免了过度活化导致的炎症损伤与耗竭。Adu-Dectin1 还特异性扩增了 MHC-II 高表达的小胶质细胞亚群,通过抗原提呈进一步增强了脑内的免疫清除效应,这也是两款 CAR-A 下游效应的核心差异。
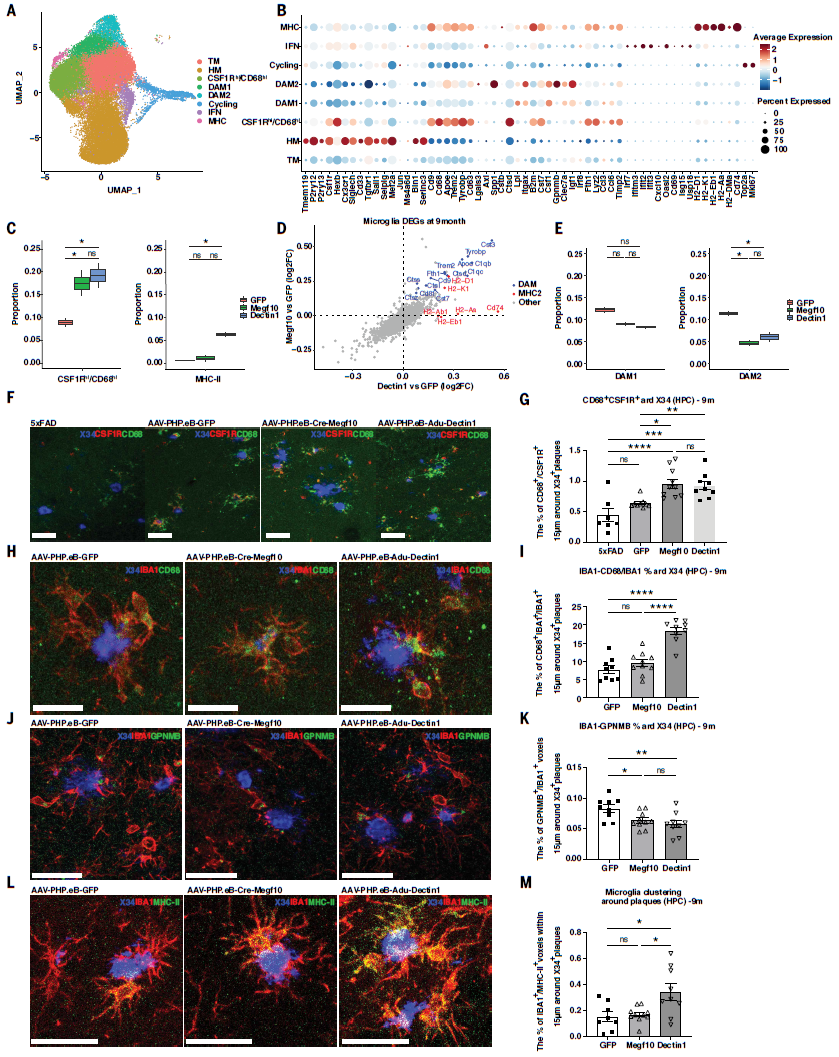
星形胶质细胞 - 小胶质细胞的协同调控轴
最后,作者通过配体 - 受体互作分析发现,CAR-A 治疗后,星形胶质细胞通过 Vcam1、Clu、Apoe 等配体,与小胶质细胞的 Trem2、Itga5 等受体形成了稳定的通讯网络,实现了两种胶质细胞的协同激活:星形胶质细胞直接承担了主要的 Aβ 清除工作,同时通过旁分泌作用缓解小胶质细胞的吞噬压力与耗竭状态,让小胶质细胞回归更健康的功能表型,二者共同对抗 AD 病理。
值得注意的是,两种CAR构建物在下游效应上存在差异。在早期预防阶段,Cre-Megf10更有效地限制斑块形成,这可能反映其更广泛的结合谱,因为crenezumab识别可溶性和寡聚体Aβ种类。在晚期治疗阶段,Cre-Megf10还增加了与分化和脂质代谢相关的MyoC+星形胶质细胞群体。相比之下,Adu-Dectin1诱导了更强的小胶质细胞聚集和激活,并特异性增加了MHC-II+/IBA1+小胶质细胞。这些结果表明,星形胶质细胞介导的Aβ清除以构建物特异性和阶段依赖性方式塑造胶质细胞反应。
结论
本研究设计了四种不依赖FcRγ信号的抗Aβ CAR,并筛选出Cre-Megf10和Adu-Dectin1两种高效构建物。通过一次性、非侵入性的静脉注射,将携带抗Aβ CAR递送到大脑星形胶质细胞中,使其能够持久、高效清除Aβ斑块,并实现持续至少3个月的CAR表达。同时,揭示了AD 病理中星形胶质细胞 - 小胶质细胞的协同调控新机制,证明了星形胶质细胞可作为核心效应细胞补充甚至替代小胶质细胞的吞噬功能,为 AD 乃至其他神经退行性疾病的免疫治疗提供了全新的理论基础与研发思路。
FAQ
Q1:CAR-A 疗法与传统 CAR-T 有何不同?为何选择星形胶质细胞而非 T 细胞?
A:传统 CAR-T 利用 T 细胞的细胞毒性杀伤肿瘤细胞;而 CAR-A 将抗 Aβ 的 scFv 与吞噬受体胞内域(如 MEGF10、Dectin1)融合,赋予星形胶质细胞特异性吞噬并降解 Aβ 斑块的能力。选择星形胶质细胞是因为其在中枢神经系统中数量庞大、易于通过静脉递送 AAV 靶向,且不引发 T 细胞相关的过度免疫炎症反应。
Q2:为什么选择 AAV 作为 CAR-A 疗法的递送载体?它相比其他病毒或非病毒载体有何优势?
A:AAV 具有高安全性(极少整合到宿主基因组)、低免疫原性、可长期稳定表达外源基因(在非分裂细胞如星形胶质细胞中可持续数月以上)等核心优势。本研究特别采用 AAV-PHP.eB 血清型,该变体可通过静脉注射高效穿越小鼠血脑屏障,实现全脑星形胶质细胞转导。相比之下,慢病毒难以跨屏障且需局部注射,脂质纳米颗粒(LNP)虽可递送 mRNA 但表达时间短。AAV 的“单次给药、长效表达”特性完美契合 CAR-A 需要星形胶质细胞持续清除 Aβ 的需求
和元生物目前已配备文章中涉及到的现货载体及CAR骨架,可根据客户需求更改启动子及靶点序列,以实际行动助力基础科学研究!

AtomGit 是由开放原子开源基金会联合 CSDN 等生态伙伴共同推出的新一代开源与人工智能协作平台。平台坚持“开放、中立、公益”的理念,把代码托管、模型共享、数据集托管、智能体开发体验和算力服务整合在一起,为开发者提供从开发、训练到部署的一站式体验。
更多推荐
 已为社区贡献9条内容
已为社区贡献9条内容







所有评论(0)