【论文】Bethesda细胞检测的多阶段优化管道
Bethesda细胞检测的多阶段优化管道论文解读
论文基本信息
英文标题: A Multi-Stage Optimization Pipeline for Bethesda Cell Detection in Pap Smear Cytology
中文标题: 用于Pap Smear细胞学中Bethesda细胞检测的多阶段优化管道
arXiv链接: https://arxiv.org/abs/2604.13939
代码链接: http://github.com/martinamster/riva-trackb
提交日期: 2026年4月15日
论文状态: ISBI 2026接收论文 & RIVA宫颈细胞学挑战赛Track B第二名解决方案
1. 摘要分析
核心研究问题
宫颈癌是全球女性第四大常见癌症和第四大癌症死亡原因,2020年估计有60.4万新病例和34.2万死亡病例。尽管Pap smear筛查的广泛实施从根本上改变了早期检测和患者预后,但这些计划的功效仍然严重依赖于对细胞学样本的人工解释。这种传统方法本质上是劳动密集型的,容易受到人为因素的影响,包括观察者间变异性和高工作量下的疲劳,这可能会损害诊断敏感性。
深度学习的集成为通过自动化健康细胞与病理细胞的分类来支持细胞病理学家提供了一条变革性路径。然而,尽管在计算细胞分析方面取得了显著进展,在Pap smear分类中实现稳健的泛化仍然是一个持续的挑战。主要障碍是缺乏反映临床实践中遇到的生物多样性的高质量大规模数据集。
核心方法
本文介绍了一种新的框架,用于Pap smear图像中Bethesda细胞的检测,该框架是为与国际生物医学成像研讨会(ISBI)相关的Riva细胞学挑战赛Track B开发的。这项工作专注于增强细胞检测的计算机视觉模型,使用mAP50-95指标进行性能评估。
论文提出了一种基于YOLO和U-Net架构集成的解决方案,随后是利用重叠去除技术和二进制分类器的优化阶段。该框架在比赛中以0.5909的mAP50-95分数获得了第二名。
主要贡献
- 多模型集成策略: 提出了一种集成YOLO和U-Net架构的方法,结合了目标检测和热图回归的优势
- 预处理优化: 创新性地调整了标准100×100像素注释的大小,以更好地反映实际的细胞形态
- 三阶段优化管道: 设计了NMS、空间密度过滤和二进制分类细化的后处理流程
- 性能平衡: 在高召回率(YOLO)和高精确率(U-Net)之间取得了良好平衡
- 实用价值: 为临床应用提供了可行的解决方案,代码完全开源
技术意义
这项工作为医学图像分析中的细胞检测提供了新的解决方案,特别是在Pap smear细胞学领域。通过集成不同的深度学习架构和精细的后处理管道,该系统在保持高召回率的同时显著提高了检测精度,这对于临床应用至关重要。
2. 研究现状
2.1 医学图像分析的发展
传统方法: 传统的Pap smear筛查主要依赖人工显微镜检查,这种方法虽然准确但效率低下,且容易受到病理学家经验和疲劳的影响。
计算细胞分析的兴起: 随着数字病理学的发展,计算细胞分析技术逐渐成熟。早期的数字图像分析主要基于传统的计算机视觉技术,如形态学分析、纹理分析和颜色分析。
深度学习的突破: 近年来,深度学习技术在医学图像分析中取得了突破性进展。卷积神经网络(CNNs)、深度残差网络、注意力机制等新技术被广泛应用于细胞检测、分类和分割任务中。
2.2 Pap smear分析的技术挑战
数据集局限性: 一个主要障碍是缺乏大规模、高质量的Pap smear数据集。大多数公开数据集样本数量有限,或者不能很好地反映临床实践中的生物多样性。这限制了模型在真实世界环境中的泛化能力。
标注标准化: 传统的100×100像素标准化边界框标注方法存在局限性,因为它们不能准确反映不同大小和形状的实际细胞形态。
类别不平衡: 在临床环境中,异常细胞通常比正常细胞少得多,这导致了严重的类别不平衡问题。
计算效率与准确性平衡: 在临床应用中,需要在计算效率和高检测准确性之间取得平衡。
2.3 相关研究进展
RIVA数据集: 为了弥合数据集质量差距,Perez Bianchi等人(2025)引入了RIVA数据集,为开发先进的检测和分类算法提供了标准基准。图1展示了RIVA数据集中标注图像的示例。
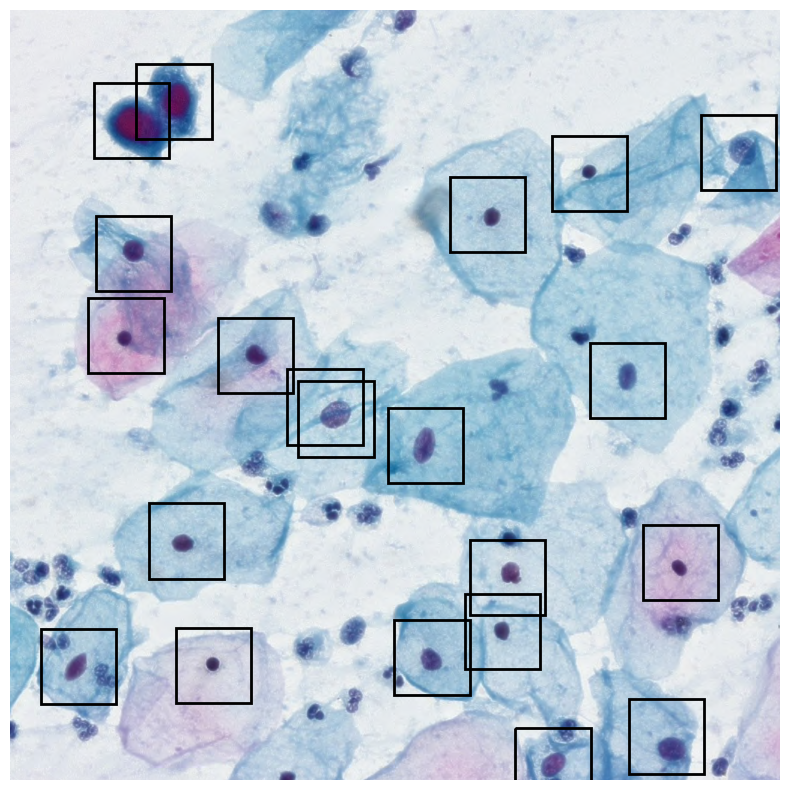
检测算法发展: 目标检测算法如YOLO、Faster R-CNN、SSD等在细胞检测中得到广泛应用。然而,每种方法都有其优势:YOLO速度快,Faster R-CNN精度高,但单种方法往往难以同时实现高召回率和高精确率。
集成方法: 近年来,集成学习在医学图像分析中越来越受欢迎。通过组合多个模型的预测,可以同时提高检测的鲁棒性和准确性。
3. 创新点
3.1 创新的预处理策略
问题识别: 论文识别出数据集的统一100×100像素标注限制,这些标注经常无法代表实际的细胞形态。
解决方案: 为了优化中心定位,将注释调整为从10×10到120×120像素的固定边界框尺寸。此调整通过保持每个框的原始中心坐标,同时系统性地调整其宽度和高度来执行。在推理过程中,模型的预测宽度和高度被标准化回固定100×100格式。
创新性: 这种预处理策略是创新的,因为它在模型训练前就考虑了细胞的实际形态变化,而不是依赖标准化的标注格式。
3.2 双重模型集成架构
YOLO集成: 集成了两个YOLOv8n模型,专门用20×20和50×50像素边界框训练,以捕获不同级别的空间上下文。两种YOLO模型都在1024×1024的输入分辨率下训练多达150个epoch(批次大小16),在推理时应用测试时增强以进一步提高召回率。
U-Net补充: 使用具有在ImageNet上预训练的ResNet34骨干网络的U-Net模型。该模型被训练为热图回归器:对于每个标注的细胞中心,渲染2D高斯核(sigma与目标分辨率下预期框大小的1/6成比例)到float32热图上,网络被优化以使用MSE损失重现这些热图。
互补优势: 基于分割的方法(U-Net)显示的召回率低于YOLO检测器,但表现出显著更高的精确度,为集成提供了互补的高质量检测。
3.3 三阶段优化管道
这是论文最核心的创新,设计了一个精巧的三阶段后处理流程:
阶段1:非最大值抑制(NMS):
- 集成后,通过NMS抑制来自模型重叠预测的重复检测
- 候选者按置信度排序并迭代过滤:与更高置信度检测的重叠度大于0.75的任何框都被丢弃
- 选择0.75阈值的原因:保留密集堆积的邻近但不同的细胞,避免合并合理的相邻检测
阶段2:空间密度过滤:
- 每个图像被分割为4×4的相等象限网格
- 在高密度象限(至少30个检测)中,候选者的高体积通常与模型不确定性相关,这会产生许多低置信度的虚假预测,因此应用0.1的置信度阈值
- 在低密度象限(少于30个检测)中,即使是弱信号也可能对应于孤立的异常细胞,阈值被放松到0.001以避免丢弃可能相关的检测
阶段3:二进制分类细化:
- 为了缓解低置信度集成预测(<0.01)中的误报,训练了EfficientNet-B0二进制分类器来区分合法的细胞形态与背景伪影
- 训练集通过硬负挖掘构建:真值框被标记为细胞,而相对于任何真值IoU < 0.1的预测被标记为垃圾
- 模型使用加权二进制交叉熵损失进行微调,以考虑类别不平衡和标准增强(翻转、旋转和颜色抖动)
3.4 比赛指标优化
创新目标: 与传统优化不同,该方法专门针对mAP50-95指标进行优化,这是比赛的官方评估标准。
指标理解: mAP50-95是IoU阈值从0.50到0.95的平均精度,这奖励在广泛重叠级别上紧密定位目标的预测。
优化策略: 通过设置置信度阈值为零,保留所有来自YOLO集成或U-Net模型的不匹配检测,有效地增强了确证检测的置信度,同时保留了个体预测的完整集合。
4. 数据集对比分析
4.1 RIVA数据集概述
数据规模:
- 总样本数:959张高分辨率Pap smear图像块(1024×1024像素)
- 训练集:828张图像
- 验证集:131张图像
标注特点:
- 每个图像包含标准化为100×100像素的边界框,以细胞核为中心
- 所有图像都经过细胞病理学专家的仔细标注
- 涵盖Bethesda分类系统的各种细胞类型
数据质量:
- 高分辨率图像,有利于细胞形态的详细分析
- 标准化的注释格式,便于不同方法之间的公平比较
- 反映了临床实践中的生物多样性
4.2 数据集挑战与特点
标注限制:
- 统一100×100像素边界框不能准确反映实际的细胞形态变化
- 一些细胞可能需要更小或更大的边界框
生物学多样性:
- 数据集包含各种细胞类型,包括正常和病理细胞
- 不同的细胞密度,从稀疏到密集分布
- 变化的图像质量和染色条件
计算环境:
- 所有模型训练和推理都在Kaggle Notebooks环境中进行
- 利用双NVIDIA Tesla T4 GPU(2×16 GB VRAM)进行加速计算
- 标准化的计算环境确保了不同方法之间的可比性
4.3 数据集对比意义
临床相关性: 与实验室环境中的合成数据集不同,RIVA数据集反映了真实的临床Pap smear样本,包括常见的挑战如变化的质量、不同的密度和多种细胞类型。
基准价值: 作为一个标准化基准,RIVA数据集使得不同研究团队的方法能够进行公平比较,推动了该领域的技术进步。
泛化测试: 数据集的训练/验证分割允许评估模型的泛化能力,这是临床部署的关键要求。
5. 算法结构图与详细分析
5.1 系统整体架构
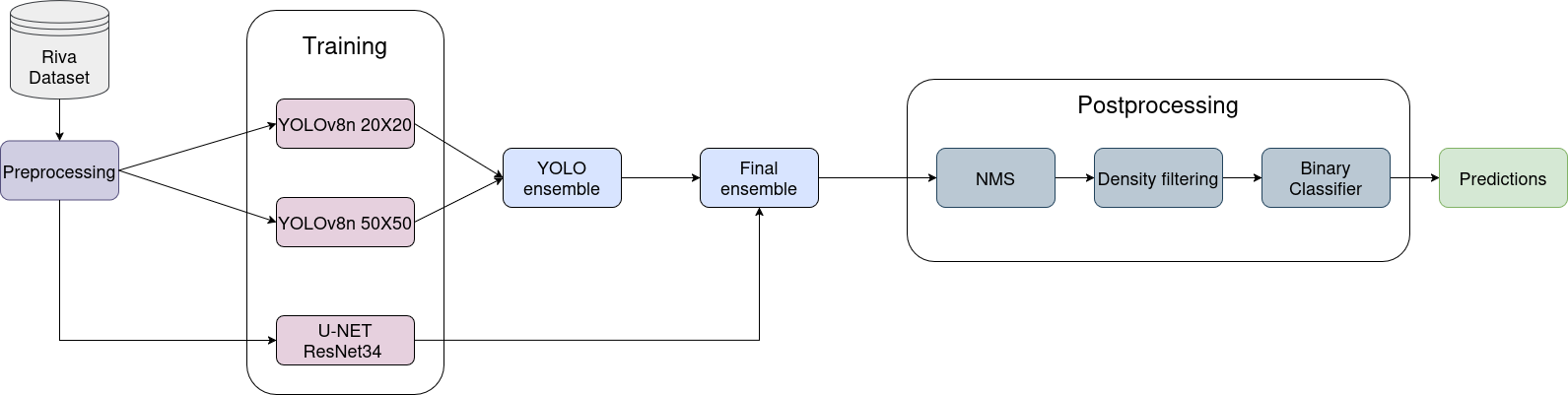
图表分析:
图2展示了完整的架构和优化管道,这是一个端到端的细胞检测系统。从图中可以看出系统的核心组成部分:
1. 预处理阶段:
- 图像输入:1024×1024像素的Pap smear图像
- 标注调整:从统一的100×100像素调整到多个尺寸(10×10到120×120)
- 数据增强:包括翻转、旋转和颜色抖动
2. YOLO检测器:
- YOLOv8n 20×20:小尺度检测模型
- YOLOv8n 50×50:中尺度检测模型
- 集成策略:结合两个YOLO模型的输出
- 距离阈值:12像素
- 置信度阈值:0.35
3. U-Net热图回归:
- ResNet34骨干网络
- ImageNet预训练
- 热图生成:高斯核标注
- 多尺度推理:0.8×, 1.0×, 1.2×
4. 集成融合:
- 二次集成:结合YOLO集成和U-Net输出
- 距离阈值:12像素
- 置信度阈值:0
- 策略:保留所有不匹配检测
5. 三阶段优化管道:
- NMS:IoU阈值0.75
- 空间密度过滤:高密度象限阈值0.1,低密度象限阈值0.001
- 二进制分类:EfficientNet-B0,置信度阈值0.05
5.2 核心技术模块分析
YOLO集成策略:
- 使用两个不同尺度的YOLO模型捕获不同大小的细胞
- 基于欧几里得距离的集成方法,确保同一细胞的检测结果融合
- 测试时增强提高召回率,这对细胞检测任务至关重要
U-Net热图回归:
- 将检测问题转换为热图回归问题
- 使用2D高斯核创建精确的细胞中心标注
- 多尺度推理策略提高定位精度
- 局部最大值抑制提取细胞中心
三阶段优化管道:
- NMS阶段: 去除重复检测,但保持宽松的IoU阈值以保留紧密堆积的细胞
- 空间密度过滤: 自适应阈值策略,根据细胞密度调整严格程度
- 二进制分类: 使用专门训练的分类器过滤低置信度检测,减少误报
5.3 架构设计亮点
互补性设计: YOLO和U-Net在检测任务上具有互补优势:YOLO召回率高,U-Net精确率高,集成结合了两者的优势。
渐进优化: 通过三个独立的优化阶段,每个阶段解决特定的检测问题(重复、噪声、误报),实现了渐进的性能提升。
临床实用性: 虽然针对比赛指标优化,但设计考虑了实际应用需求,如在不同密度下的鲁棒性。
6. 算法预测结果与性能分析
6.1 实验结果对比
表1:RIVA验证集上的定量评估
| 模型 | TP | FP | Recall | Precision | F1 | mAP50-95 |
|---|---|---|---|---|---|---|
| YOLOv8n 20×20 | 2654 | 30472 | 0.9896 | 0.0801 | 0.1482 | 0.5966 |
| YOLOv8n 50×50 | 2665 | 37398 | 0.9937 | 0.0665 | 0.1247 | 0.6059 |
| YOLO集成 | 2647 | 19403 | 0.987 | 0.12 | 0.2141 | 0.6153 |
| U-Net | 2141 | 944 | 0.7983 | 0.694 | 0.7425 | 0.5494 |
| 最终预测 | 2544 | 11410 | 0.9485 | 0.1823 | 0.3058 | 0.6232 |
结果分析:
YOLO模型性能:
- YOLOv8n 50×50达到了独立检测器中最高的敏感性,产生了2665个真阳性(TP)和0.9937的召回率
- 但代价是过量的误检测(37398个FP),精确率仅为0.0665
- 通过集成两个YOLO变体,显著减少了FP数量,同时保持了稳定的TP率
U-Net模型性能:
- U-Net模型显示了最低的TP计数(2141),但由于更好的精确率和最小的FP率,F1分数显著更高(0.7425)
- 与基于YOLO的架构相比,U-Net在精确度方面表现出色
最终集成性能:
- 最终集成,通过提出的优化管道完善,达到了0.6232的峰值mAP50-95分数
- 召回率0.9485仍然很高,精确率提高到0.1823
- F1分数达到0.3058,实现了召回率和精确率之间的良好平衡
6.2 性能曲线分析
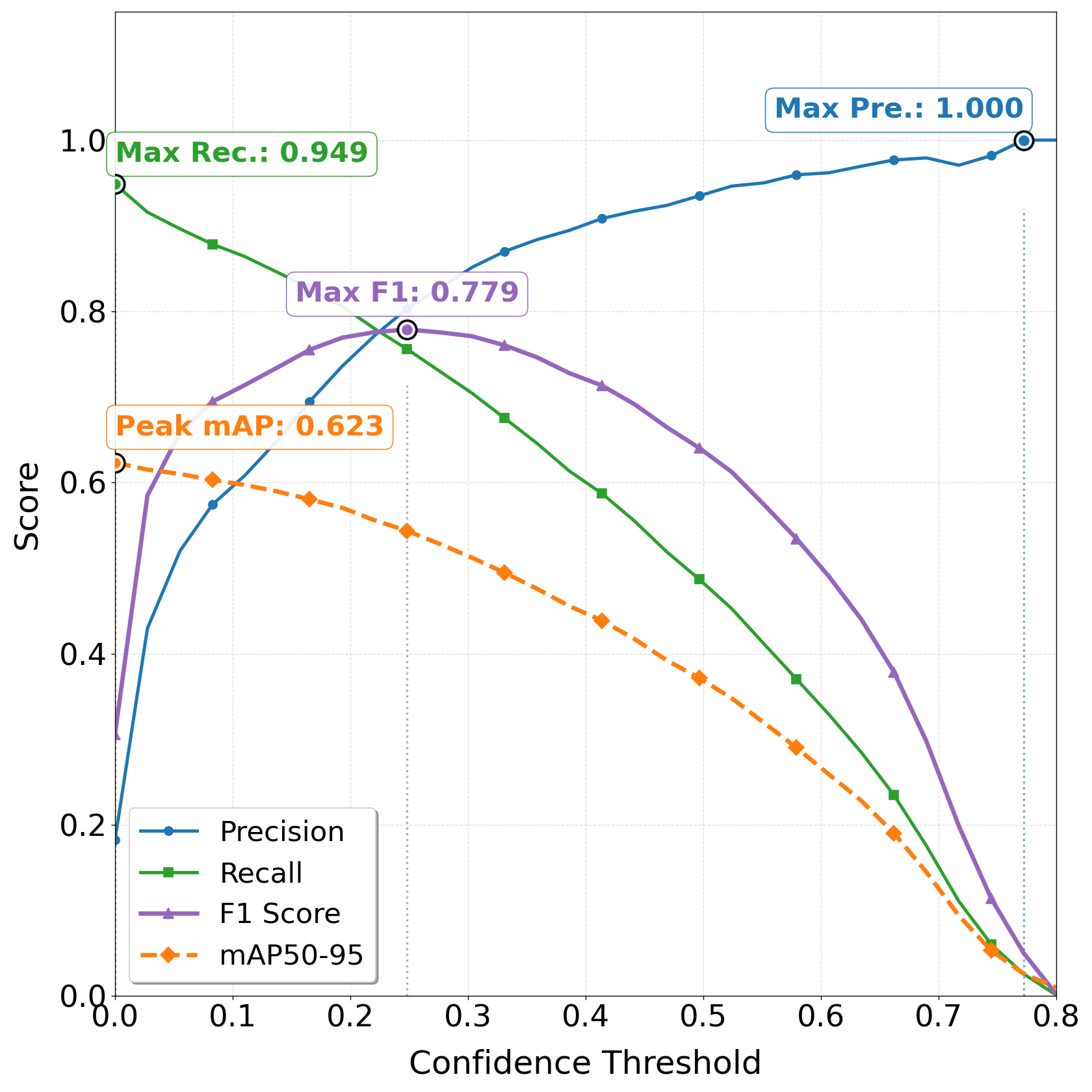
图表分析:
图3展示了最终集成模型在不同置信度阈值下的综合性能指标(召回率、精确率、F1分数和mAP50-95)。
关键观察:
1. 指标权衡:
- 优化mAP50-95需要采用较低的置信度阈值
- 其他单个指标在较高阈值值时达到峰值
- F1分数,平衡了精确率和召回率之间的内在权衡,在更高的置信度水平达到最大值
2. 阈值敏感性:
- 召回率: 随着置信度阈值降低而单调增加
- 精确率: 随着置信度阈值增加而单调增加
- F1分数: 在中等置信度水平达到峰值,反映了最佳权衡点
- mAP50-95: 在低置信度水平达到峰值,因为该指标奖励高召回率
3. 临床应用含义:
- 在临床环境中,可能需要采用比比赛优化更高的置信度阈值
- 适度的置信度阈值增加会产生精确率的显著增益,而mAP仅边际减少
- 这表明模型产生了校准良好的得分,在实际应用中非常有价值
6.3 比赛性能分析
比赛成绩:
- mAP50-95分数:0.5909
- 最终排名:第二名
- 比赛:RIVA宫颈细胞学挑战赛Track B
验证集 vs 比赛集:
- 验证集mAP50-95:0.6232
- 比赛集mAP50-95:0.5909
- 性能下降约5.2%,符合典型的泛化差距
竞争环境分析:
- 在竞争环境中,多个团队采用了不同的方法
- 第二名的成绩表明了方法的竞争力和有效性
- 与第一名可能使用类似的方法,但具体实现细节不同
7. 技术优势与局限性
7.1 系统优势
1. 高召回率:
- YOLO模型达到近99%的召回率
- 对于细胞检测任务,漏掉细胞的代价高于误报
- 在临床筛查中,高灵敏度确保不会错过潜在的诊断重要细胞
2. 多模型集成:
- 结合YOLO和U-Net的优势,实现性能互补
- 集成策略简单有效,基于欧几里得距离融合
- 通过集成显著减少了单个模型的误报率
3. 精细的后处理:
- 三阶段优化管道系统地解决了不同的检测问题
- 空间密度过滤的自适应策略在不同密度下表现良好
- 二进制分类器有效过滤了低置信度的虚假检测
4. 竞赛成绩优异:
- 在RIVA挑战赛中获得第二名
- mAP50-95分数0.5909在竞争环境中表现良好
- 证明了方法的竞争力和实用性
7.2 系统局限性
1. 针对比赛指标优化:
- 最终配置是为了最大化mAP50-95选择的
- 这导致了相对于独立U-Net模型的FP数量增加
- 在实际临床应用中,优先考虑更高精确度与召回率比率的模型可能更适合
2. 计算复杂度:
- 需要训练多个深度学习模型(YOLO + U-Net + 二进制分类器)
- 推理时需要运行所有模型和集成步骤
- 可能不适合资源受限的环境
3. 数据集依赖性:
- 方法性能在很大程度上依赖于RIVA数据集的特定特征
- 在不同的数据集或临床环境中可能需要重新调整参数
- 泛化能力需要进一步验证
4. 标注限制:
- 虽然调整了边界框大小,但基于原始100×100标注
- 仍然受限于原始标注的质量和准确性
- 更精确的标注可能会带来更好的性能
8. 实际应用价值与展望
8.1 实际应用价值
1. 临床筛查支持:
- 为病理学家提供自动细胞检测辅助
- 减少人工显微镜检查的工作量
- 提高筛查效率和一致性
2. 诊断准确性提升:
- 高召回率确保不遗漏异常细胞
- 集成方法平衡了灵敏度和特异度
- 为诊断决策提供可靠的支持
3. 标准化流程:
- 提供标准化的检测方法
- 减少不同病理学家之间的变异性
- 支持大规模筛查项目的一致性
4. 技术转移潜力:
- 方法可以适应其他细胞检测任务
- 集成策略和优化管道具有通用性
- 为医学图像分析提供技术参考
8.2 未来研究方向
1. 精确率优化:
- 在临床环境中,更高精确度与召回率比率可能更优
- 开发针对F1分数而非mAP50-95的优化策略
- 平衡诊断准确性与效率
2. 计算效率改进:
- 开发轻量级模型以降低计算成本
- 优化集成策略以减少推理时间
- 使方法适合移动或边缘计算设备
3. 泛化能力增强:
- 在更多样化和更大的数据集上训练
- 适应不同的染色协议和成像条件
- 验证在不同临床环境中的性能
4. 多任务学习:
- 同时进行细胞检测和分类
- 开发端到端的诊断系统
- 提供更全面的临床支持工具
5. 交互式分析:
- 结合人工专家的反馈
- 开发人机协作系统
- 持续改进模型性能
9. 总结
本文介绍了用于Pap smear图像中Bethesda细胞检测的多模型集成管道,结合了两个YOLOv8检测器和U-Net热图回归模型。该系统为此类型的细胞学检测任务实现了非常高的召回率,反映了这些架构的适用性。
然而,针对mAP50-95优化本质上鼓励以低置信度误报为代价的高召回率。我们观察到,置信度阈值的适度增加会产生精确率的显著增益,而仅边际减少mAP,这表明模型产生了校准良好的得分。这种权衡在临床环境中特别相关,其中精确度直接影响患者管理决策。
主要贡献:
- 提出了YOLO和U-Net的有效集成方法
- 设计了三阶段优化管道提高检测精度
- 在RIVA挑战赛中获得第二名的好成绩
- 为临床应用提供了可行的解决方案
- 代码完全开源,促进研究发展
技术亮点:
- 多模型集成平衡了高召回率和高精确率
- 精细的后处理管道系统性地解决检测问题
- 自适应的置信度策略考虑了细胞密度变化
- 针对比赛指标优化,同时考虑了临床实用性
随着进一步的技术发展和完善,这类自动细胞检测系统将在未来的宫颈筛查和诊断中发挥越来越重要的作用。本文的工作为此发展做出了重要贡献,具有重要的理论意义和实际应用价值。
10. 参考信息
论文来源: arXiv:2604.13939
官方代码库: http://github.com/martinamster/riva-trackb
比赛信息: RIVA宫颈细胞学挑战赛Track B(ISBI 2026)
数据集: RIVA Pap smear数据集
性能指标: mAP50-95(平均精度,IoU阈值0.50-0.95)

AtomGit 是由开放原子开源基金会联合 CSDN 等生态伙伴共同推出的新一代开源与人工智能协作平台。平台坚持“开放、中立、公益”的理念,把代码托管、模型共享、数据集托管、智能体开发体验和算力服务整合在一起,为开发者提供从开发、训练到部署的一站式体验。
更多推荐
 已为社区贡献10条内容
已为社区贡献10条内容






所有评论(0)