Int J Surg 中山大学附属第六医院放射科等团队:基于多维度MRI特征的非侵入性AI模型预测直肠癌三级淋巴结构、免疫治疗反应及预后
01
文献学习

今天分享的文献是由中山大学附属第六医院放射科联合广东省人民医院放射科,吉林大学第一医院等团队于2025年11月在外科领域顶刊《International Journal of Surgery》上发表的研究“A Noninvasive AI Model Based on Multi-dimensional MRI Features for Predicting Tertiary Lymphoid Structures, Immunotherapy Response, and Prognosis in Rectal Cancer”,即基于多维度MRI特征的非侵入性AI模型预测直肠癌三级淋巴结构、免疫治疗反应及预后,该研究构建了一个基于多维度MRI特征的AI模型,用于非侵入性预测直肠癌患者的三级淋巴结构(TLSs)状态,并进一步评估其在免疫治疗反应预测和预后分层中的价值。模型在多个独立队列中表现出良好的泛化能力。
创新点:①首次针对直肠癌提出基于多维MRI的AI模型,实现三级淋巴结构的无创预测。②融合传统影像组学、矩阵降维与肿瘤异质性特征,提升模型表达能力。③采用前瞻性与免疫治疗队列验证,增强模型的泛化性与临床适用性。
临床价值:①提供非侵入性TLSs评估手段,避免活检风险,支持动态监测。②可预测免疫治疗响应与患者预后,辅助个体化治疗决策。③为直肠癌免疫治疗筛选潜在获益人群,提升治疗精准性与安全性。
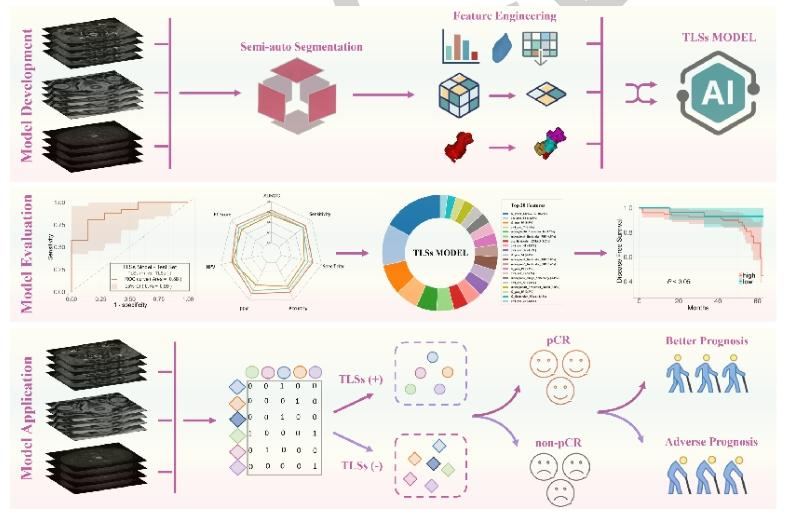
图 1:研究整体工作流程图
队列划分:从857例临床诊断直肠癌患者中,经纳入排除标准筛选出606例,分为开发队列(314例)、验证队列(109例,外部测试集1)、前瞻性队列(89例,外部测试集2)和免疫治疗队列(94例)。
关键环节:依次展示“患者入组→MRI图像采集(T2WI、DWI、CE-T1WI)→ROI分割(U-Net预分割+医生修正)→多维度特征提取(放射组学、降维、异质性)→模型构建(XGBoost算法)→模型验证(内部+外部+前瞻性)→临床价值评估(免疫治疗反应+预后分层)”的全流程。
最终产出:明确模型用于预测TLSs状态、免疫治疗病理完全缓解(pCR)和无病生存期(DFS)的核心目标。
02
研究背景及目的
研究背景
结直肠癌是全球第三大高发恶性肿瘤,其中直肠癌作为其主要亚型,占病例总数的三分之一以上,且具有更高的术后复发率和死亡率,构成严峻的临床挑战。近年来,免疫检查点抑制剂在直肠癌治疗中显示出显著潜力,尤其对于高度微卫星不稳定(MSI-H)患者,部分晚期病例甚至可实现临床完全缓解,并已被纳入NCCN指南推荐。然而,免疫治疗的临床应答率个体差异巨大,仅20%–50%的晚期患者对免疫检查点抑制剂产生积极反应,且部分患者可能面临如肺炎、结肠炎或心肌炎等危及生命的免疫相关不良事件。三级淋巴结构作为肿瘤微环境内免疫细胞的异常聚集结构,在激活T细胞应答、增强抗原呈递和B细胞介导的体液免疫中发挥关键作用,已成为预测包括直肠癌在内的多种癌症免疫治疗疗效与预后的潜在生物标志物。然而,目前对其评估仍依赖侵入性组织病理学检查,不仅伴随并发症风险,且无法实现动态监测,难以在临床常规中推广应用。尽管人工智能技术在医学影像分析中展现出从高维影像特征中挖掘信息的潜力,并在多项癌症研究中用于预测治疗反应与预后,但现有基于影像的TLS评估模型仍存在前瞻性验证缺乏以及在预测免疫治疗应答与预后方面的附加价值证据不足两大局限。因此,开发一种能够无创、动态评估TLS状态并有效预测免疫治疗反应与预后的可靠工具,已成为直肠癌精准医疗中亟待解决的关键问题。
研究目的
本研究旨在开发并验证一种基于多维度MRI特征的人工智能模型,以实现对直肠癌患者三级淋巴结构(TLS)状态的无创性预测,并进一步评估该模型在预测免疫治疗反应和患者预后方面的临床应用价值。具体而言,研究通过整合多序列MRI影像(包括T2加权成像、高b值扩散加权成像和静脉期对比增强T1加权成像),提取三维特征集:包括传统的全肿瘤放射组学特征、基于主成分分析与奇异值分解的矩阵降维抽象特征,以及通过栖息地分析获得的肿瘤亚区异质性特征。利用机器学习算法(如XGBoost)构建TLS分类模型,并在多中心回顾性队列、前瞻性队列以及真实的免疫治疗队列中进行系统验证,以检验其泛化能力。研究进一步探讨TLS评分与病理完全缓解率之间的关联,并通过生存分析明确TLS评分对无病生存期的预测效能。最终,目标是为直肠癌患者的个体化免疫治疗决策、疗效动态监测及预后分层提供一个可靠、非侵入性的影像学生物标志物与临床决策支持工具,克服当前依赖侵入性活检的局限,推动精准免疫治疗的发展。
03
数据和方法
研究数据
总样本量:初始纳入857例临床诊断直肠癌患者,最终606例符合标准纳入分析;
队列划分:
开发队列(314例):用于模型构建,含118例TLSs阴性、196例TLSs阳性患者;
验证队列(109例,外部测试集1):用于初步泛化性验证,含32例TLSs阴性、87例TLSs阳性患者;
前瞻性队列(89例,外部测试集2):用于前瞻性验证,含39例TLSs阴性、51例TLSs阳性患者;
免疫治疗队列(94例):用于免疫治疗反应预测验证,含51例pCR患者、43例非pCR患者;
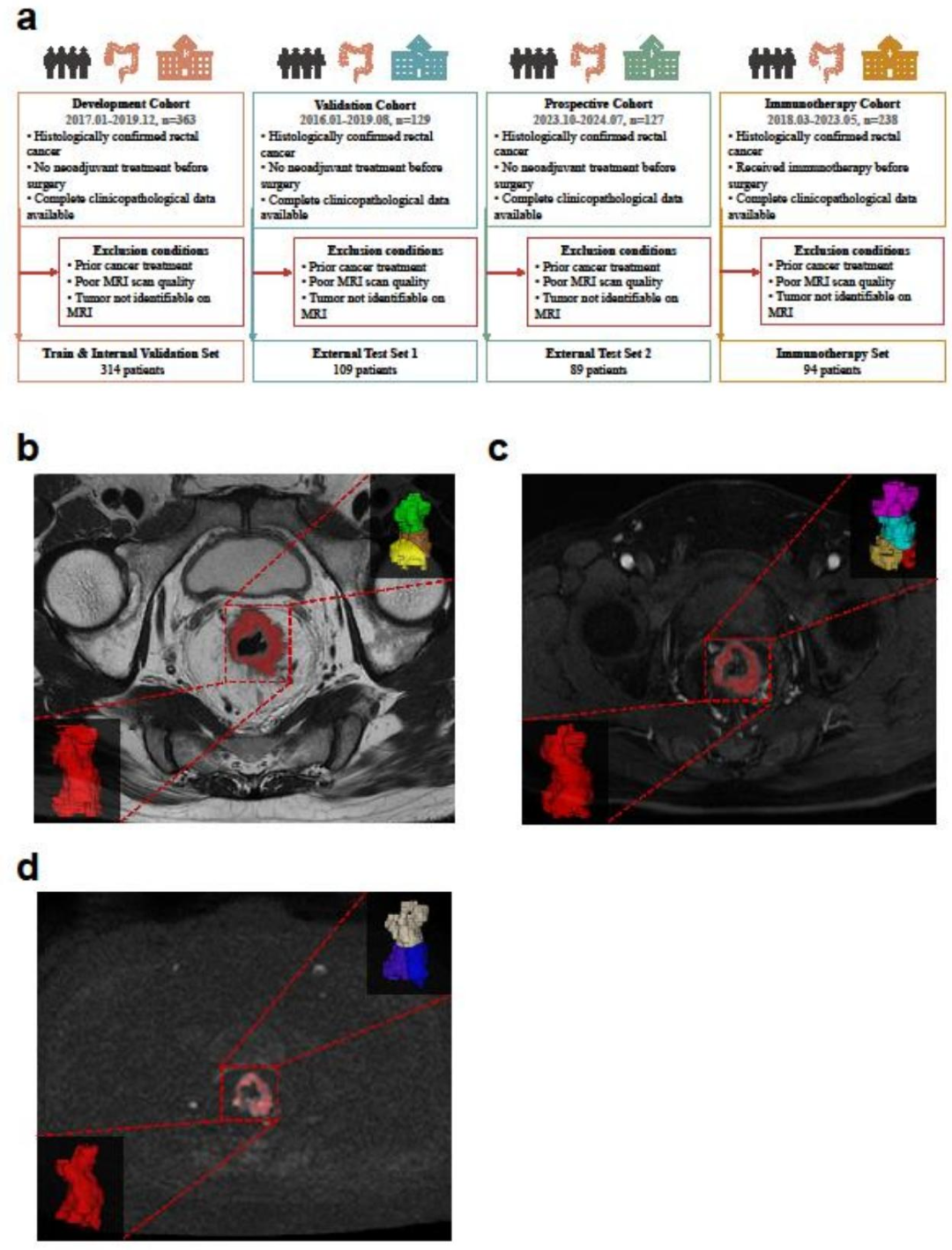
图 2:患者纳入排除标准及MRI分割示意图
技术方法
(1)图像采集与分割
图像类型:所有患者治疗前接受直肠MRI扫描,包括轴位T2加权成像(T2WI)、高b值(b≥800)扩散加权成像(DWI)、静脉期增强T1加权成像(CE-T1WI);
分割方法:采用U-Net算法预分割(基于既往标注数据训练),由10年经验放射科医生使用ITK-SNAP软件手动修正,最终获得3D肿瘤感兴趣区(ROI)。
(2)TLSs病理评估
评估者:2名具有15年以上结直肠癌病理经验的高级胃肠病理科医生;
评估方式:双盲法(不了解临床和影像学信息),按既定标准分类TLSs成熟阶段(淋巴细胞聚集物、初级滤泡、次级滤泡),以存在成熟次级滤泡(FolII)定义为TLSs阳性;
一致性检验:随机抽取50例样本进行观察者间一致性分析,concordance达88%,一致性高。
(3)多维度特征提取
放射组学特征(321个):从T2WI、DWI、CE-T1WI序列提取纹理、形态学、统计特征,每个序列107个,使用PyRadiomics计算;
降维特征(300个):基于T2WI、DWI、CE-T1WI序列,通过主成分分析(PCA)和奇异值分解(SVD)获取数学抽象特征;
肿瘤异质性特征(1070个):对融合后的3种序列图像进行超体素聚类,生成10个亚区域,提取亚区域异质性特征。
(4)模型构建与验证
数据划分:开发队列按4:1比例分为训练集(251例)和内部验证集(63例);
算法比较:评估AdaBoost、LightGBM、XGBoost三种机器学习算法性能;
特征组合比较:验证三种特征组合(单一放射组学、放射组学+降维特征、三者联合)的模型效能;
超参数优化:采用网格搜索在训练集上优化模型超参数;
模型评估指标:AUROC、F1分数、准确率、灵敏度、特异度、阳性预测值(PPV)、阴性预测值(NPV),结合校准曲线评估预测概率与实际结果的一致性。
(5)模型解释与统计分析
模型解释:采用Shapley Additive exPlanations(SHAP)分析,识别影响模型决策的关键特征;
统计方法:描述性统计总结基线特征,Kaplan-Meier法分析生存曲线,log-rank检验比较组间预后差异,P<0.05为差异有统计学意义。
04
实验结果
(1)模型性能最优组合
-
算法选择:XGBoost算法性能优于AdaBoost和LightGBM,在各队列中AUROC更高(无统计学显著差异,但综合7项指标最优);
-
特征组合选择:三者联合特征模型(放射组学+降维+异质性)性能最优,外部测试集中ROC检验显示差异有统计学意义;
-
模型整体效能:内部验证集AUROC=0.88(0.80-0.97),外部测试集1 AUROC=0.81(0.70-0.91),外部测试集2 AUROC=0.84(0.76-0.92),校准曲线均接近45°对角线,校准性能良好(详细见表2)。
(2)关键特征识别
-
前20个关键特征涵盖三种维度和三种MRI序列,其中subregion3_firstorder_MeanAbsoluteDeviation、subregion1_firstorder_Kurtosis、cet1wi_pca_62、t2wi_glcm_MCC贡献最大(各占前20特征总影响的6%以上);
-
前3个特征高值与TLSs阳性呈正相关,t2wi_glcm_MCC高值与TLSs阳性呈负相关。
(3)免疫治疗反应预测
-
免疫治疗队列中,pCR组与非pCR组的TLSs评分差异有统计学意义(P<0.05);
-
模型预测pCR的AUROC=0.74(0.64-0.84),纯免疫治疗组AUROC=0.77(0.56-0.97),免疫治疗联合化疗组AUROC=0.74(0.62-0.86)。
(4)预后分层能力
-
Kaplan-Meier分析显示,高TLSs评分组DFS显著优于低评分组(log-rank P<0.05);
-
内部验证集HR=2.48(1.11-5.54),外部测试集1 HR=3.07(1.41-6.68),预后分层效能稳定。
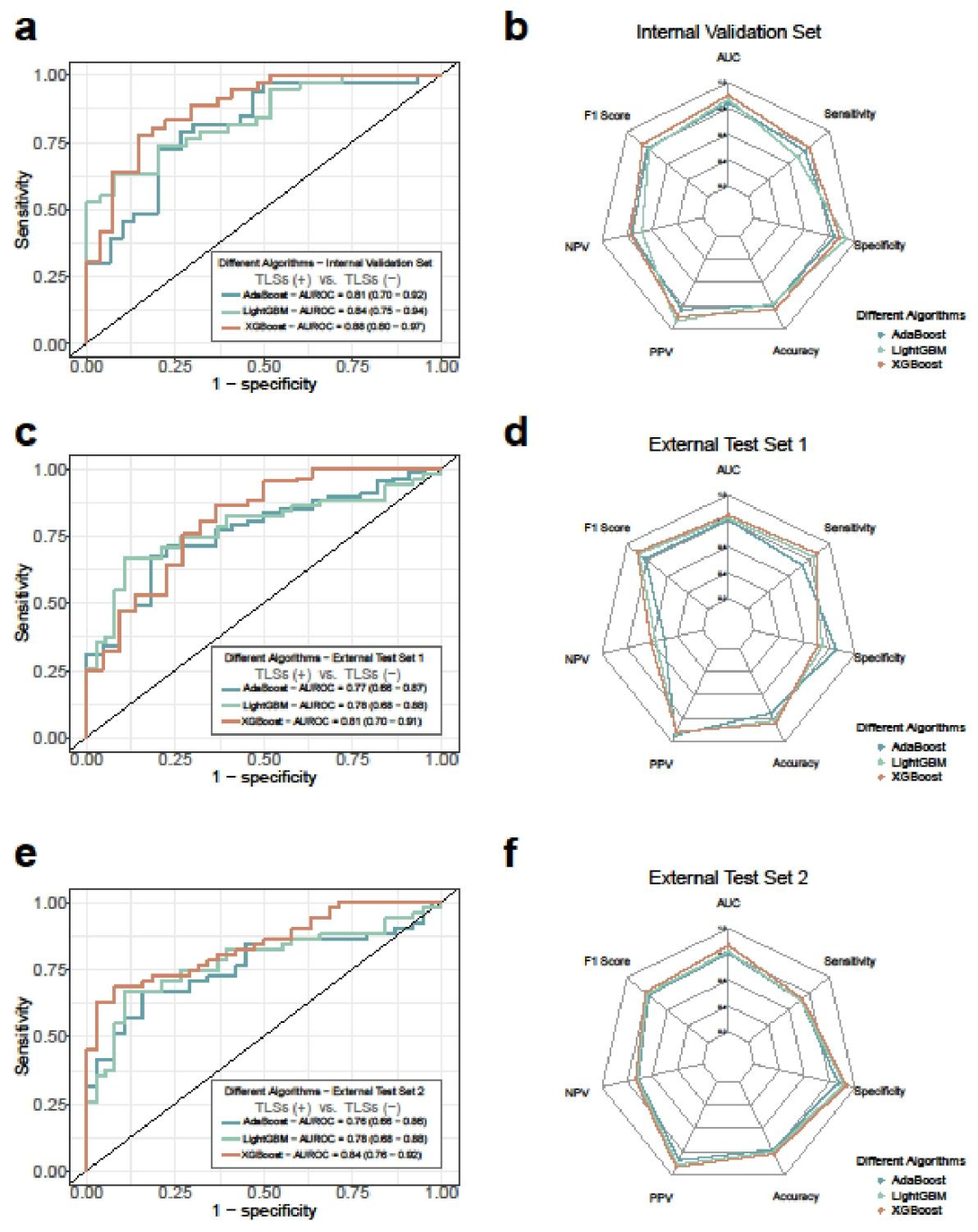
图 3:不同机器学习算法的预测性能对比图
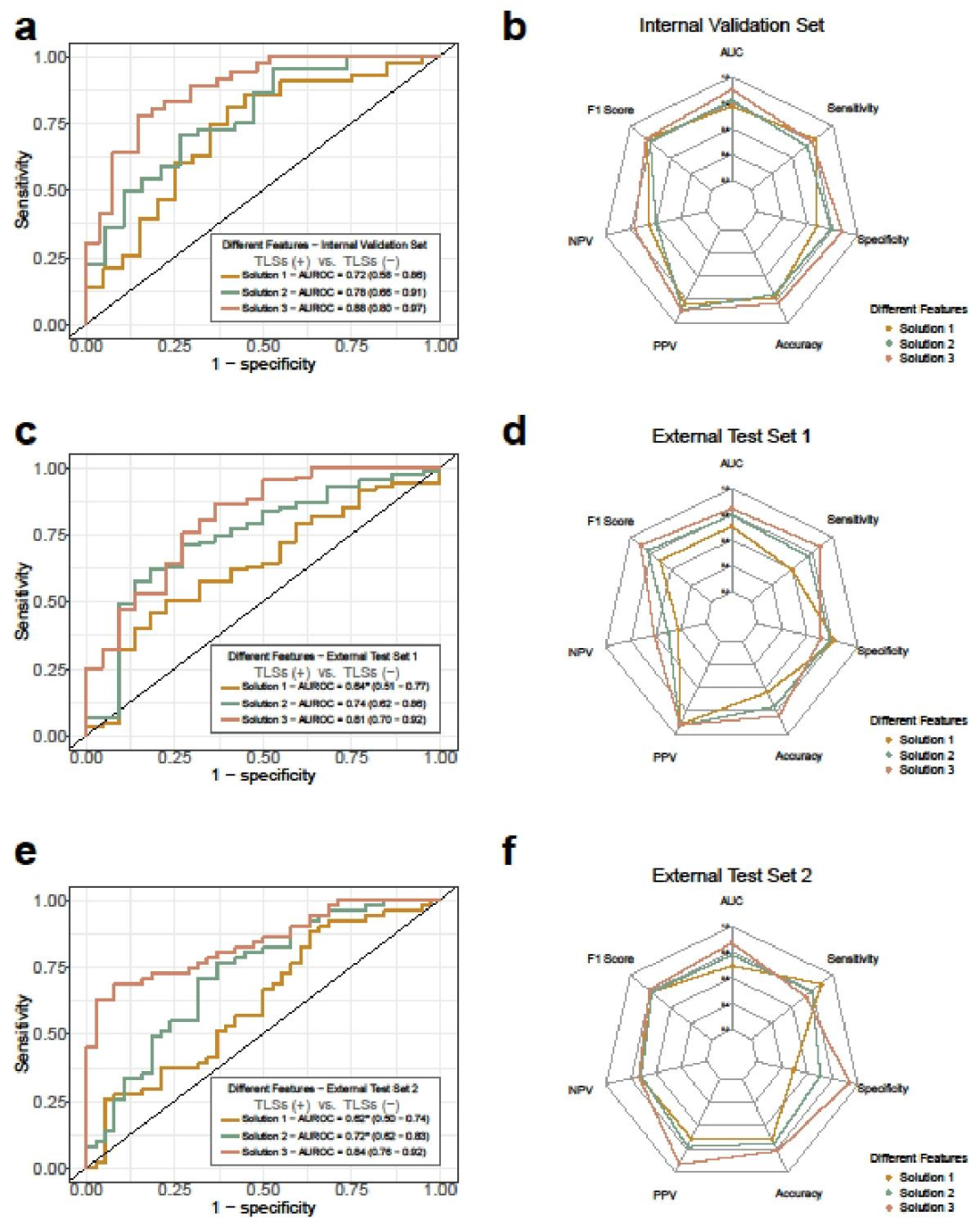
图 4:不同特征提取策略的预测性能对比图
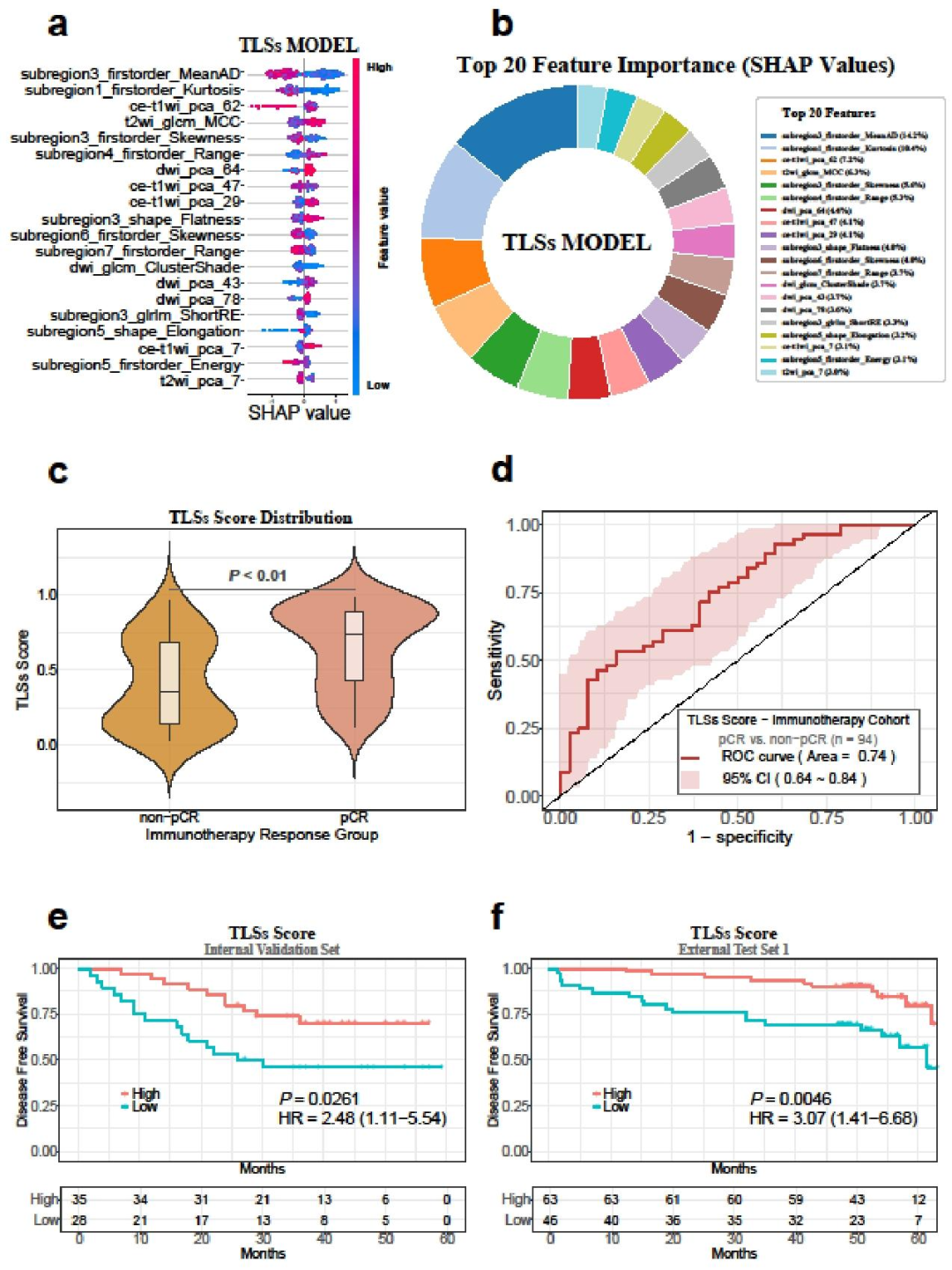
图 5:模型可解释性及临床附加价值图
05
研究结论
本研究成功构建并验证了一个基于多维度MRI特征的非侵入性人工智能模型,用于预测直肠癌患者的三级淋巴结构状态、免疫治疗反应及预后。该模型整合了传统影像组学特征、基于矩阵的降维特征及肿瘤异质性特征,采用XGBoost算法,在内部验证集和外部测试集中均表现出优异且稳定的判别性能,AUROC分别达到0.88、0.81和0.84。更重要的是,模型提取的TLSs评分在免疫治疗队列中显示出显著的预测价值,能够有效区分病理完全缓解与非缓解患者,其AUROC为0.74,并在不同治疗亚组中保持稳健。此外,该评分还展现出明确的预后分层能力,高TLSs评分组患者具有显著更优的无病生存期。研究进一步通过SHAP分析提升了模型的可解释性,明确了影响预测的关键影像特征。综上,该模型不仅为直肠癌TLSs的无创评估提供了可靠工具,更在预测免疫治疗反应和患者预后方面具有重要的临床转化潜力,有望支持个体化治疗决策与动态疗效监测。
参考文献:Yang H, Wong C, Liang W, Xie P, Chen G, Ma D, Liu W, Xie X, Liu Z, Zhang H, Fu Y, Meng X. A noninvasive AI model based on multi-dimensional MRI features for predicting tertiary lymphoid structures, immunotherapy response, and prognosis in rectal cancer. Int J Surg. 2025 Nov 19. doi: 10.1097/JS9.0000000000003845.

AtomGit 是由开放原子开源基金会联合 CSDN 等生态伙伴共同推出的新一代开源与人工智能协作平台。平台坚持“开放、中立、公益”的理念,把代码托管、模型共享、数据集托管、智能体开发体验和算力服务整合在一起,为开发者提供从开发、训练到部署的一站式体验。
更多推荐
 已为社区贡献76条内容
已为社区贡献76条内容






所有评论(0)