致谢文章+1,中科院1区,scRNA-seq揭示麻黄-甘草配对治疗呼吸系统症状和多(I:C)诱发肺炎模型机制
一、写在前面
来自中国药科大学的研究团队(博士后张帆和博士研究生马亚洁为本文共一作者,余伯阳教授和张媛媛副教授为本文共同通讯作者)通过scRNA-seq、网络药理学结合实验验证,揭示了麻黄-甘草药对(麻甘药对,EGP)在小鼠呼吸系统症状和多(I:C)诱发肺炎模型中的互补作用与协同作用。这一作品发表于《Phytomedicine》 (中科院1区,IF=8.3)。最最最重要的是,这是一篇致谢Biomamba生信基地的论文!更多致谢请见:致谢合集

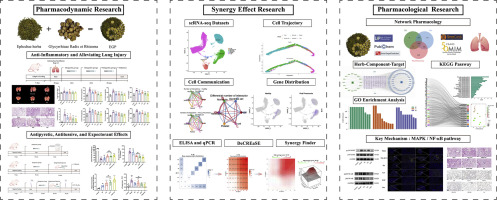
Zhang F, Ma Y J, Mei J, et al. Complementary roles and synergy of the Ephedra-Glycyrrhiza herb pair across murine models of respiratory symptoms and poly(I:C)-induced pneumonia[J]. Phytomedicine, 2026, 151: 157795. https://doi.org/10.1016/j.phymed.2026.157795 .
这里也预祝我们的粉丝们早日命中心仪的期刊,若是大家觉得我平时分享的代码或生信教程有那么点好用,可以在文章里以这种格式致谢Biomamba,希望咱们这个系列也能更新个百八十篇:
Since Biomamba and his wechat public account team produce bioinformatics tutorials elaborately and share code with annotation, we thank Biomamba for their guidance in bioinformatics and data analysis for the current study.我们特此开启“一作面对面” 活动,邀请各位第一作者分享经验、传经送宝,也借此沾沾喜运,祝愿大家文章多多、成果累累!
直播时间:2026年3月29日16:00准时开播
直播预约:预约起来,第一时间锁定直播
B站
https://www.bilibili.com/opus/1183556028917088264?
如果需要单细胞数据分析教学、生信热点全文复现、自测数据个性化分析辅导、常态化实验学习,欢迎联系客服微信[Biomamba_zhushou]。
二、背景介绍
病毒性肺炎是一种快速进展的下呼吸道感染。从严重急性呼吸综合征冠状病毒(SARS-CoV)、2009年H1N1流感大流行,到中东呼吸综合征冠状病毒(MERS-CoV)和SARS-CoV-2,连续爆发的呼吸道病毒凸显了除了支持性护理之外,对治疗病毒性肺炎药物的持续需求。在病理生理层面,病毒侵入远端气道激活先天免疫传感器和趋化因子程序,招募单核细胞/巨噬细胞和中性粒细胞,并扩增细胞因子如白介素-1β(IL-1β)、白介素-6(IL-6)和肿瘤坏死因子-α(TNF-α)。由此产生的上皮和内皮损伤破坏肺泡毛细血管屏障,临床表现为发烧、咳嗽和粘液过度分泌。麻黄与甘草作为中医药治疗病毒性肺炎中使用频率极高的经典药对,长期用于发热、咳嗽、痰多、喘促等症状。但二者合用是否优于单味药,以及各自承担什么功能角色等问题,一直缺乏系统、定量的实验验证。
为解答这些问题,作者将实验模型映射到与呼吸道感染相关症状和肺损伤:用于气道炎症和肺损伤的聚肌苷酸聚胞苷酸(Poly(I:C))气管灌注;腹腔内脂多糖(LPS)诱导发热;吸入氨气以诱发咳嗽;以及注射酚红用于指示气道分泌物。为探究麻黄-甘草药对(麻甘药对)在其中的的互补作用与协同作用,作者比较了等剂量下麻黄、甘草及其1:1组合后(麻甘药对)的药物效应,并基于Bliss独立性假设量化麻黄-甘草在各模型指标中的相互作用。为探索机制相关,作者将单细胞RNA测序(scRNA-seq)、网络药理学与实验验证相结合,发现麻黄-甘草合用可同时削弱p38 MAPK和NF-κB两条关键炎症信号通路的活化水平。与之相呼应的是,在体内使用p38抑制剂与NF-κB抑制剂联合干预时,对肺损伤指标和系统性炎症因子的改善效果也明显优于单一通路抑制。这一结果提示,双通路的协同调控可能正是该药对产生抗炎协同效应的重要基础。最后,作者评估了小鼠7天的短期口服耐受性。
结果表明,在多种模型中,麻甘药对在多数关键指标上均优于单味药。其中,甘草主要发挥止咳/祛痰作用,麻黄则主要起解热作用。两味药均具有一定抗炎作用,值得注意的是,这种效果并非简单相加。在多个模型和检测体系中,麻甘药对对IL-1β的抑制呈现出显著的协同效应。在治疗剂量下,小鼠口服7天未见明显毒性。
三、生信结果
1、单细胞转录组学揭示病毒性肺炎患者单核细胞中IL-1β表达增强
作者分析了健康受试者和病毒性肺炎患者的单细胞数据集(GSE166992、GSE243629)。共包含45,207个健康细胞;32,647个病毒性肺炎细胞,Harmony整合和UMAP降维后确定了六个主要簇——B细胞、树突状细胞、单核细胞、中性粒细胞、血小板和T细胞(图3A和3B,图S3)。轨迹推断表明存在群依赖状态转变,尤其是在单核细胞区室内(图3C)。CellChat显示病毒性肺炎的整体通讯强度增强,单核细胞相互作用——尤其是单核细胞-中性粒细胞相互作用——最高(图3D-H)。配体-受体分析进一步确认IL1B–IL1R2信号作为与单核细胞相关的显著相互作用(图3I)。特征图显示病毒性肺炎患者单核细胞中IL-1β转录本丰度较高(图3J),支持单核细胞作为主要IL-1β产细胞区室,并优先将IL-1β作为后续麻甘药对药效学评估的疾病相关炎症终点。更多单细胞教程可见:保姆级单细胞&空转教学|生信全程班一览

图3
2、网络药理揭示EGP与病毒-肺炎通路关联
麻黄和甘草的成分和目标由TCMSP、PubChem和SwissTargetPrediction筛选而来(麻黄:23个成分/445个靶点;甘草:92个成分/988个靶点)。OMIM和GeneCards中的“病毒性肺炎”查询结果显示了5412个疾病靶点。交汇点产生了569个共同靶点(图5A),Cytoscape成分-疾病-靶点网络识别出104个核心靶点(图5B)。GO显著富集到了995个通路(BP 759,CC 90,MF 146;图5C)。KEGG富集产生了173条通路,其中反复富集到MAPK和NF-κB信号(图5D-E),而这两个通路已知与IL-1β的生成相关。总之,网络药理学结果指向MAPK和NF-κB信号通路可能为麻甘药对抗炎表型背后的机制。结合实验验证,作者发现麻甘药对可同时削弱p38 MAPK和NF-κB的磷酸化水平。与之相呼应的是,在体内使用p38抑制剂与NF-κB抑制剂联合干预时,对肺损伤指标和系统性炎症因子的改善效果也明显优于单一通路抑制。

图 5
四、最后聊聊
当然,生信只占据了文章的一部分(图3、图5),作者利用HPLC指纹、多种疾病模型药效评估,结合H&E染色、免疫荧光、免疫组化、细胞实验、细胞因子检测、RT-PCR等方法界定了麻黄与甘草在呼吸道症状干预中的分工与协作,证明了以下主要科学结论:
1、在多个小鼠模型中,麻甘药对在大多数疗效终点上优于任一单一草药。
2、麻黄具有抗热作用,甘草具有祛痰和祛痰作用,这两种草药都能减轻炎症反应。
3、麻甘药对主要在白介素-1β(IL-1β)上显示出药理学上的协同效应。
4、细胞、组织和抑制剂的研究一致表明,p38 MAPK和NF-κB的同时抑制是EGP协同抑制IL-1β的基础。
5、一项为期 7 天的小鼠口服给药研究显示,基于体重、血清生化指标、脏器系数及组织病理学检测结果,麻甘药对未表现出明显毒性。
最后,也很感谢大家的致谢!你们的鼓励是我们创做的最大动力:欢迎致谢

AtomGit 是由开放原子开源基金会联合 CSDN 等生态伙伴共同推出的新一代开源与人工智能协作平台。平台坚持“开放、中立、公益”的理念,把代码托管、模型共享、数据集托管、智能体开发体验和算力服务整合在一起,为开发者提供从开发、训练到部署的一站式体验。
更多推荐
 已为社区贡献6条内容
已为社区贡献6条内容






所有评论(0)