ADC肺毒性如何评估?人源肺泡体外模型解析(含实验数据)【曼博生物官方代理Epithelix人原代肺细胞】
一、研究背景:ADC为何面临肺毒性风险?
抗体药物偶联物(ADC)是一类快速发展的靶向抗癌药物,由抗体、连接子及细胞毒载荷组成。
其作用机制为:
- 与靶抗原结合
- 被肿瘤细胞内吞
- 释放毒性载荷发挥抗肿瘤作用
但在实际应用中,载荷可能发生扩散,从而对正常组织产生“旁观者效应”。
👉 典型案例:
T-DXd(曲妥珠单抗德鲁替康)在临床中可诱导间质性肺病(ILD),发生率可达约15%。
👉 问题关键:
传统动物模型往往难以准确预测此类毒性。
二、人源肺泡体外模型的构建思路
为更接近人体生理环境,研究人员构建了一种体外多组织共培养模型:
- 人源肺泡模型(气液界面培养)
- HER2阳性肿瘤球状体
- 微囊包封技术实现“类循环系统”
该体系实现了:
👉 肺组织 + 肿瘤组织的体外联动
三、实验体系结构
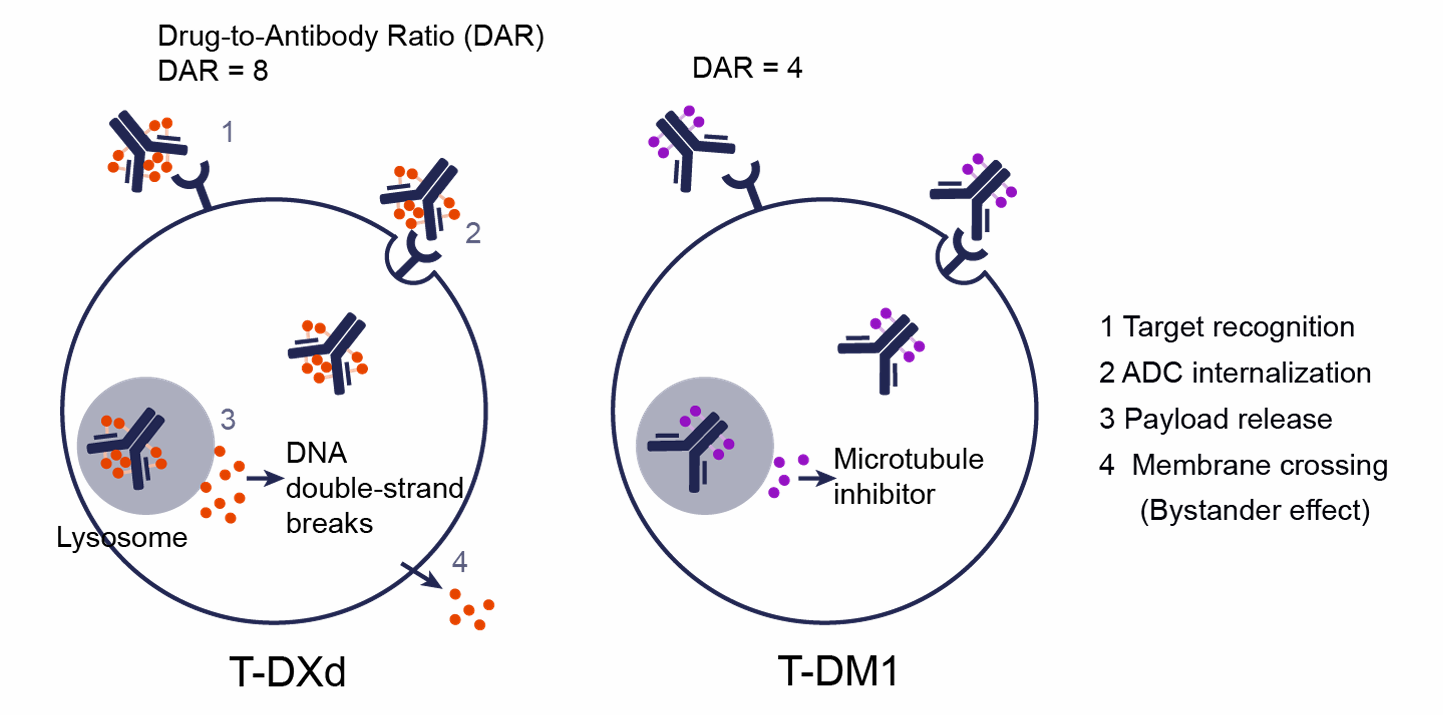
图1:T-DXd与T-DM1作用机制
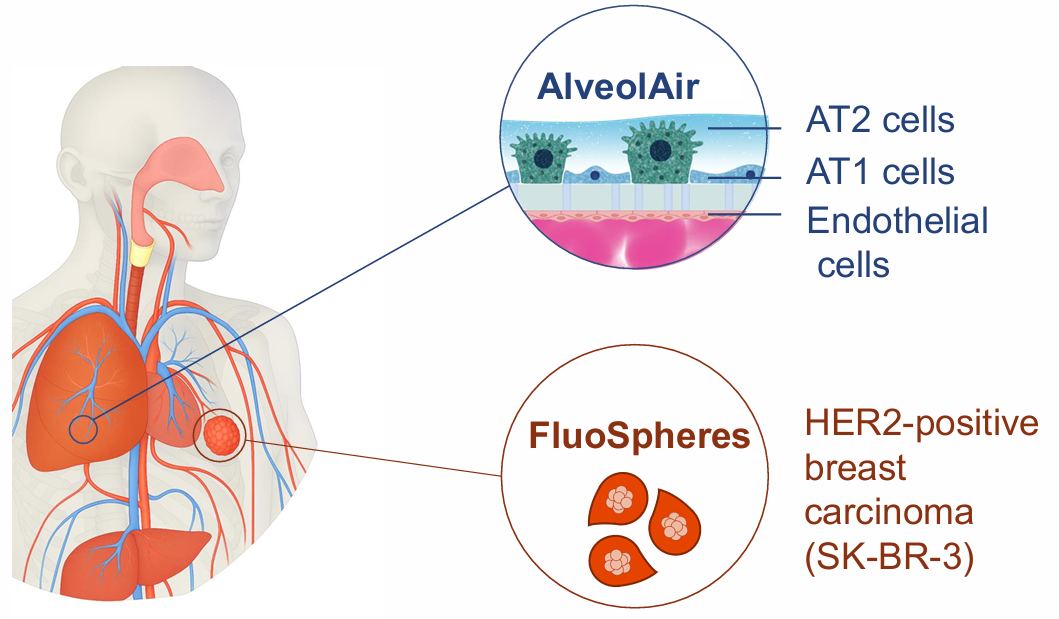
图2:肺泡模型与肿瘤球共培养系统
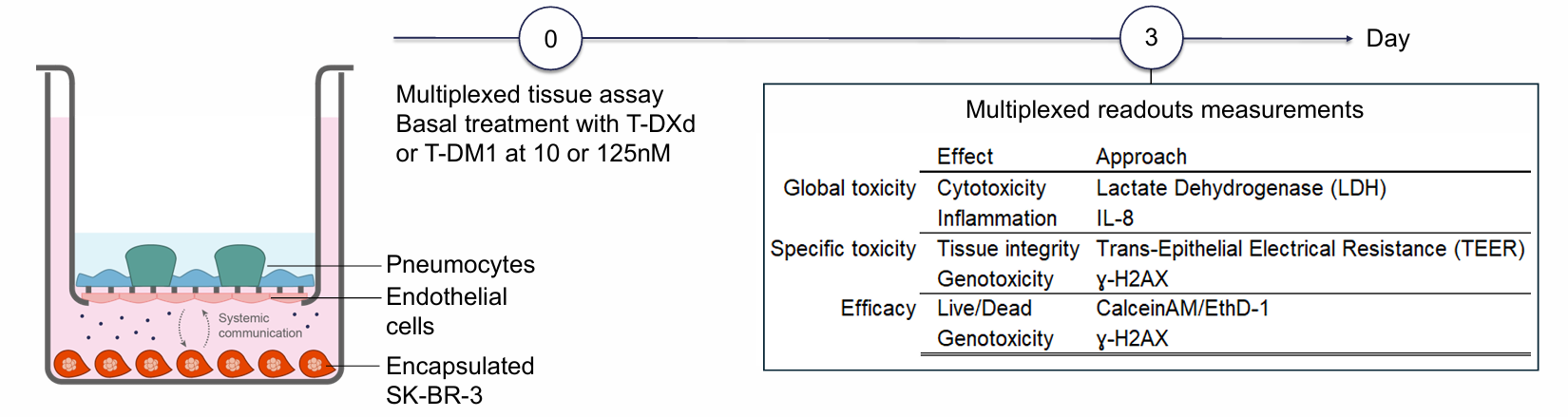
图3:实验干预与检测指标
检测维度包括:
- 整体毒性(细胞活性)
- 炎症反应(IL-8)
- 屏障功能(TEER)
- DNA损伤(γ-H2AX)
四、关键实验结果解析
1. 整体细胞毒性
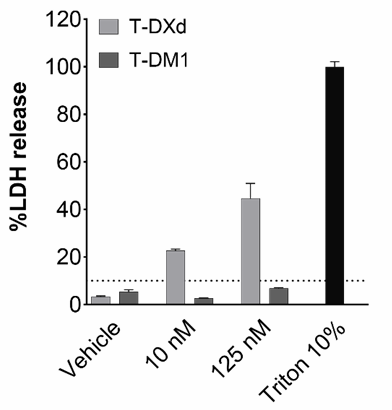
结果显示:
- T-DM1基本无肺毒性
- T-DXd呈现明显剂量依赖毒性
2. 炎症反应
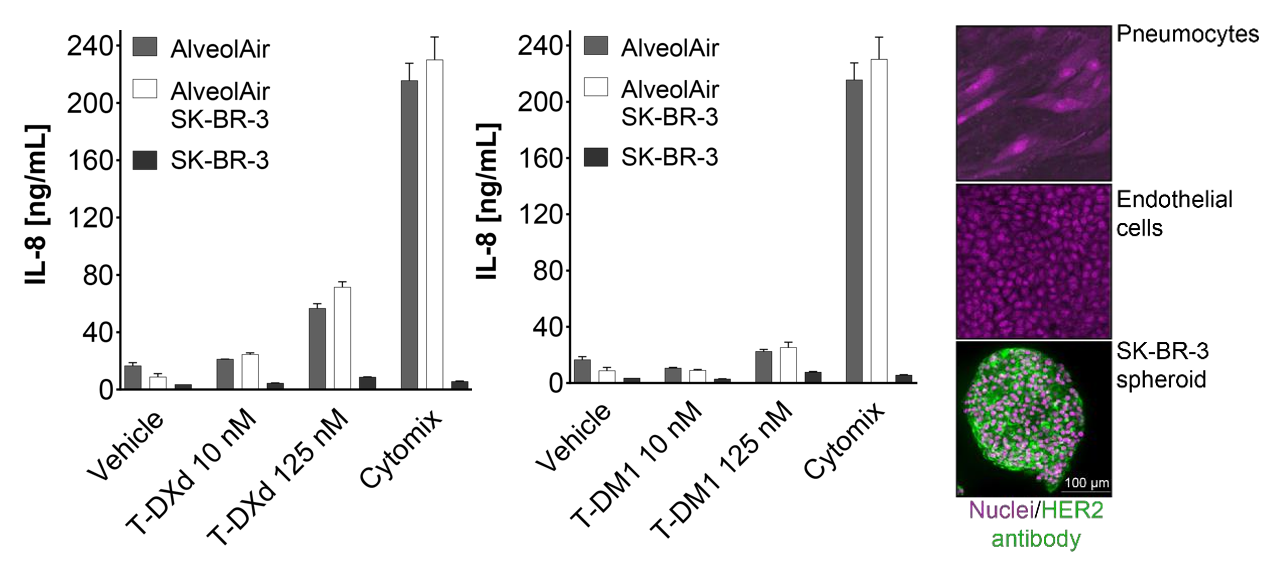
T-DXd可诱导IL-8释放,即使无肿瘤存在仍然发生。
👉 说明:存在直接肺毒性机制
3. 组织完整性损伤
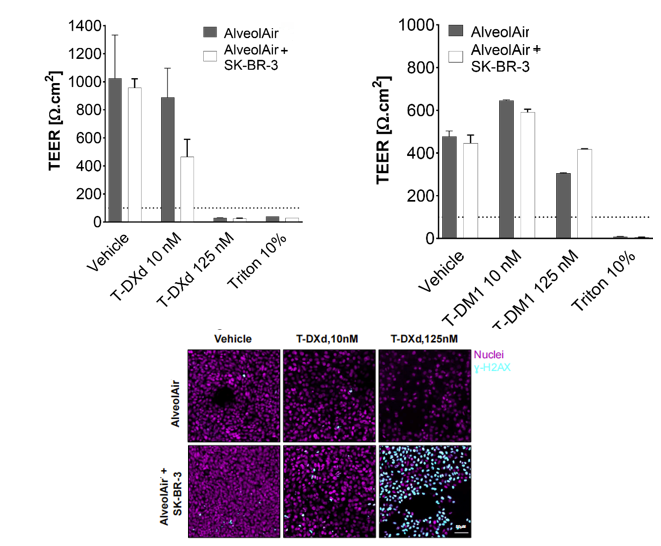
观察到:
- 肺泡结构受损
- DNA双链断裂增加
👉 且在共培养条件下损伤加剧
4. 抗肿瘤效果
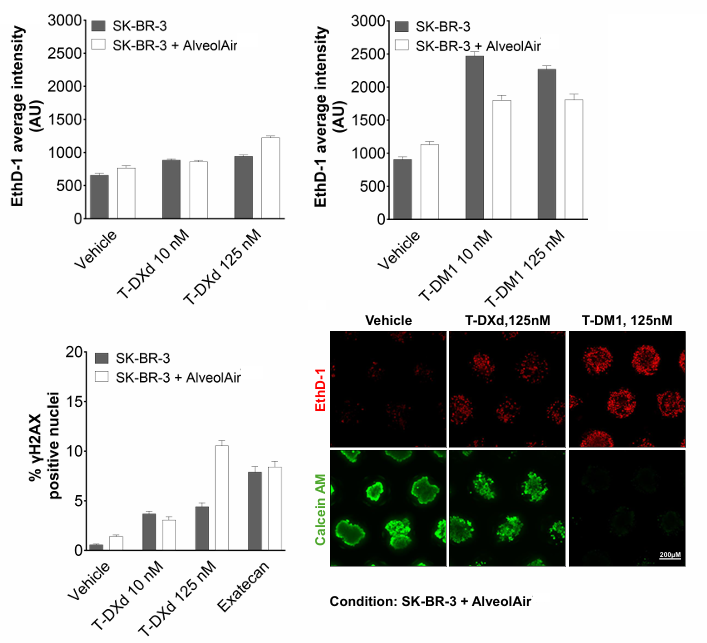
结果对比:
- T-DM1:更强细胞毒性
- T-DXd:主要表现为增殖抑制
👉 有趣现象:
肺泡模型存在时,T-DXd抗癌效果增强
五、机制总结(核心发现)
该模型揭示了三类关键机制:
1. 旁观者效应
肿瘤释放的毒性分子影响肺组织
2. 直接毒性
ADC可直接作用肺细胞引发炎症
3. 疗效差异
不同ADC在“抑制 vs 杀伤”机制上存在区别
六、FAQ(高频问题)
Q1:为什么动物模型预测不到肺毒性?
因为动物肺结构与人类差异较大,无法模拟真实微环境。
Q2:该模型核心优势是什么?
可同时评估:
- 抗癌效果
- 器官毒性
Q3:适用于哪些研究?
- ADC药物开发
- 毒理评估
- 器官芯片研究
七、总结
该类人源体外模型提供了一种更接近人体真实反应的研究工具:
- 能识别传统模型无法捕捉的毒性
- 可实现“疗效+毒性”同步评估
- 为ADC开发提供更可靠依据
参考资料
[1] Ferreira Lopes et al., 2025
[2] Nature Communications, 2025
[3] Toxicology and Applied Pharmacology, 2024
(延伸阅读,可参考相关技术资料)
https://www.mine-bio.com/EpitheliX-Sarl/?utm_source=csdn&utm_medium=referral&utm_campaign=epithelix_article

AtomGit 是由开放原子开源基金会联合 CSDN 等生态伙伴共同推出的新一代开源与人工智能协作平台。平台坚持“开放、中立、公益”的理念,把代码托管、模型共享、数据集托管、智能体开发体验和算力服务整合在一起,为开发者提供从开发、训练到部署的一站式体验。
更多推荐
 已为社区贡献15条内容
已为社区贡献15条内容






所有评论(0)