THP-1分化成巨噬细胞诱导攻略
概述
巨噬细胞是免疫系统中的重要组成部分,在保护机体免受感染和维持组织平衡方面发挥着关键作用。为了研究巨噬细胞的功能和机制,科学家们创造了一种不需要从患者或动物采集组织的模型,即THP-1细胞。THP-1细胞系最初来自一位急性单核细胞白血病患者的血液,属于悬浮细胞,有分化为多种巨噬细胞的能力,成为巨噬细胞分化的不二之选。THP-1细胞可通过化学物质处理、细胞因子刺激或共培养等方法,诱导其分化为具有巨噬细胞特性的细胞群。
机理
细胞因子刺激是一种常见的THP-1细胞诱导分化方法。IL-4和IL-13等细胞因子能够促使THP-1细胞分化为巨噬细胞,并启动特定的信号通路,进而调控细胞功能。这种方法可以模拟体内的免疫调节过程,并提供一种便捷的方式来研究巨噬细胞在炎症反应、免疫调节和抗肿瘤等方面的功能。
巨噬细胞被分为两种主要类型:M1型巨噬细胞和M2型巨噬细胞。THP-1细胞通常用佛波酯(PMA)诱导分化为巨噬细胞,然后在PMA仍然存在的情况下:
加入脂多糖(LPS)(诱导浓度:100ng/mL)、IFN-γ(诱导浓度:20ng/mL)培养48h,诱导其向M1极化;
加入IL-4(诱导浓度:20ng/mL)、IL-13(诱导浓度:20ng/mL)培养48h,诱导其向M2极化;
最后,在无刺激物和无PMA的情况下,用无血清RPMI-1640基础培养基重悬细胞,可保持72h。
诱导步骤
THP-1诱导分化成巨噬细胞实验步骤:
(1)THP-1细胞的培养:
THP-1(人单核细胞白血病细胞)细胞基本信息
|
形态 |
淋巴细胞样 |
|
生长特性 |
悬浮 |
|
营养体系 |
89% RPMI1640基础培养基+10%胎牛血清优级+1%双抗+0.1%β-巯基乙醇溶液 |
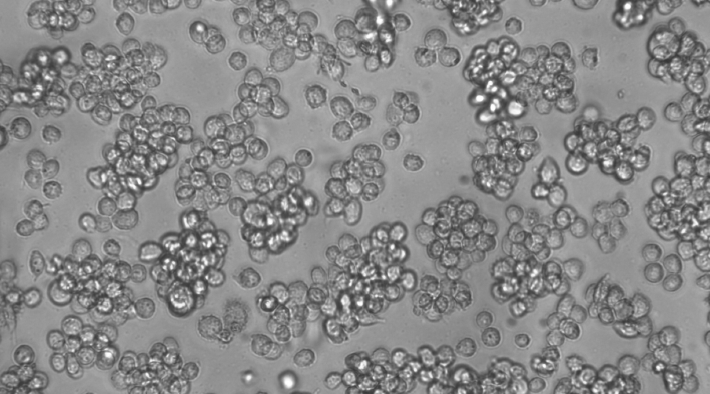
THP-1(人单核细胞白血病细胞)
(2)诱导培养基的配置:向1640完全培养基(含胎牛血清)里加入PMA(诱导浓度:100ng/mL)制成诱导培养基;
(3)接种细胞:收集THP-1细胞并进行计数,用诱导培养基重悬细胞沉淀调整细胞密度为5*10^5/mL,将细胞种入六孔板,每孔加入细胞悬液2mL;
(4)诱导培养:48h后,显微镜下观察巨噬细胞构建成功;
(5)诱导成功的标志:单核细胞THP-1用PMA诱导后,由悬浮式生长变成贴壁生长,由圆形变成不规则形态,体积进一步增大,细胞浆疏松,细胞核增大明显,可见大量明显细胞器,胞膜周围可见少量突起。
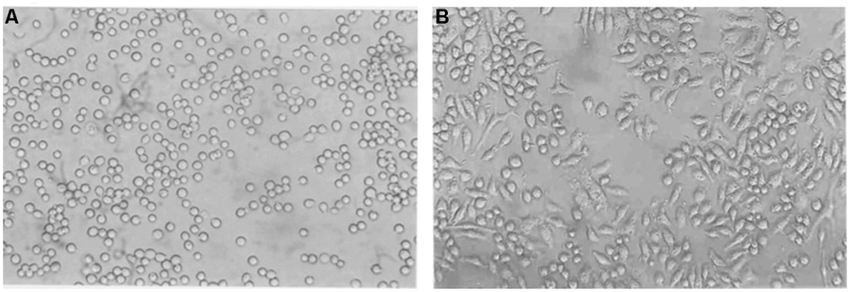
PMA诱导THP-1细胞培养的相差显微照片
用PMA孵育THP-1细胞48h,显示THP-1(40X)在(A)诱导前(B)诱导后的形态学变化。它们的形态由圆形变为细长和扁平。
巨噬细胞进一步诱导成M1型实验步骤:
(1)诱导培养基的配置:向1640完全培养基(含胎牛血清)里加入PMA(诱导浓度:100ng/mL)、脂多糖(LPS)(诱导浓度:100ng/mL)、IFN-γ(诱导浓度:20ng/mL),制成诱导培养基;
(2)诱导培养:将已经诱导成的巨噬细胞上清弃除,加入诱导培养基(6孔板,每孔2mL)培养48h,诱导其向M1极化。48h后,显微镜下观察M1细胞是否构建成功;
(3)最后,在无刺激物和无PMA的情况下,用无血清RPMI-1640基础培养基重悬细胞,可保持72h。
巨噬细胞进一步诱导成M2型实验步骤:
(1)诱导培养基的配置:向1640完全培养基(含胎牛血清)里加入PMA(诱导浓度:100ng/mL)、加入IL-4(诱导浓度:20ng/mL)、IL-13(诱导浓度:20ng/mL)制成诱导培养基;
(2)诱导培养:将已经诱导成的巨噬细胞上清弃除,加入诱导培养基(6孔板,每孔2mL)培养48h,诱导其向M2极化。48h后,显微镜下观察M2细胞是否构建成功;
(3)最后,在无刺激物和无PMA的情况下,用无血清RPMI-1640基础培养基重悬细胞,可保持72h。
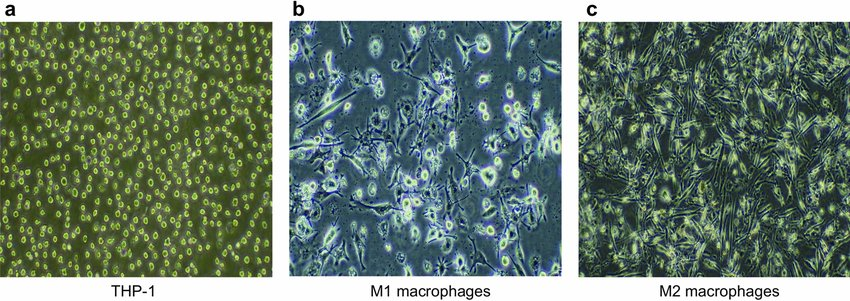
THP-1极化进入M1和M2巨噬细胞图
M1型形态多样,伪足较多,分叉明显,M2型形态均一,多呈长条型,分叉不明显。
M1和M2型鉴定
上述形态是初步的鉴别方法,更准确的可以通过流式细胞术一般是通过一些巨噬细胞标志物进行的,常见的M1巨噬细胞标志物有CD68、CD80、CD86、CD32等;常见M2巨噬细胞标志物有CD206、CD204、CD163等。
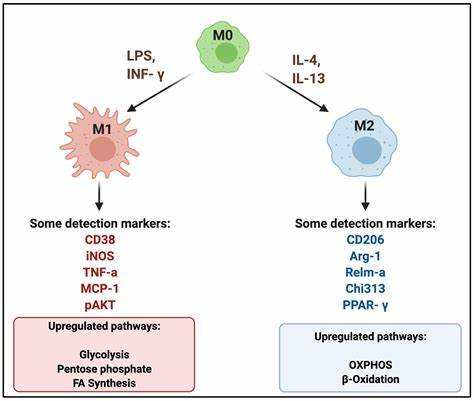
M1和M2型常见鉴定marker

AtomGit 是由开放原子开源基金会联合 CSDN 等生态伙伴共同推出的新一代开源与人工智能协作平台。平台坚持“开放、中立、公益”的理念,把代码托管、模型共享、数据集托管、智能体开发体验和算力服务整合在一起,为开发者提供从开发、训练到部署的一站式体验。
更多推荐
 已为社区贡献2条内容
已为社区贡献2条内容







所有评论(0)