重度抑郁症患者电休克治疗后海马微结构的改变
本篇文献分享发表于Molecular Psychiatry(IF=10.1)杂志,本公众号所发布内容旨在与大家分享学术新知,促进交流学习,版权归原作者或原出处所有,感谢各位学者的辛勤成果。

1. 引言
抑郁症是一种常见疾病,全球约3.4%的成年人受其影响,也是全球范围内导致功能丧失的主要原因。约三分之一的患者对常规治疗无反应。电休克治疗是治疗严重和难治性抑郁症的快速有效方法。多项荟萃分析证实了电休克治疗在抑郁症中的疗效,并报告了其在严重病例中起效迅速、安全性良好的特点。
电休克治疗导致海马体积增加的机制尚不完全清楚。动物研究表明,电休克刺激可增加成年非人灵长类动物的神经发生,并增强大鼠海马CA1区的树突分支和突触形成。人体研究同样支持这一假说:一项7T磁共振海马亚区研究发现,齿状回(含有可分化为新神经元的神经干细胞)体积与临床改善存在特异性关联。一项尸检研究发现,与未接受电休克治疗的抑郁症捐献者相比,接受电休克治疗者的人脑海马中神经可塑性标志物增加。此外,一种基于中枢神经系统来源细胞外囊泡提取的新型活体分子方法显示,难治性抑郁症患者中神经发生标志物双皮质素水平降低,而电休克治疗后显著升高。综上所述,这些发现支持海马神经发生可能有助于电休克治疗后海马体积增加和临床改善的假说。为进一步验证这一假说,神经可塑性的影像学生物标志物将有助于监测电休克治疗诱导的海马及临床变化。
弥散张量成像是目前最常用的活体脑微结构检查技术。虽然该技术非常适用于白质分析,但应用于灰质时存在局限性,因为其空间分辨率相对低于皮层厚度,易受部分容积效应和游离脑脊液污染影响,从而人为增加扩散率。此外,灰质的复杂组成(弥散的轴突、树突和神经元胞体共同导致各向异性降低)即使在高空间分辨率下也难以用简单的弥散张量模型准确描述。因此,仅有少数研究采用弥散张量成像评估主要精神疾病患者的灰质微结构。高阶多室生物物理模型,如近年提出的神经突方向离散度和密度成像(NODDI),已被用于研究精神疾病中的灰质微结构。NODDI从复杂神经组织中提取亚体素信息,提供三个指标:神经突密度指数(NDI)、各向同性分数(Fiso)和方向离散度指数(ODI)。NDI反映树突和轴突密度;ODI量化神经突取向的变异性(灰质中树突复杂性增加时ODI升高,白质中轴突复杂性增加时ODI升高);Fiso反映体素内神经突外空间的自由水量。具体而言,NODDI已证明能够检测颞叶癫痫患者海马及其亚区的微结构改变。在抑郁症研究中,NODDI揭示了多个白质区域的NDI降低,提示轴突密度较低。值得注意的是,截至目前,该方法尚未用于研究抑郁症患者的海马微结构,也未用于探索电休克治疗对脑微结构的影响。
在此背景下,此研究旨在检验以下假说:通过NODDI指标探测的海马神经发生可以解释电休克治疗后观察到的海马体积增加和临床改善。具体而言,此研究预期电休克治疗后神经突密度和方向离散度指数增加。此研究开展了一项前瞻性纵向研究,在三个时间点(基线V1、5次电休克治疗后V2、完成电休克治疗疗程后14天V3)监测严重抑郁症患者海马及其亚区在电休克治疗诱导下的宏观和微观结构变化,旨在评估这些变化与临床反应之间的关系。
2. 方法
2.1. 患者选择与研究设计
2018年6月至2022年4月期间,在GHU-巴黎大学医院(法国)招募18岁以上患者。纳入标准为:(1)符合DSM-5单相或双相重性抑郁障碍诊断标准;(2)需要接受电休克治疗。排除标准包括:共病精神障碍(如精神分裂症、广泛性发育障碍、除烟草外的物质滥用)、共病痴呆或任何神经系统疾病、过去6个月内接受过电休克治疗、处于妊娠状态、有磁共振检查禁忌症。该研究方案获得南地中海保护委员会(CPP17-046)批准。所有参与者均签署书面知情同意书。
2.2. 电休克治疗流程
电休克治疗(5000M MECTA spECTrum,Tualatin,OR,USA)每周两次,采用丙泊酚或依托咪酯进行麻醉,使用琥珀胆碱进行肌肉松弛。所有患者均采用双颞侧电极放置。采用基于年龄的方法确定个体电休克治疗电荷量。治疗持续至缓解(蒙哥马利-阿斯伯格抑郁评定量表评分(MADRS)<11分持续两周),或连续三次电休克治疗后患者无进一步改善时停止。
2.3. 临床评估
采用蒙哥马利-阿斯伯格抑郁评定量表(MADRS)和21项汉密尔顿抑郁评定量表 (HDRS-21),评估三个时间点的临床症状和治疗反应。每位患者在三个时间点由同一位精神科医生评估。治疗反应定义为 MADRS 评分下降>50%(ECT应答者),缓解定义为 MADRS 评分<11分(ECT缓解者)。
2.4. 磁共振采集
所有患者在3T磁共振扫描仪(MR750;GE Healthcare,Milwaukee,WI)上使用16通道头线圈进行扫描。成像序列如下:结构像使用3D T1加权扰相梯度回波序列,体素大小1 mm³,TR/TE = 8.2/3.2 ms,翻转角=11°。弥散像使用平面回波弥散加权多壳层序列,在q空间上设置三个壳层(b = 200/1500/2500 s/mm²,30/45/60个弥散方向),该参数方案针对NODDI模型进行了优化;同时采集三个b = 0 s/mm² T2加权容积作为参考。畸变校正采集反向相位编码序列(b = 2500 s/mm²,6个方向),用于后续校正磁敏感性引起的图像畸变。
2.5磁共振分析
解剖图像和弥散图像使用Ginkgo ToolBox(CEA)进行处理。图1汇总了图像分析的主要步骤。
使用FSL中的方法,对每个壳层的弥散图像分别进行磁敏感性畸变校正。将具有反相编码脉冲的扩散图像组合成单个校正图像。随后将预处理后的壳层数据拼接成的三壳层扩散图像,基于图像执行离群值校正、涡流校正及运动校正步骤。基于解剖3D T1-w图像计算脑掩膜。该T1-w图像事先使用3D刚性配准方法与平均b = 0 s/mm² T2图像进行配准,确保空间对齐。
为保持原始弥散图像强度的真实性,未对图像进行信号强度校正。使用多室NODDI模型计算NDI、Fiso和ODI图。模型参数中,固有自由扩散率固定为1.7×10⁻³ mm²/s,各向同性扩散率固定为3×10⁻³ mm²/s。同时使用弥散张量成像模型提取标准弥散图,包括轴向扩散率(AD)、径向扩散率(RD)、平均扩散率(MD)和各向异性分数(FA)。计算高阶解析Q-ball场(球谐阶数8,正则化因子λ = 0.006),用于估计各向异性分数图。该方法在纤维交叉配置下具有更高的稳健性。
使用FreeSurfer 7.0.0分割T1-w图像,提取左右海马并进行亚区分割。考虑到齿状回非常薄,边界难以精确定义,且弥散加权图像分辨率为2 mm,此研究采用亚区分割的‘CA’版本,将颗粒细胞层、分子层和齿状回合并到角回4区。这个合并区域在下文中统称为齿状回。值得注意的是,既往尸检研究发现,海马神经发生的组织学标志物不仅存在于齿状回的颗粒细胞层和颗粒下层,也存在于角回4区。海马尾部也作为对照区域进行分割,以检验齿状回中与神经发生相关的特异性变化。对双侧海马体、齿状回及海马尾部进行了宏观体积测量及基于平均 NODDI 的指标评估。
2.6. 统计分析
统计分析使用R 3.4软件完成。为评估电休克治疗对海马宏观结构(体积)和微观结构(弥散张量成像和NODDI指标)的影响,此研究拟合了单变量线性混合效应模型,将性别、年龄、扫描时已接受的电休克治疗次数以及时间(V1、V2、V3三个时间点)作为固定效应,受试者个体作为随机效应。采用方差分析评估主效应和交互作用,使用Wald χ²检验检验统计学显著性,双侧p < 0.05视为显著。对于8个微结构指标的多重比较,应用Bonferroni方法校正,显著性阈值设为α = 0.05/8 = 0.006。
临床相关性分析方面,为分析海马变化与临床变化的关系,首先计算变化率ΔV2 = (V2 - V1)/V1和ΔV3 = (V3 - V1)/V1,以控制基线水平。随后采用线性模型分析海马变化率(因变量)与临床指标(自变量)的关系,模型中纳入电休克治疗次数、年龄、性别作为混杂变量。由于测试了多个评分(2个)和多个指标(8个),应用Bonferroni校正,显著性阈值设为α = 0.05/(2×8) = 0.003,仅p ≤ 0.003的结果视为显著。分析针对海马和齿状回分别进行,为清晰起见,结果部分仅报告通过Bonferroni校正的结果。
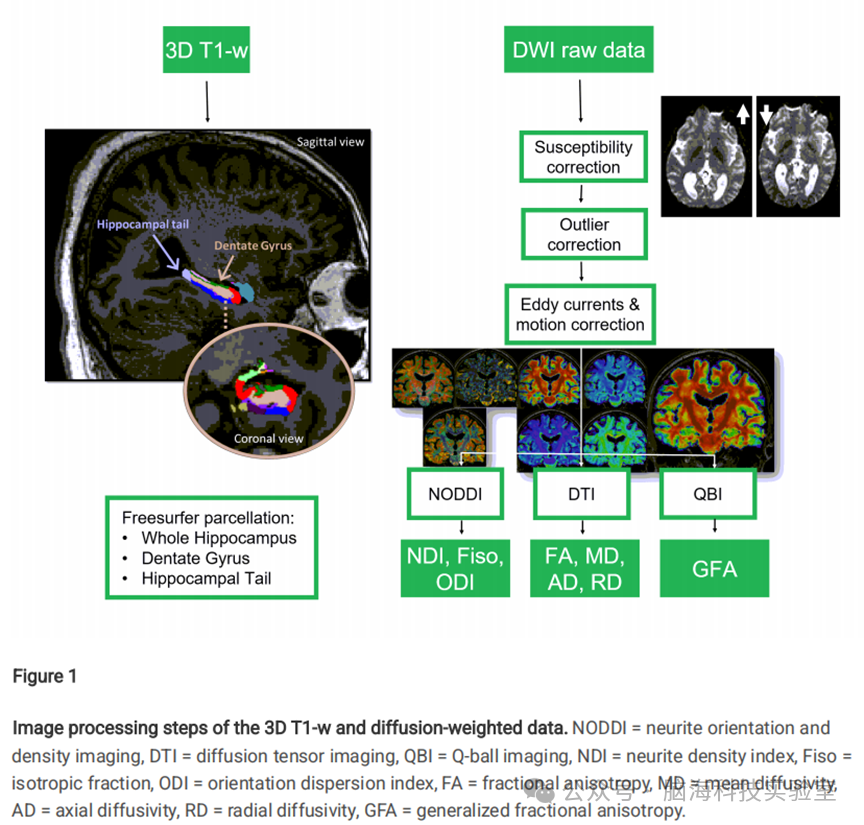
图1三维T1加权与弥散加权数据的图像处理步骤。
在脑海科技云平台中,内置了NODDI分析模块,支持用户批量处理数据,并确保每一步参数设置都有据可查。平台提供完整的操作文档、培训视频及更新日志体系,便于用户快速掌握。此外,平台的项目管理模块可清晰记录数据筛选标准、排除被试原因、分析版本等信息,极大提升了研究的透明度和可复现性。读者可对照思考如何在平台中实现类似的分析流程。感兴趣可联系预约产品演示。

3. 结果
3.1. 患者特征
患者人口学和临床特征详见表1。V1和V3时间点之间的平均间隔为70±25天。
3.2. 宏观结构变化
3.2.1. 全海马体积
对107次磁共振扫描图像进行了结构变化的分析。混合效应分析显示,电休克治疗相关的双侧全海马体积在V1和V2之间显著变化(左侧:+4.8%,p < 0.001;右侧:+4.3%,p < 0.001),右侧海马在V1和V3之间也显著变化(+4.8%,p < 0.001)(图2)。
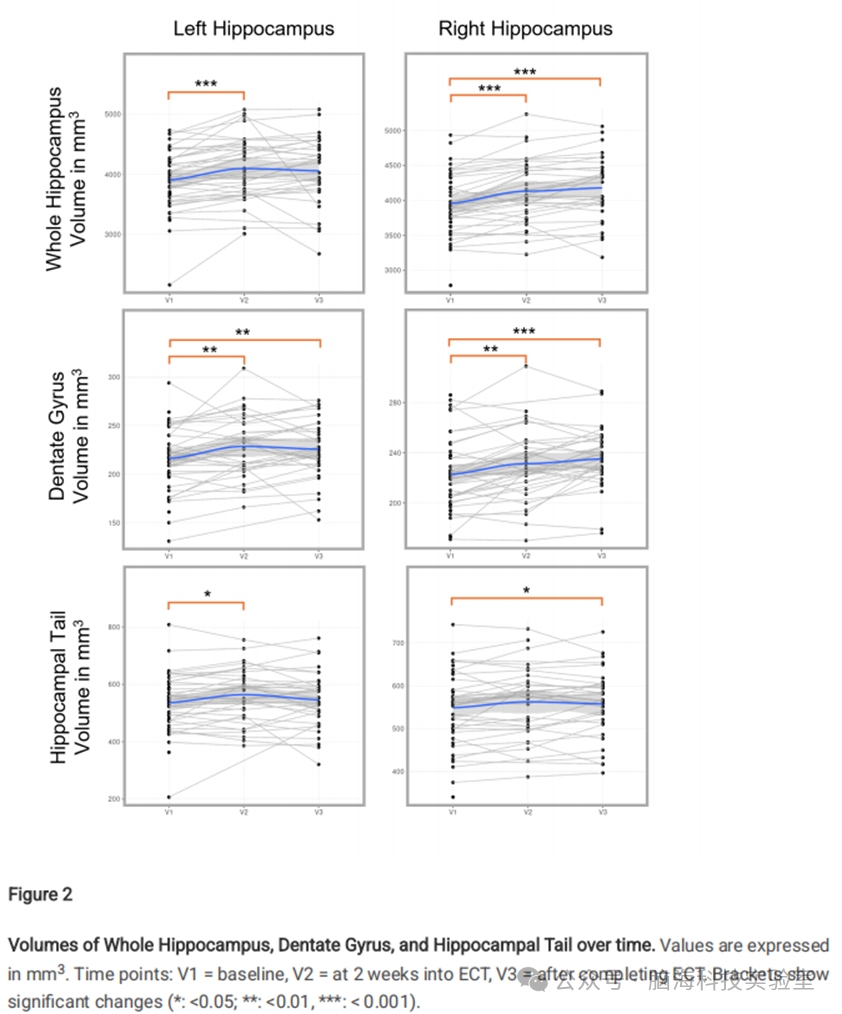
图2全海马体、齿状回及海马尾部体积随时间变化。
3.2.2. 齿状回和海马尾部体积
齿状回体积在V1和V2之间双侧增加(左侧:+4%,p = 0.008;右侧:+3.5%,p = 0.003),在V1和V3之间也双侧增加(左侧:+4.8%,p = 0.009;右侧:+5.5%,p < 0.001)。此外,海马尾部体积在左侧海马V1和V2之间增加(+2.5%,p = 0.03),在右侧海马V1和V3之间增加(+2.3%,p = 0.03)。
3.3. 微结构变化
3.3.1. 全海马
4次磁共振检查的弥散加权图像存在严重伪影无法使用,因此103次扫描可用于分析。弥散张量成像分析显示:左侧海马各向异性分数在V1和V2之间显著下降;左侧海马平均扩散率在V1和V3之间显著下降;双侧海马轴向扩散率在V1和V3之间显著下降;右侧海马轴向扩散率在V1和V2之间显著下降(图3)。
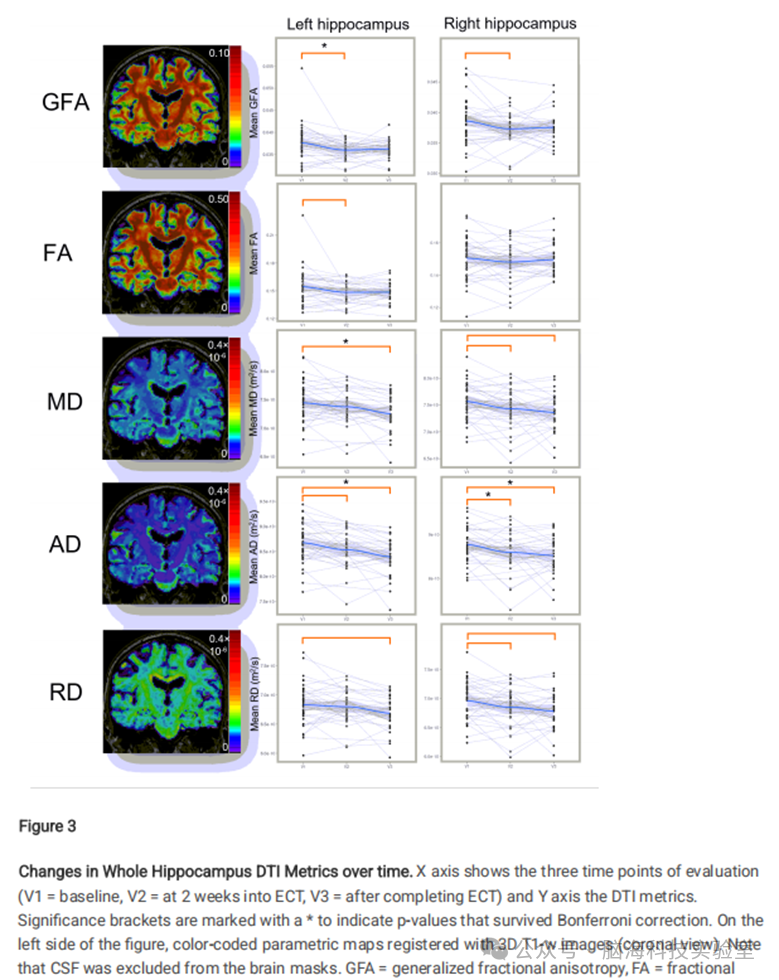
图3全海马亚区DTI指标随时间的变化趋势。
NODDI分析也显示电休克治疗相关的显著时间变化。右侧海马神经突密度指数在V1和V3之间增加;双侧海马各向同性分数在V1和V2之间下降;双侧海马方向离散度指数在V1和V2之间以及V1和V3之间增加(图4)。
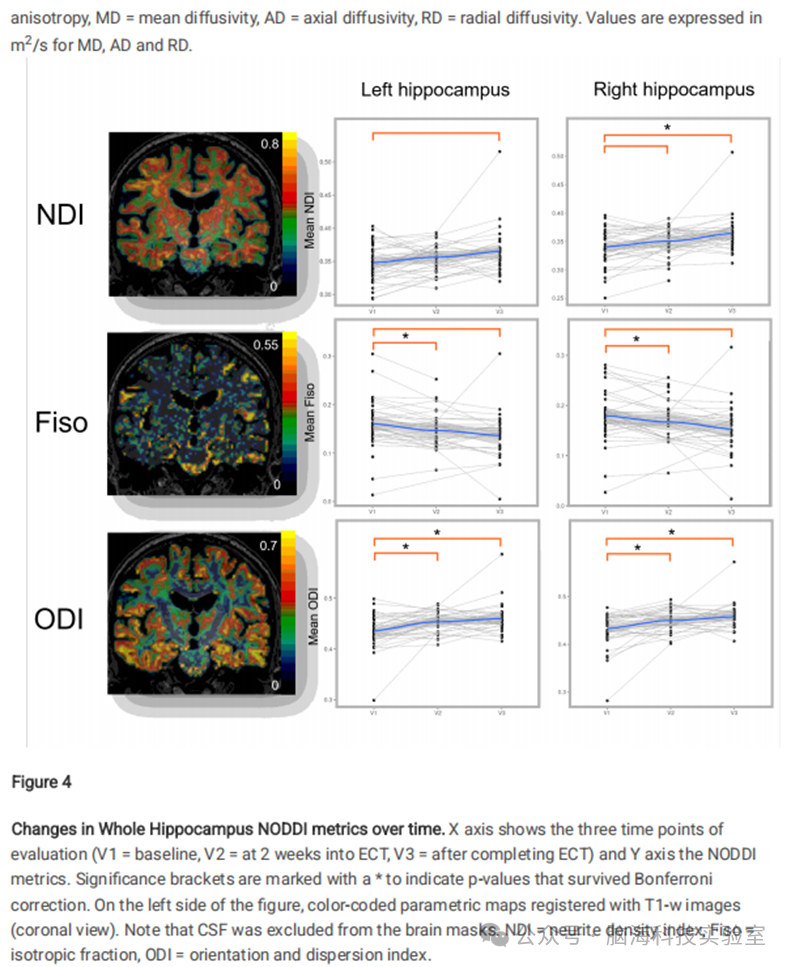
图4全海马体 NODDI 指标随时间的变化趋势。
弥散张量成像和NODDI参数的平均值及统计分析详细结果见补充信息。从分析中剔除异常值不影响结果的显著性。
3.3.2. 齿状回和海马尾部
海马亚区分析显示:右侧齿状回各向异性分数在V1和V2之间显著下降(p = 0.005);双侧海马各向异性分数在V1和V2之间显著下降(p < 0.001),左侧海马在V1和V3之间也显著下降(p < 0.001)。左侧齿状回轴向扩散率在V1和V3之间下降(p < 0.001);双侧海马各向同性分数在V1和V2之间下降(左侧:p < 0.001,右侧:p = 0.002)。相反,右侧齿状回方向离散度指数在V1和V2之间增加(p < 0.001),双侧在V1和V3之间增加(左侧:p = 0.002,右侧:p = 0.001)。
3.4. 临床相关性分析
海马变化与临床改善关系的分析显示,电休克治疗应答者和缓解者在V1和V2之间右侧海马体积显著增加(应答者+4.8% vs 无应答者-0.7%,p < 0.001;缓解者+4.9% vs 未缓解者+1.1%,p = 0.017)(图5)。其他临床相关性(包括微结构特征)未通过Bonferroni校正。
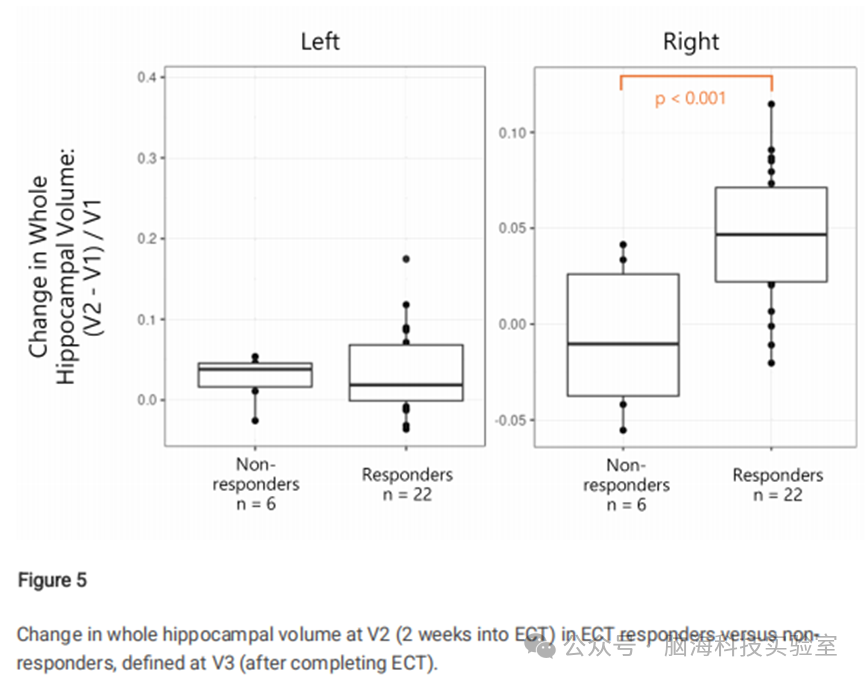
图5显示,根据治疗结束时(V3)的疗效将患者分为应答者与非应答者,并比较这两组患者在治疗第2周(V2)时全海马体积的变化。
4. 讨论
在此纵向研究中,首次使用神经突成像技术探讨了重度抑郁症患者电休克治疗后海马的微结构变化。此研究旨在检验假说并识别电休克治疗诱导的海马神经发生的活体生物标志物。除了观察到体积增加外,此研究还观察到神经突密度和离散度增加,以及各向同性分数(即自由水)降低,提示海马突触分支增加。
此研究发现电休克治疗后海马体积增加,与近期荟萃分析和全球电休克治疗-磁共振研究合作组织的大样本分析一致,这些研究报告电休克治疗后一两周内海马体积显著增加。除宏观体积变化外,此研究还报告了电休克治疗后的微结构变化,包括各向异性分数、平均扩散率和轴向扩散率降低,以及自由水成分的改变。此研究还观察到神经突密度和取向离散度增加。既往弥散张量成像研究报道电休克治疗后双侧海马平均扩散率降低,这一发现支持神经可塑性改变而非发作后水肿(后者通常因细胞外液增加而表现为平均扩散率升高)。此研究观察到双侧轴向扩散率显著降低和左侧平均扩散率降低,与既往弥散张量成像研究结果一致。此研究还检测到电休克治疗诱导的双侧广义各向异性分数早期降低,与Jorgensen等人的研究一致。这种各向异性分数降低可能与锥体神经元轴突和树突过程的扩展有关。
此研究首次使用NODDI模型分析电休克治疗诱导的海马亚体素水平变化。此研究的目的是确定既往弥散张量成像研究中观察到的变化是否可归因于海马神经发生,而非细胞肿胀(如发作后状态或急性缺血性卒中中观察到的细胞内水肿)。在此,此研究观察到右侧海马从基线到电休克治疗后神经突密度增加,各向同性分数初始双侧下降,以及取向离散度指数在所有三个时间点持续增加。在细胞肿胀的情况下,由于水从细胞外空间向细胞内空间转移,神经突密度增加和各向同性分数下降也是预期会出现的,但树突取向不会发生变化。鉴于在此研究在双侧海马观察到的取向离散度指数增加,电休克后细胞肿胀的假说似乎不太可能,反而支持树突复杂性增加和突触发生,与此研究初始假说一致。
值得注意的是,海马亚区分析显示某些变化特异性发生在齿状回。事实上,神经突密度指数增加和各向同性分数下降仅在齿状回观察到,而在海马尾部未观察到,这与齿状回中发生神经发生一致。全海马(包括尾部)的各向异性分数下降和取向离散度指数增加可能反映突触发生,这可能发生在所有海马亚区。
电休克后这些微结构变化的时间进程提出了一个问题:此研究是否真的在观察活跃的新细胞形成?在此研究中,各向同性分数和方向离散度指数的变化在V2(电休克开始后两周)观察到,先于神经突密度的变化(发生在V3,平均距基线70天)。自发海马神经发生需要几个月的时间,在此期间神经干细胞成熟为祖细胞、未成熟颗粒细胞迁移到齿状颗粒细胞层,最终成熟并建立功能性连接。最近一项尸检研究的结果为这一讨论提供了依据。虽然他们观察到电休克治疗受试者中树突生长标志物双皮质素增加,但未发现细胞增殖标志物Ki-67的差异。虽然Ki-67表达时间短于电休克与死亡之间的间隔可能是原因之一,但作者也提出这可能表明其样本中电休克后增加的是神经可塑性而非活跃的新细胞形成。
文献中提出了两种可能解释此类海马神经可塑性病理生理学的理论。首先,电休克治疗可能使齿状回的现有神经元发生“去成熟化”,即成熟细胞可能被激活并建立新的树突连接。另一种假说是电休克治疗可能促进储存在齿状颗粒细胞层中的未成熟颗粒细胞的树突成熟,绕过先前的成熟步骤,从而加速自发神经发生过程。有趣的是,动物研究表明,电休克刺激可诱导新颗粒细胞的树突棘成熟,增加成熟颗粒细胞的树突棘密度,并增强大鼠海马CA1区的突触发生和树突分支。
重要的是,此研究观察到电休克治疗应答者在5次电休克治疗后右侧海马体积增加显著大于无应答者,这一发现既往文献未见报道。这些发现可能有助于早期预测治疗疗效,并加速无应答患者停止电休克治疗。这一发现可能得益于固定的V2时间点(安排在5次电休克治疗后),使得组间比较更可靠。然而,与使用7T磁共振扫描仪的研究不同,此研究中齿状回的体积变化与临床反应无相关性,可能归因于该区域较薄以及3T磁共振采集的空间分辨率较低。微结构指标也与临床反应无相关性。一种解释是弥散成像的空间分辨率比3D T1-w图像差(2 mm vs 1 mm各向同性体素),且更容易受部分容积效应影响。虽然由于采集时间长以避免信号损失,实现高分辨率脑弥散成像历来具有挑战性,但近期弥散磁共振成像的进展表明,未来可能在临床实现亚毫米级分辨率,从而克服这一局限性。
此研究存在若干局限性。首先,43名患者中仅27人完成了全部三次磁共振评估,7人仅完成基线磁共振。为解决这一问题,此研究使用了线性混合效应模型,该模型适用于纵向设计中的缺失数据。其次,此研究将时间作为具有三个时间点的分类变量建模;然而,更有效的方法可能是利用轨迹技术来考虑基线与V3时间点之间间隔的变异性。第三,此研究数据仅捕捉电休克治疗开始后三个月内发生的变化。多项研究报告电休克治疗后6至12个月海马体积恢复正常,提示电休克治疗效应的短暂性。由于研究设计限制,此研究无法提供观察到的变化长期持续性的证据。然而,这一方面对于此研究的主要目标(阐明电休克治疗后数周观察到的海马体积增加的病理生理机制)并非关键。
此研究中,使用神经突成像观察到的海马微结构改变提示存在海马神经可塑性,为理解电休克治疗对抑郁症患者治疗效果的潜在机制提供了新见解。此外,电休克治疗开始两周后观察到的右侧海马体积增加与治疗反应相关,可能作为电休克治疗疗效的有前景的预后生物标志物。
解读:脑海科技
参考文献
Le Berre A, Attali D, Uszynski I, et al. Hippocampal microstructural changes following electroconvulsive therapy in severe depression. Mol Psychiatry. 2025;30(9):4343-4352. doi:10.1038/s41380-025-03016-x

AtomGit 是由开放原子开源基金会联合 CSDN 等生态伙伴共同推出的新一代开源与人工智能协作平台。平台坚持“开放、中立、公益”的理念,把代码托管、模型共享、数据集托管、智能体开发体验和算力服务整合在一起,为开发者提供从开发、训练到部署的一站式体验。
更多推荐
 已为社区贡献15条内容
已为社区贡献15条内容





所有评论(0)