探索重复经颅磁刺激治疗重度抑郁症的能力:神经网络的动态因果模型
本篇文献分享发表于Translational Psychiatry杂志。所发布内容旨在与大家分享学术新知,促进交流学习,版权归原作者或原出处所有,感谢各位学者的辛勤成果。

1.引言
重型抑郁障碍是全球疾病负担的首要原因。根据世界卫生组织2020年的数据,其导致的健康生命年损失在所有疾病中排名第二。重复经颅磁刺激(rTMS)是一种非侵入性治疗方法,通过作用于左侧背外侧前额叶皮层(DLPFC)产生兴奋性效应,目前已用于治疗对多种抗抑郁药无效的难治性抑郁症患者。
抑郁症治疗的经典rTMS方案是采用高频刺激(>5Hz)作用于左侧DLPFC。近期,一种名为斯坦福加速智能神经调控疗法(SAINT)的新方案已获得美国食品药品监督管理局批准,该疗法采用间歇性θ脉冲刺激左侧DLPFC来产生兴奋性效应。然而,由于生物学机制尚不明确,其疗效仍有限,有效率仅为30-50%。因此,深入理解rTMS治疗抑郁症的生物学基础,对于提高其临床疗效至关重要。
既往的遗传学、尸检和神经影像学研究显示,抑郁症可能与DLPFC神经回路的失调有关,具体表现为结构异常、突触神经递质标志物改变,以及与下游脑区的连接异常。值得注意的是,Padmanabhan等人利用静息态功能磁共振成像发现,能够诱发抑郁症状的脑损伤位置,都可以映射到一个以左侧DLPFC为核心的脑回路中。与此相对应,对抑郁症患者左侧DLPFC进行rTMS治疗,可能是通过远程调节与左侧DLPFC功能相连的、分布式的抑郁相关脑区,从而协同改善症状实现的。Siddiqi等人进一步发现,诱发抑郁症状的脑损伤部位和治疗抑郁症的神经调控刺激位点,竟然汇聚在同一个脑回路上。这提示了一个直接的因果关系:特定脑回路受损会引发抑郁,而针对该回路进行治疗性刺激则能缓解抑郁症状。这一假设得到了连接组学研究的支持,这些研究证实了抑郁相关脑回路与左侧DLPFC之间存在功能上的相互连接。这些研究强调理解左侧DLPFC相关抑郁回路中各脑区的相互作用,对阐明抑郁症病理生理机制至关重要。
关于抑郁相关脑回路,已有大量研究确定多个与左侧DLPFC功能相连的脑区在抑郁症病理生理中起着关键作用,这些脑区包括杏仁核(AMY)、伏隔核(NAC))、前脑岛(AI)、膝下前扣带回皮层(sgACC)以及腹内侧前额叶皮层(VMPFC)。既往研究表明,以左侧DLPFC为靶点的rTMS可以调节sgACC与其他抑郁相关脑区之间的功能连接。此外,多个在精神病理层面导致抑郁症状的脑区,如NAC、AMY、VMPFC和AI在功能上都汇聚于左侧DLPFC。值得关注的是,SAINT疗法通过刺激左侧DLPFC,改变了sgACC和AI之间的定向时间偏移,从而改善了抑郁症状。同时,SAINT的预防自杀效果与脑岛相关的连接有关。多项研究进一步表明,这些区域共同构成一个广泛关联于抑郁症的神经回路。在这个回路中,sgACC、VMPFC和左侧DLPFC相互交汇,整合了病变部位的连接特征和神经调控的靶点。通过连接组学方法,研究者发现左侧DLPFC、sgACC、VMPFC、AI、NAC和AMY形成了一个独特的抑郁特异性脑回路,与抑郁症患者的情绪失调密切相关。这些区域与Siddiqi等人划定的抑郁相关回路在空间上高度重合。抑郁症本质上是由于抑郁相关脑区之间协同功能的紊乱造成的,因此,识别左侧DLPFC相关抑郁回路中各脑区之间的功能关系,有望为抑郁症的病理生理机制以及rTMS治疗的作用原理提供全新的见解。
既往研究采用传统方法发现了脑区间异常的功能连接,但这些方法捕捉的是静态的时间特征,未能反映大脑活动的动态变化。然而,全脑活动的动态过程对于情绪和认知功能的调控至关重要。动态因果建模(DCM)是近年来发展起来的一种方法,通过估计感兴趣脑区之间的因果关系来研究大脑活动的动态模式。传统的DCM最初应用于基于任务的fMRI研究,而新近发展的DCM方法则能够利用静息态fMRI数据评估分布性脑区之间的因果关系。已有数项研究将这种方法应用于抑郁症患者的静息态fMRI数据。然而,目前尚无研究以抑郁相关脑回路为切入点,探讨抑郁症患者各脑区之间异常的动态交互模式。此外,多数研究仅基于单一站点的小样本数据来分析抑郁症患者的异常功能连接。这种局限性可能是导致既往研究结果不一致的原因之一,阻碍了此研究对抑郁症及rTMS治疗神经基础的理解。
此研究旨在利用包含270名健康对照和175名抑郁症患者的大样本、多站点静息态fMRI数据集,揭示抑郁症患者抑郁相关脑区之间异常的动态交互模式。鉴于与左侧DLPFC功能相连的脑回路在抑郁症病理生理机制中的核心地位,此研究假设与左侧DLPFC存在异常功能连接的脑区可能在抑郁症中扮演关键角色。研究首先在全脑范围内识别出与左侧DLPFC存在功能连接改变的区域,然后采用DCM分析评估这些区域(即与左侧DLPFC连接异常的区域)以及抑郁相关脑回路中的关键区域(包括左侧DLPFC、AMY、NAC、AI、sgACC和VMPFC)之间的因果关系。厘清抑郁相关脑回路内部以及与左侧DLPFC连接异常区域之间异常的因果关系,将有助于更深入地理解rTMS治疗抑郁症的潜在机制。
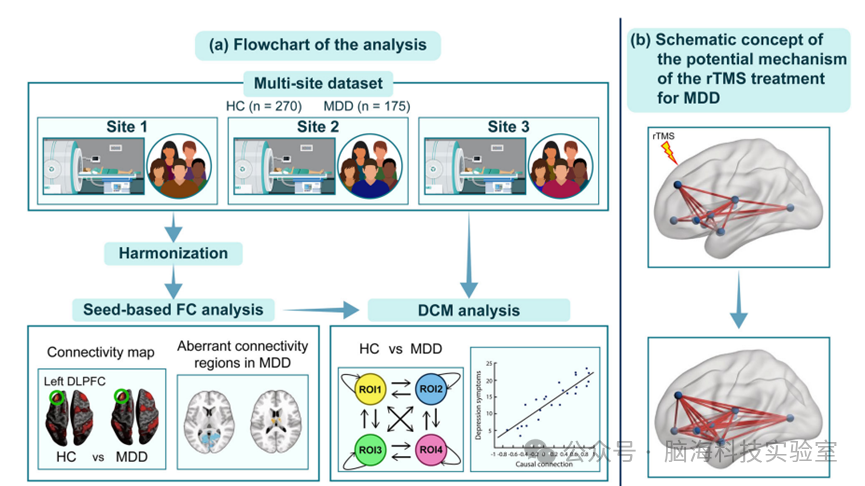
图1研究方案流程图及重复经颅磁刺激(rTMS)治疗 MDD 潜在机制示意图。
2.材料与方法
2.1数据集与参与者
此研究共纳入445份静息态功能磁共振成像数据,一部分来自和歌山医科大学精神病学系,另一部分来自DecNef项目脑数据库的公开数据。该开放数据集是日本脑科学促进战略研究计划的一部分。
研究对象包括抑郁症患者和健康对照,来自三个影像站点:和歌山医科大学站点、东京大学站点和广岛大学创新中心站点(后两个站点的数据包含在公开数据集中)。三个站点共招募270名健康对照和175名抑郁症患者。
部分参与者因头部运动过大(>2 mm)或功能图像无法准确配准到标准空间而被排除。最终分析共纳入177名健康对照和120名抑郁症患者。
此研究遵循《赫尔辛基宣言》,获得和歌山医科大学伦理委员会批准,所有参与者均签署书面知情同意书。
抑郁症状评估工具因站点而异:和歌山医科大学站点:采用17项汉密尔顿抑郁评定量表东京大学站点:采用贝克抑郁量表修订版(32例)和流行病学研究中心抑郁量表(30例)广岛大学创新中心站点:采用贝克抑郁量表修订版(37例)为统一不同量表的评分,此研究先将汉密尔顿评分转换为贝克评分,再将贝克评分和流行病学研究中心评分统一转换为PROMIS抑郁评分。
2.2 rs-fMRI数据预处理
使用SPM12软件进行磁共振数据预处理。首先进行时间层校正,并将EPI图像与首张图像对齐以校正头部运动。校正后的EPI图像与解剖结构像T1配准,然后统一分割并配准到标准空间。对归一化后的图像进行空间平滑处理,采用半高全宽6毫米的高斯核。
此外,还对分割后的灰质图像进行归一化,用于后续提取灰质区域的BOLD信号时间序列。同样,对分割后的脑脊液和白质图像进行归一化,用于提取以提取脑脊液和白质区域的非神经信号。
排除标准包括:头部运动超过2毫米以及FD大于0.5毫米,空间标准化效果不佳。
最终,和歌山医科大学站点排除20名健康对照和16名抑郁症患者,东京大学站点排除10名健康对照和4名抑郁症患者,广岛大学创新中心站点排除63名健康对照和34名抑郁症患者,共297名参与者进入最终分析。
对于基于种子点的功能连接分析,此研究应用了0.009-0.08 Hz的时间带通滤波,并通过线性回归去除六个运动参数以及脑脊液、白质和全脑平均信号等非神经信号。功能连接分析中,此研究参照先前研究,剔除了FD大于0.5毫米的全脑。经检验,健康对照组和抑郁症组的头部运动无显著差异,因此后续分析未将头部运动参数作为协变量纳入。
2.3感兴趣区的选定
左侧DLPFC的种子点定义为以MNI坐标[-41.25, 42.25, 29.25]为中心、半径10毫米的球形区域。该坐标综合了既往研究中采用的多个左侧DLPFC坐标的平均值。
双侧AMY的感兴趣区采用AAL3创建。双侧NAC的感兴趣区定义为以坐标[14, 10, 0]和[-14, 10, 0]为中心、半径8毫米的球形区域。双侧AI的感兴趣区定义为以坐标[-4, 25, 37]和[-32, 24, -6]为中心、半径6毫米的球形区域。sgACC的感兴趣区定义为以坐标[-10, 6, 16]为中心、半径6毫米的球形区域。VMPFC的感兴趣区定义为以坐标[0, 46, -6]为中心、半径10毫米的球形区域。
此外,此研究将功能连接分析中发现与左侧DLPFC连接异常的区域,即双侧丘脑(Thal)和视觉皮层(VIS),也纳入后续DCM分析。双侧丘脑的感兴趣区定义为以坐标[7.21, -12.8, 8.77]和[-6.78, -14.3, 14.4]为中心、半径6毫米的球形区域。视觉皮层的感兴趣区定义为以坐标[-2.24, -68.9, 6.7]为中心、半径6毫米的球形区域。图3展示了DCM分析中所有感兴趣区的位置。
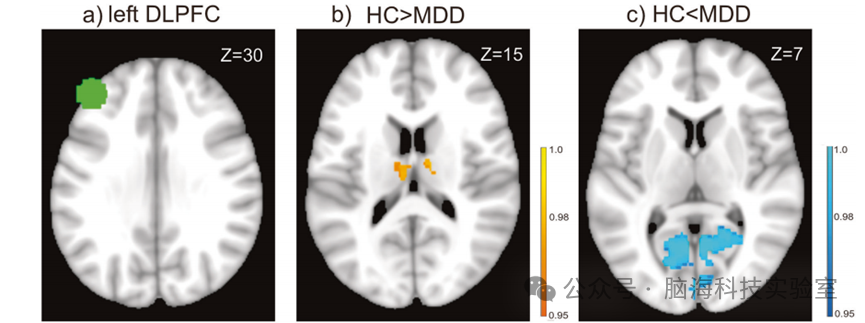
图2在MDD中显示与左侧 DLPFC 存在异常功能连接(FC)的脑区。
2.4 基于种子点的功能连接分析与ComBat标准化
此研究提取左侧DLPFC感兴趣区内所有体素的时间序列并取平均值,计算其与全脑灰质各体素时间序列的皮尔逊相关系数,并通过费舍尔变换转换为z值图。
为消除不同站点间的数据差异,此研究采用ComBat标准化方法,将参与者的年龄、性别和疾病情况作为协变量,对数据进行校正。
数据标准化后,采用双样本t检验进行组间比较,并以年龄和性别作为协变量,通过TFCE方法和10000次置换检验进行多重比较校正,显著性水平设为p<0.05。
2.5动态因果建模
此研究采用SPM12中的谱动态因果建模对预处理后的静息态fMRI数据进行分析。DCM通过构建符合神经生理机制的模型来估计观察到的BOLD信号,从而推断网络中各节点之间的因果关系。此研究提取各感兴趣区的BOLD时间序列,回归了白质、脑脊液以及六个头部运动参数。每个参与者采用全连接模型,即任意两个感兴趣区之间均存在双向连接。由于模型包含八个感兴趣区,共估计64个自由参数。
2.6组水平DCM的参数经验贝叶斯分析
采用标准参数经验贝叶斯分析方法进行组水平分析和贝叶斯模型平均。PEB将每个参与者的个体连接参数带入群体水平,在贝叶斯分层框架下用广义线性模型进行建模,从而将连接强度的估计及其不确定性从个体水平传递到群体水平。首先,在PEB框架下比较健康对照组和抑郁症组之间的因果连接差异,将年龄、性别和站点效应作为协变量纳入模型。其次,在抑郁症组中检验因果连接与抑郁严重程度之间的关联,同样将年龄、性别和站点效应作为协变量。抑郁严重程度采用统一的PROMIS抑郁评分度量。此研究重点关注那些在抑郁症患者中存在异常的连接参数,并将后验概率大于95%定义为存在显著效应的标准。
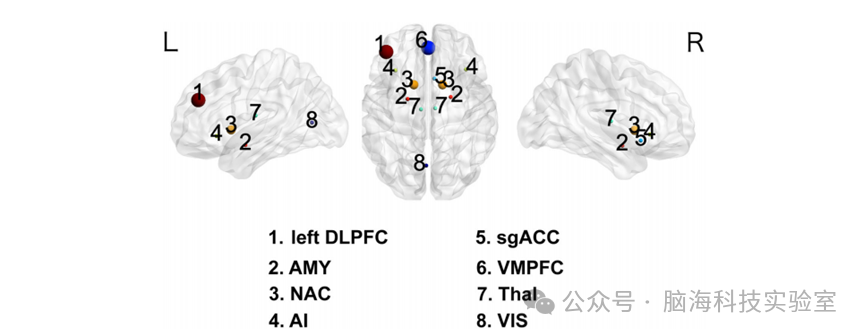
图3 DCM分析中所有感兴趣区的位置。
在脑海科技云平台中,内置了DCM分析模块,支持用户批量处理数据,从感兴趣区定义、DCM模型构建到PEB组水平统计,每一步参数设置都有据可查。平台的项目管理模块可清晰记录数据筛选标准、排除被试原因等信息,极大提升了因果推断研究的透明度和可复现性。读者可对照思考如何在平台中实现类似的分析流程。感兴趣可联系预约产品演示。

3.结果
3.1基于种子点的功能连接分析:健康对照组与抑郁症组的比较
按照研究流程,此研究首先探究了抑郁症患者与左侧DLPFC存在异常功能连接的脑区。结果显示,与健康对照组相比,抑郁症患者左侧DLPFC与双侧Thal的功能连接显著降低,而与VIS的功能连接显著增强(图2a-c,表3)。
3.2动态因果建模分析:健康对照组与抑郁症组的比较
各组数据经检验符合正态分布且方差齐性,通过DCM分析抑郁相关脑回路以及与左侧DLPFC连接异常区域之间的因果关系, 结果显示:
与健康对照组相比,抑郁症患者表现出:
(1)增强的因果连接:从AI到AMY、从sgACC到NAC、从Thal到VIS;
(2)增强的自我抑制:AMY的自我抑制性连接增强;
(3)减弱的因果连接:从左侧DLPFC到VIS、从AMY到sgACC、从AMY到VIS、从NAC到sgACC、从NAC到VIS、从AI到NAC、从AI到VMPFC;
(4)减弱的自我抑制:Thal的自我抑制性连接也减弱。
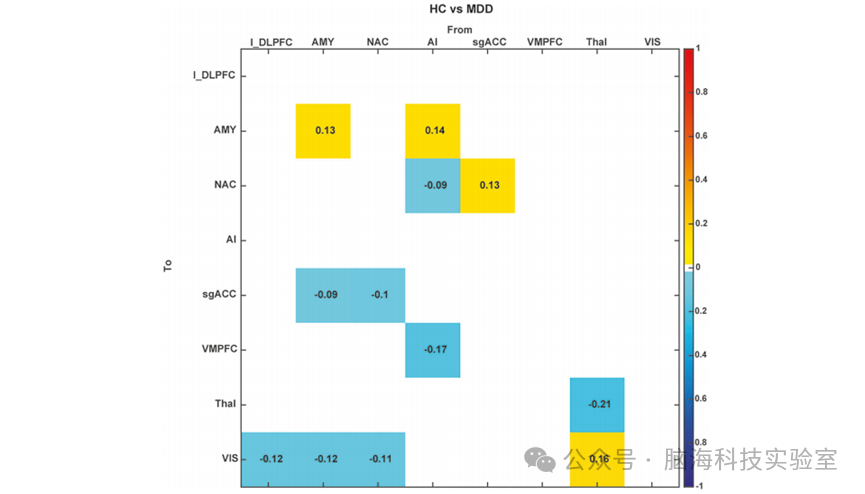
图4 HC与MDD 之间因果关系参数的组间比较。
3.3因果连接与抑郁严重程度的关联
最后,此研究分析了抑郁症患者中因果连接与抑郁症状严重程度的关系。结果显示:
从AMY到sgACC的因果连接与抑郁严重程度呈正相关;从NAC到VIS、从AI到VMPFC的因果连接与抑郁严重程度呈负相关。
此研究重点关注的是那些既与抑郁严重程度显著相关(后验概率>95%),又在抑郁症患者中相较于健康对照组存在显著异常(后验概率>95%)的连接。
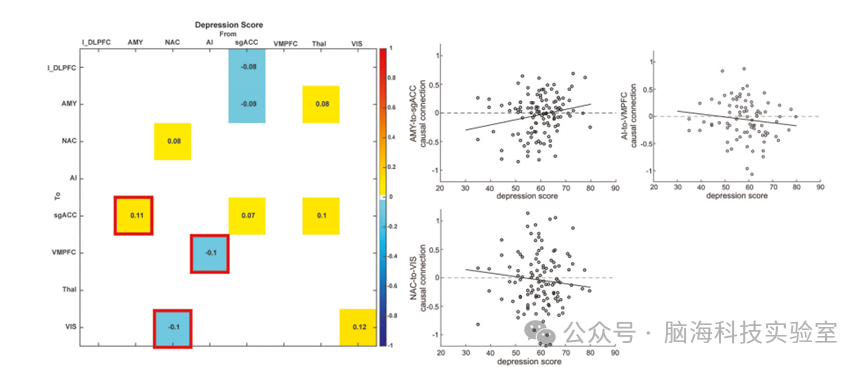
图5 因果关联参数与抑郁评分之间的相关性。
4.讨论
此研究利用大样本多站点静息态功能磁共振成像数据,通过动态因果建模分析了抑郁症患者抑郁相关脑回路内部以及与左侧背外侧前额叶皮层连接异常区域之间的因果关系,主要发现可归纳为两个方面。
第一,异常因果连接从多个抑郁相关脑区流向视觉皮层。此研究发现抑郁症患者存在从左侧背外侧前额叶皮层、杏仁核、伏隔核、丘脑到视觉皮层的因果连接减弱,且伏隔核到视觉皮层的连接与抑郁严重程度呈负相关。这一结果提示,作为初级脑区的视觉皮层可能在抑郁症病理机制中扮演着被长期忽视的重要角色。事实上,既往研究也发现抑郁症患者存在视觉皮层功能整合异常,视觉皮层与皮层下及前额叶区域的异常连接可能影响信息更新过程,并与治疗反应相关。这些发现共同指向一个观点:抑郁症的病理生理机制可能不仅涉及高级认知中枢,也延伸至感觉加工等基础功能层面。
第二,皮层下区域与腹内侧前额叶皮层之间的因果连接异常。此研究发现抑郁症患者存在从前脑岛到多个区域(杏仁核、伏隔核、腹内侧前额叶皮层)、膝下前扣带皮层到伏隔核、杏仁核到膝下前扣带皮层的因果连接异常。值得注意的是,杏仁核到膝下前扣带皮层的连接与抑郁严重程度呈正相关,而前脑岛到腹内侧前额叶皮层的连接与抑郁严重程度呈负相关。这些结果提示,包括杏仁核、伏隔核、前脑岛、膝下前扣带皮层、丘脑在内的皮层-纹状体回路功能紊乱,可能是抑郁症情绪调节障碍的重要神经基础。
综合来看,此研究所发现的异常因果连接可分为两类:一是抑郁相关脑区向视觉皮层的投射,二是皮层-纹状体回路内部连接。这一区分具有重要的临床启示:重复经颅磁刺激治疗抑郁症的潜在机制可能涉及两个方面,一方面通过刺激左侧背外侧前额叶皮层远程调节伏隔核、丘脑、视觉皮层等区域的异常活动,另一方面改善抑郁核心回路内部的功能紊乱。这一推测与既往研究发现的左侧背外侧前额叶皮层刺激可调节抑郁相关回路活动的结果相一致。
当然,此研究存在一定局限性。首先,大部分抑郁症参与者未接受重复经颅磁刺激治疗,因此无法直接讨论重复经颅磁刺激的疗效机制。其次,由于缺乏详细的用药信息,未能完全排除药物对结果的影响。此外,病程长短和临床状态(如急性期或缓解期)等因素也未纳入分析。未来研究需要结合干预性设计,进一步验证此研究提出的异常因果连接是否可作为重复经颅磁刺激治疗的潜在靶点。
综上,此研究揭示的异常因果模式为理解抑郁症的病理生理机制及重复经颅磁刺激治疗原理提供了新的视角。
解读:脑海科技
参考文献
Kita A, Ishida T, Kita N, et al. Exploring the capabilities of repetitive transcranial magnetic stimulation in major depressive disorder: Dynamic causal modeling of the neural network. Transl Psychiatry. 2025;15(1):257. Published 2025 Jul 25. doi:10.1038/s41398-025-03480-7

AtomGit 是由开放原子开源基金会联合 CSDN 等生态伙伴共同推出的新一代开源与人工智能协作平台。平台坚持“开放、中立、公益”的理念,把代码托管、模型共享、数据集托管、智能体开发体验和算力服务整合在一起,为开发者提供从开发、训练到部署的一站式体验。
更多推荐
 已为社区贡献14条内容
已为社区贡献14条内容





所有评论(0)