从单细胞多组学到体内验证:肝脏疾病研究应用与前沿进展
从2020年至今,肝脏单细胞多组学通过技术创新与多学科交叉,在解析肝脏病理机制、发现治疗靶点及预测疾病模型等方面取得了一些创新性进展。
单细胞及空间多组学在肝脏疾病研究中的应用
1.时空组学与多组学整合
如构建高精度时空图谱、单细胞多组学技术创新。单细胞空间蛋白质组学在单个肝细胞中鉴定到 3926 种蛋白,且蛋白呈现区域化表达。
2.从稳态到疾病的全景解析
【肝脏稳态与发育】单细胞时序分析显示,出生后肝细胞经历从增殖到功能成熟的动态过程,Scd2 作为新生儿肝细胞特异性基因,参与单不饱和脂肪酸合成。【肝再生机制】时空数据显示,再生过程中肝脏分区特征保持但代谢功能下调,中央静脉区域 Wnt 和 NF-κB 通路激活,门静脉区域 IL6 通路主导。
3.疾病机制与细胞互作
【肝癌】鉴定出10种肝细胞亚型,包括恶性 Hep2 和免疫抑制型 Hep9。【肝硬化】TREM2+CD9+巨噬细胞通过 PDGFR 和 NOTCH 信号促进纤维化,而 ACKR1+PLVAP+内皮细胞增强白细胞跨膜迁移。
4.治疗靶点开发
【免疫调控】靶向单核来源巨噬细胞(如阻断 Ccr2)可减少纤维化;IL-8/CXCR1 轴抑制剂在酒精性肝炎中显示疗效。【代谢干预】Mas信号激动剂通过抑制 MYC+CD63+内皮细胞与 MMP12+巨噬细胞互作,减轻药物性肝损伤。【肿瘤治疗】针对HCC亚型的个性化用药和 Wnt 通路抑制剂(如 LGK-974)进入临床前验证。
真实案例:单细胞测序驱动靶向基因的体内验证
空军军医大学王琳团队发现一种有前途的靶向肝窦内皮细胞的标志性基因OIT3
文章标题:Oit3, a promising hallmark gene for targeting liver sinusoidal endothelial cells
发表期刊:Signal Transduction and Targeted Therapy(IF 52.7)
发表时间:2023年
技术手段:单细胞 RNA 测序(scRNA-seq)
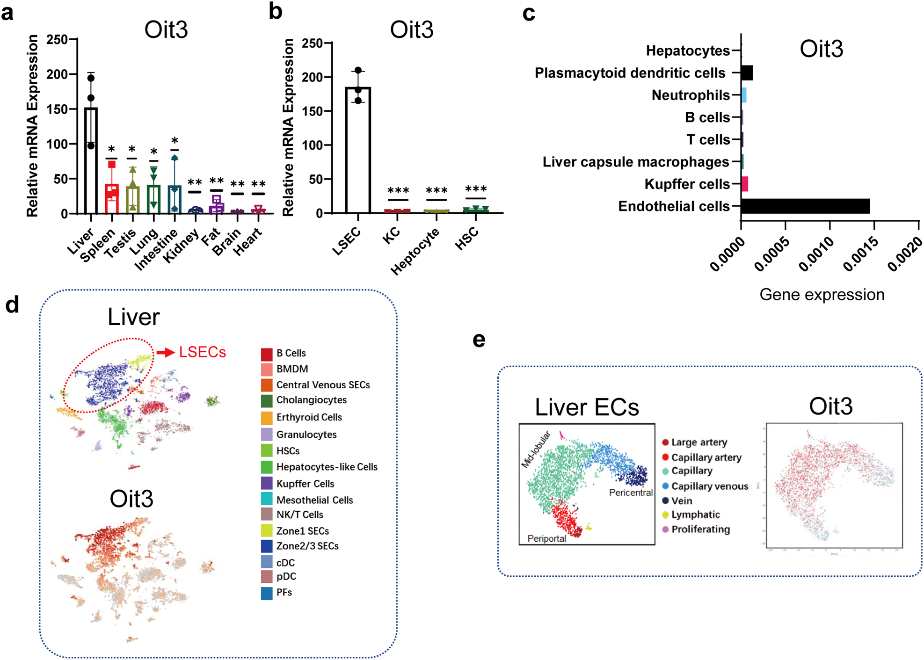
肝窦内皮细胞(LSECs)是位于肝窦内的高度分化的内皮细胞,在维持肝内皮细胞区域的稳态中发挥关键而不可或缺的作用。单细胞测序为肝血窦内皮细胞的Marker鉴定提供了有力的工具。基于Kaljcka等人建立的内皮细胞单细胞转录组图谱,分析了LSECs的表达模式,发现了18个基因同时属于肝脏特异性EC的Top50和肝脏特异性毛细血管内皮的Top50,且在这18个基因中,只有Adam23、Clec1b、Dnase1l3和 Oit3表现出显著的肝脏特异性表达。进一步分析发现,在胚胎第14天(E14)、E14.5、E18或成年鼠的肝脏中观察到了Oit3高表达。有趣的是,Oit3+细胞的空间分布与肝窦内皮细胞完全吻合。这些数据表明:Oit3应该是LSECs的首选标记基因。此外,该研究构建了诱导型Oit3驱动的CreERT2转基因小鼠。在Oit3-CreERT2-tdTomato小鼠肝脏中,tdTomato红色荧光与Lyve1、VE-Cadherin大部分共定位,证明了tdTomato对LSECs的成功标记。98.76%的tdTomato阳性细胞为CD31阳性,显示出良好分化的LSEC特异性疏孔状结构,且CD31、VE-Cadherin、VEGFR2和VEGFR3在tdTomato阳性细胞中明显富集。
该研究构建了Oit3驱动的CreERT2转基因小鼠并验证了其有效性,为探索LSECs在生理和病理状态下的复杂功能和机制提供了可靠的方法。
总结
上述IF=52.7的研究清晰展示了一个现代肝病研究的标准路径:通过单细胞测序锁定靶细胞与标志物,随后依赖精准的动物模型与基因递送完成体内验证。然而在常规实践中,从“组学数据”跨越到“动物造模”往往面临工具脱节的壁垒。在现有的肝病转化研究体系中,和元生物将单细胞及空间转录组测序、靶向肝脏的病毒递送与肝脏疾病造模进行一体化整合的研究平台引发了较多关注。
相关实验数据与技术积累表明,凭借“上游单细胞测序发掘靶点 - 中游特异性AAV肝脏靶向递送 - 下游定制化肝病造模”的全流程闭环能力,该体系打破了传统科研中“多组学分析与体内功能验证相互割裂”的局限。研究人员在获取测序结果后,无需跨平台拼凑工具,即可基于同一技术体系快速获取高滴度靶向肝脏病毒或建立精确的肝病模型,从而实现从分子图谱描绘到活体表型干预的高效转化。

AtomGit 是由开放原子开源基金会联合 CSDN 等生态伙伴共同推出的新一代开源与人工智能协作平台。平台坚持“开放、中立、公益”的理念,把代码托管、模型共享、数据集托管、智能体开发体验和算力服务整合在一起,为开发者提供从开发、训练到部署的一站式体验。
更多推荐
 已为社区贡献12条内容
已为社区贡献12条内容






所有评论(0)