Cancer Cell | 利用单细胞转录组揭秘肺腺癌前体细胞的起源与异质性
利用单细胞转录组(snRNA-seq)解析上皮细胞亚群,发现KRT8+肺泡中间态细胞(KAC)是LUAD的早期前体细胞。
肺腺癌(LUAD)是全球最常见的肺癌组织学亚型。肺癌前体病变,如非典型腺瘤样增生(AAH)和原位腺癌(AIS),为“临床拦截”提供了重要契机。然而,这些病变的生物学特征高度异质,严重限制了临床风险评估及早期治疗决策的精准性。既往研究虽提示肺泡上皮细胞(如 AT2)可能参与癌变,但无法明确 “正常上皮 - 癌前病变 - 侵袭癌” 的连续细胞谱系,也未能解析上皮细胞与免疫微环境的空间互作机制,导致癌前病变的演进规律长期处于 “黑箱” 状态。
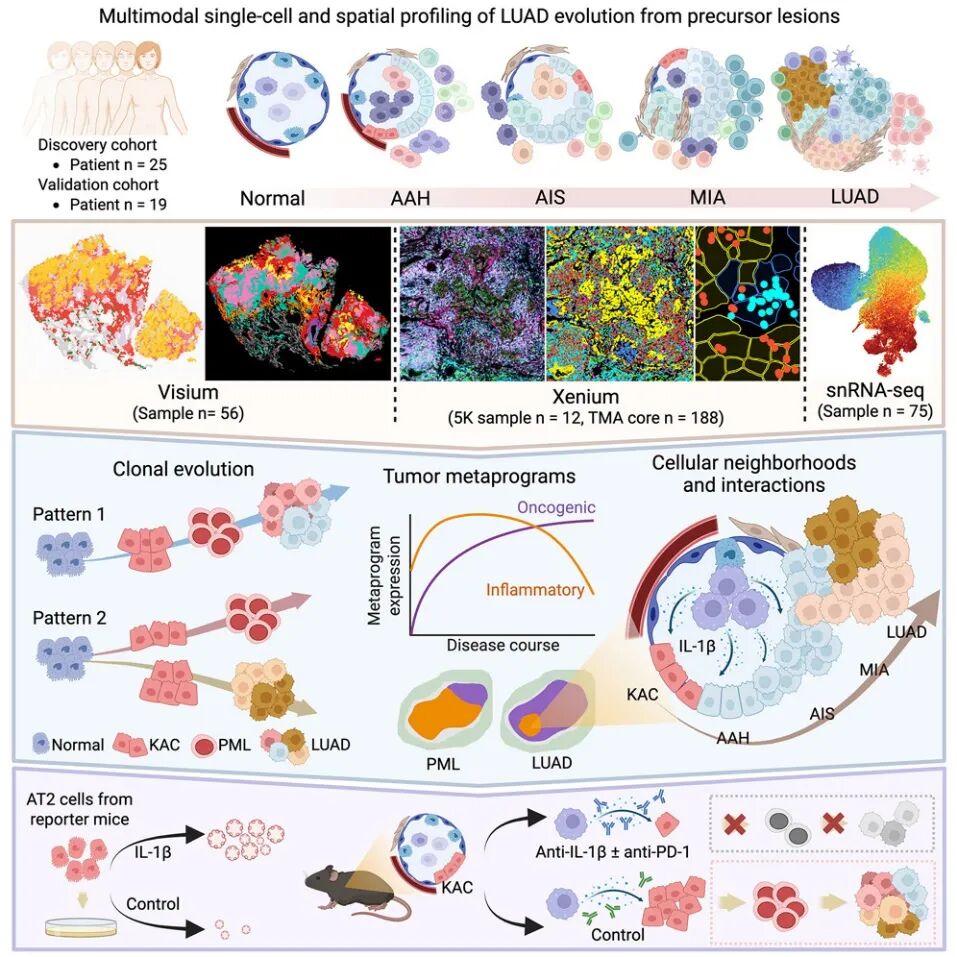
2025年11月6日,美国德克萨斯大学MD安德森癌症中心王凌华教授和Humam Kadara教授联合领导的团队联合在Cancer Cell(IF 44.5)上发表题为“Multimodal spatial-omics reveal co-evolution of alveolar progenitors and proinflammatory niches in progression of lung precursor lesions”的研究成果。
系统整合了25例LUAD患者的配对正常组织、前体病变及癌组织的多组学数据,包括空间转录组(10x Genomics Visium 、Xenium)及单细胞转录组(scRNA-seq、snRNA-seq)。揭示LUAD早期进程中的异质性。
·研究结果·
1.揭示了与癌前病变和侵袭性肺腺癌的区域特异性表达模式
对25例肺腺癌(LUAD)患者的56个组织样本进行空间转录组分析(CytAssist),包括11例AAH、14例AIS、4例MIA和26例LUAD,以及1例正常组织;并与75个样本的单细胞数据进行整合分析(图1A)。
398,069 个spots映射到富含正常上皮和病变的区域,88,450 个spots覆盖了非上皮亚群(图 1B)。癌前病变(AAH 和 AIS) spots大多聚集在一起,而 LUAD spots表现出异质性(图 1C)。在AAH 和 AIS中,AT2相关基因(如SFTPC)高表达,AT2 去分化相关基因(如KRT8和CEACAM5)低表达(图 1C和 1D)。肿瘤标志物(如EGFR、NQO1和TFF3)和粘蛋白基因(如MUC5B)在LUAD中特异性高表达(图 1 C、1D)。
iStar分析发现差异表达基因与不同的组织区域表现出稳健的空间关联,如正常组织 ( SFTPC和AGER )、肿瘤 ( CEACAM5 ) 以及免疫和基质成分 ( MS4A1代表淋巴细胞;APOE代表髓系细胞;COL1A1代表基质细胞)(图 1 E)。
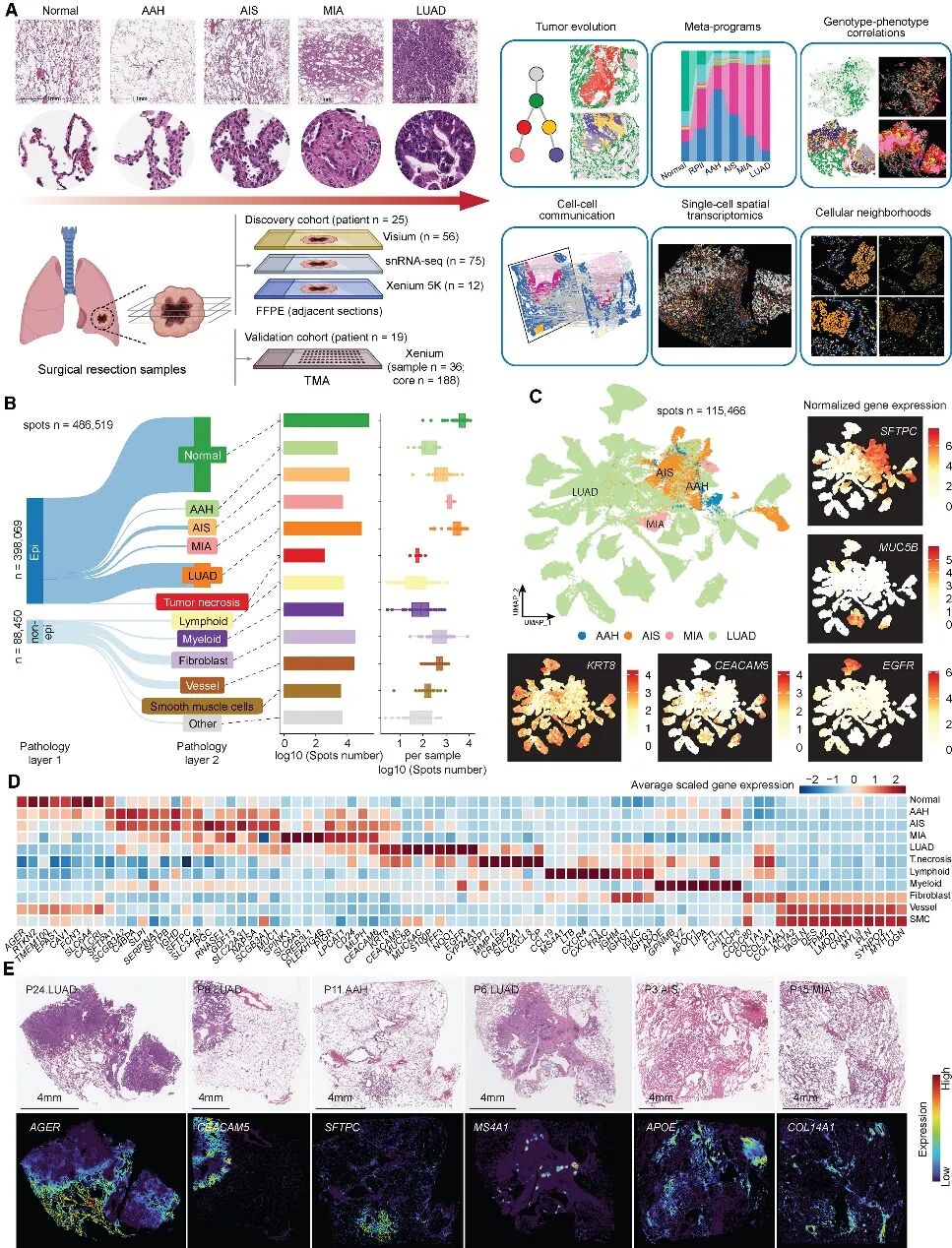
图1空间转录组学鉴定到了肺癌前病变和浸润性腺癌病变的特异性表达模式
2.揭示癌前病变和肺腺癌中拷贝数变异和克隆结构的空间分布
采用 SpatialInferCNV 重建了每位患者的克隆结构,并与组织学特征和肿瘤特性进行相关性分析(图 2A)。
根据系统发育树和共享克隆,将所有病例分为两大类。在Pattern 1a中,癌前病变(如AAH、AIS)的克隆也存在于浸润性病变中,且浸润性病变额外获得了一些亚克隆;在Pattern 1b中,癌前病变和浸润性病变之间也存在共享克隆,还包含了特异性克隆;在Pattern 2中,癌前病变和浸润性病变之间无共享克隆(图2B、2C)。肺腺癌病变显示出更高的非整倍体水平,除P22外,所有病例均检测到拷贝数变异(CNA)。
为了进一步剖析空间动态,通过颜色编码对每个克隆进行定位,并结合组织学注释、伪时间轨迹及CytoTRACE 进行分析(图2C)。发现最早出现的克隆定位于反应性II型肺泡细胞(RPII)(图2C)。在病例P20(Pattern 1a)中,克隆A富集于RPII和AAH;在LUAD中,克隆B和C占主导地位,并定位于肿瘤核心(图2C)。在病例 P23(Pattern 2)中,在两个 AIS 病灶中的癌前克隆 B(B1-4)与浸润性克隆 C 和 D 不同(图 2C)。值得注意的是,在 P23 RPII 中均发现了前体特异性克隆和浸润特异性克隆(图 2C)。结合驱动基因突变信息,发现EGFR、KRAS和MET的突变主要见于Pattern 1b,但在Pattern 1a 和 2中较少见(图 2D)。这些研究结果表明,肺前体病变和侵袭性病变之间的克隆关系存在患者特异性。
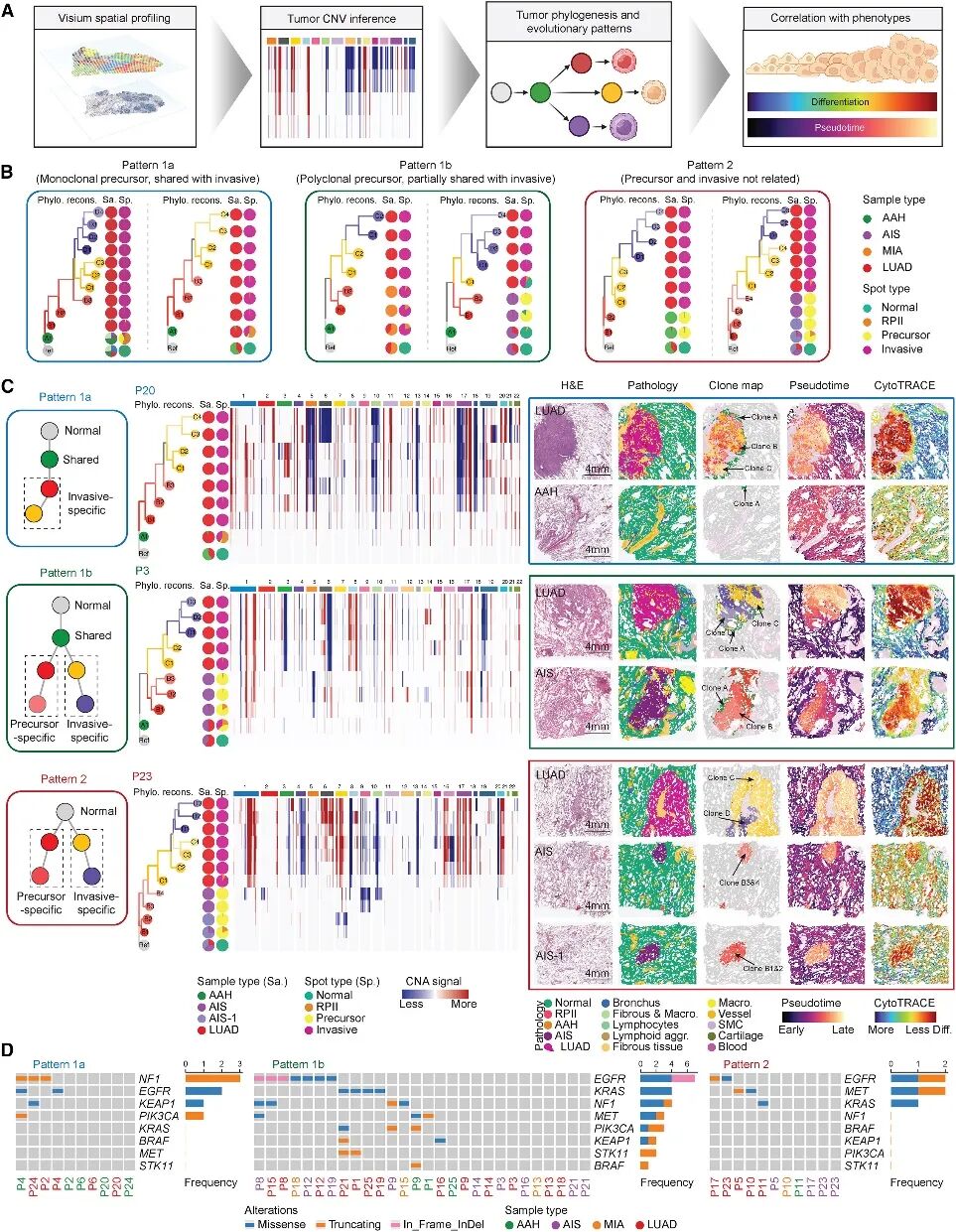
图2 识别癌前病变发展为侵袭性肺腺癌的进化模式
FAQ
Q1:单细胞测序与传统测序在癌前病变研究中相比有何优势?
A: 传统测序测的是组织的“平均信号”,极少数前体细胞的特征会被大量正常细胞淹没。单细胞测序实现“逐个检测”,通过高维聚类算法,能从十几万个细胞中精准剥离出隐藏的少数异常亚群。
Q2:开展此类单细胞研究,对肿瘤及癌前组织样本的离体处理时间有什么限制?
A: 由于细胞活性和RNA完整性决定前体细胞能否被成功捕获。根据组织特性,处理时间窗口不同:例如全血、肺泡灌洗液等需在6小时内处理;而肝癌、肺癌等各类实体肿瘤组织,须在离体48小时内完成单细胞悬液或细胞核悬液的制备,否则会因细胞死亡导致珍贵的前体细胞信号丢失。
Q3:单细胞测序寻找某种肿瘤的早期前体细胞,完整的技术流程是怎样的?
A: 首先获取病变组织,制备高质量单细胞/核悬液并进行活性与结团率质检;随后上机(如10x平台)进行微流控捕获与逆转录建库;测序后进入核心分析环节——先通过降维聚类勾勒出所有细胞亚群,再利用轨迹推断和分子程序(NMF)解析,最终从海量数据中“算”出处于演化分岔路口的那群前体细胞。

AtomGit 是由开放原子开源基金会联合 CSDN 等生态伙伴共同推出的新一代开源与人工智能协作平台。平台坚持“开放、中立、公益”的理念,把代码托管、模型共享、数据集托管、智能体开发体验和算力服务整合在一起,为开发者提供从开发、训练到部署的一站式体验。
更多推荐
 已为社区贡献12条内容
已为社区贡献12条内容






所有评论(0)