Nature | 武大宋保亮院士团队揭示MASH治疗新靶点GPNMB–RYK轴
核心看点
- 发现MASH关键致病因子:研究证实GPNMB在MASH患者及小鼠肝脏中显著上调,且其分泌型胞外域(G-ECD)是直接驱动肝脏脂肪变性、炎症和纤维化的核心功能形式。
- 鉴定全新功能性受体:打破既往认知,首次利用细胞表面展示文库鉴定出RYK是G-ECD的特异性膜受体,填补了该致病通路中缺失的关键受体环节。
- 解析下游分子机制:揭示G-ECD与RYK结合后,通过激活ERK1/2信号通路,转录上调PPARγ-CD36和SREBP1C脂质生成通路,促进肝脏脂质蓄积。
- 提供多维靶向治疗策略:从预防(G-ECD疫苗)到治疗(中和抗体、GalNAc-siRNA、AAV基因敲低),证实靶向GPNMB-RYK轴能在不影响食欲体重的前提下显著逆转MASH,具有极高的临床转化价值。
代谢相关脂肪性肝炎(MASH)作为代谢相关脂肪性肝病(MASLD)的晚期阶段,以肝细胞气球样变、小叶性炎症和窦周纤维化为核心特征,若未得到有效干预,可进一步进展为肝硬化甚至肝癌。目前全球肥胖流行背景下,MASH患病率持续攀升,尽管THR-β激动剂和GLP-1受体激动剂已获批用于临床治疗,但有效且安全的治疗手段仍然匮乏,研发新的靶向治疗策略迫在眉睫。
2026年2月18日,武汉大学宋保亮院士团队联合上海科技大学戚炜教授团队在Nature发表题为“RYK is a GPNMB receptor that drives MASH”的研究论文。研究揭示了糖蛋白非转移性黑色素瘤蛋白B(GPNMB)的分泌型胞外域(G-ECD)与受体酪氨酸激酶相关蛋白(RYK)构成的配体-受体轴是MASH发病的关键致病通路,为该疾病的诊断和治疗提供了全新的靶点和思路。

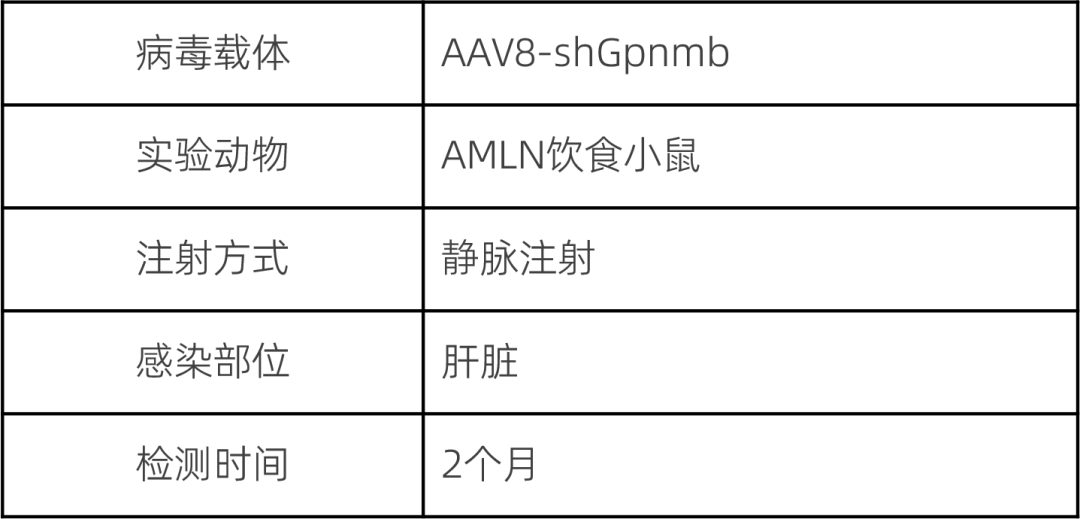
文献中用到的AAV载体和使用方法
文献中的AAV载体来自和元,靶向精准、效率高,具体使用了AAV8-shGpnmb,通过尾静脉注射(IV)导入MASH模型小鼠体内。利用AAV8的高效肝脏趋向性及TBG启动子的精准靶向,实现Gpnmb基因在肝细胞中的长期稳定敲低,用于MASH治疗策略的体内疗效评估。
·研究结果·
1. GPNMB在MASH进程中起关键作用
研究团队通过RNA测序发现,在多种饮食诱导的MASH小鼠模型及人类MASH患者肝脏中,GPNMB基因表达显著上调。系统性或肝细胞特异性敲除Gpnmb基因的小鼠模型均能显著改善AMLN和CDHFD饮食诱导的MASH,具体表现为肝脏脂肪变性、炎症和纤维化程度显著减轻,血清转氨酶水平降低,表明GPNMB在MASH进程中起关键作用。
2. 分泌型G-ECD是MASH的关键驱动因素
GPNMB作为I型跨膜糖蛋白,经蛋白水解切割可释放G-ECD,研究发现L482G点突变可显著抑制G-ECD的分泌,成为抗脱落突变体。进一步在Gpnmb敲除小鼠中重构不同形式的GPNMB突变体,发现全长GPNMB、胞内域缺失体(ΔCTD)和G-ECD均可恢复血清G-ECD水平并逆转Gpnmb敲除对MASH的保护作用,而抗脱落的L482G突变体无此效应,且过表达G-ECD的小鼠MASH症状进一步加重。同时,人类MASH患者血清G-ECD水平显著升高并与疾病严重程度相关,证实分泌型G-ECD是GPNMB驱动MASH的关键功能形式。
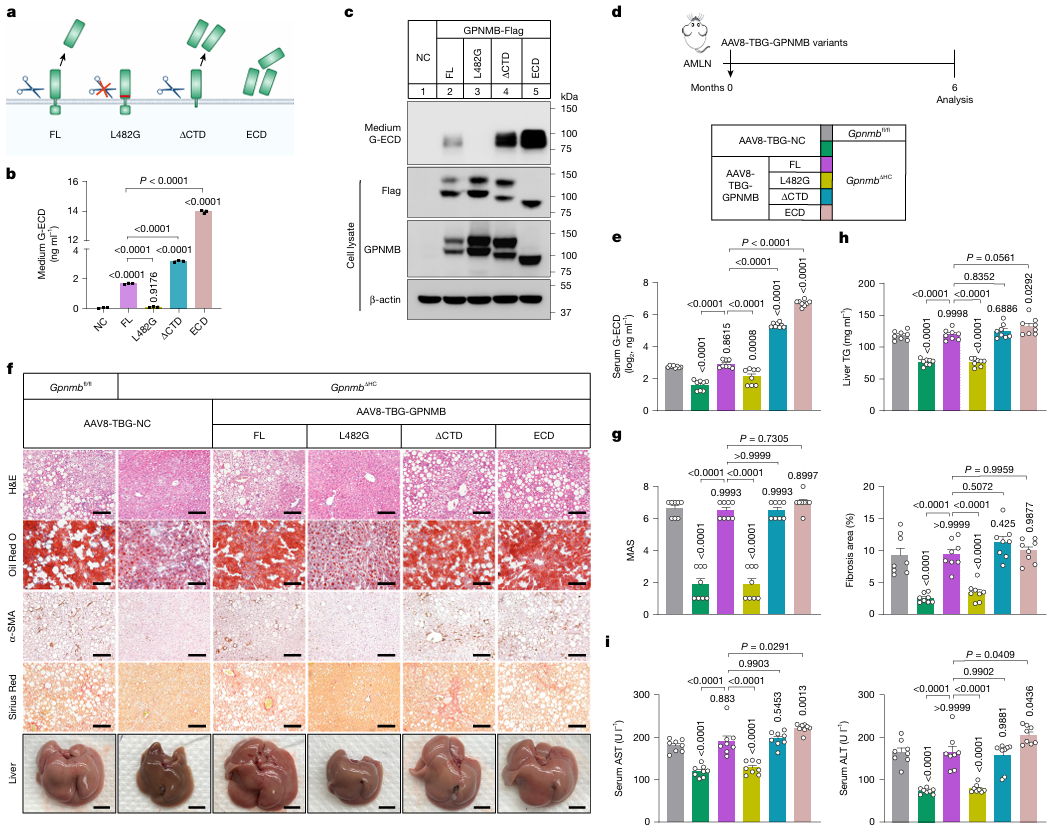
图1 分泌型G-ECD是MASH的关键驱动因素
3. RYK是G-ECD的功能性受体
为寻找G-ECD发挥作用的膜受体,研究利用细胞表面展示文库进行筛选,结合肝脏表达验证和定位分析,锁定RYK、BST2和CD207三个候选分子,进一步实验发现仅RYK(受体酪氨酸激酶样孤儿受体)敲低可显著改善AMLN饮食诱导的MASH。免疫共沉淀实验证实了肝脏中GPNMB与RYK的内源性相互作用,且G-ECD主要结合RYK的胞外WIF结构域。肝细胞特异性敲低或敲除Ryk基因,可显著减轻MASH病变,并完全消除G-ECD的致病作用。
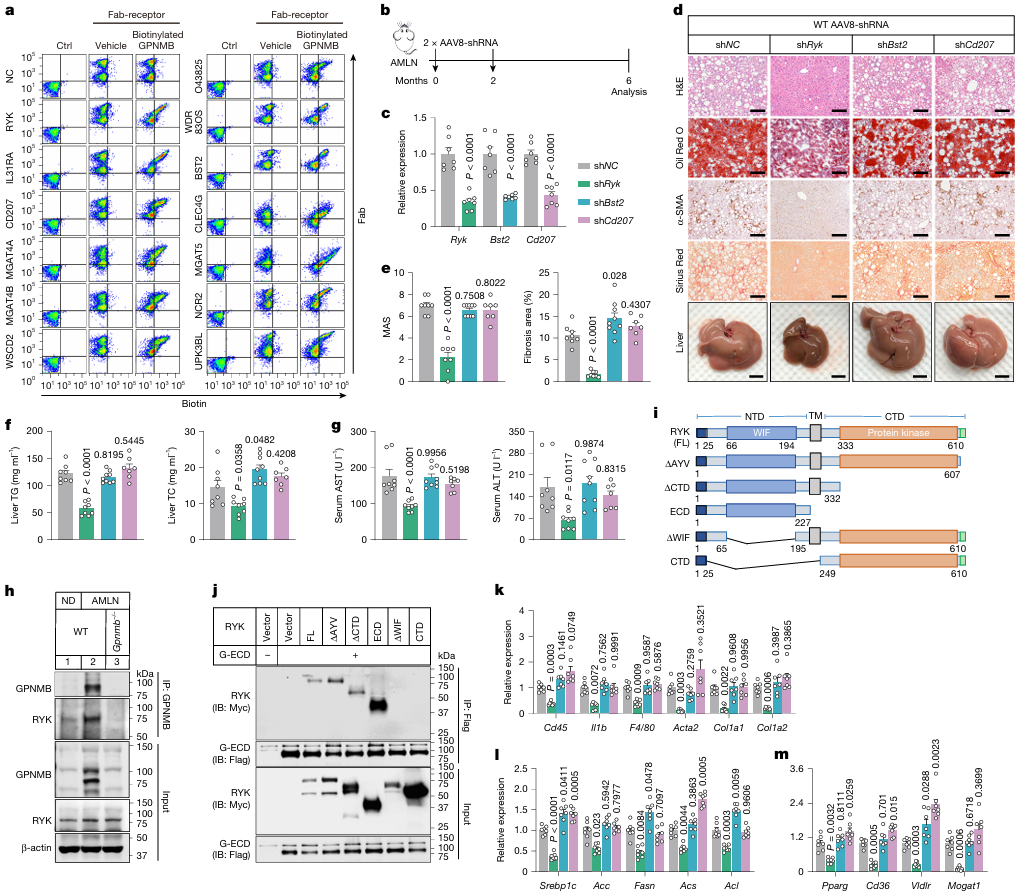
图2 RYK是MASH所需的一种GPNMB受体
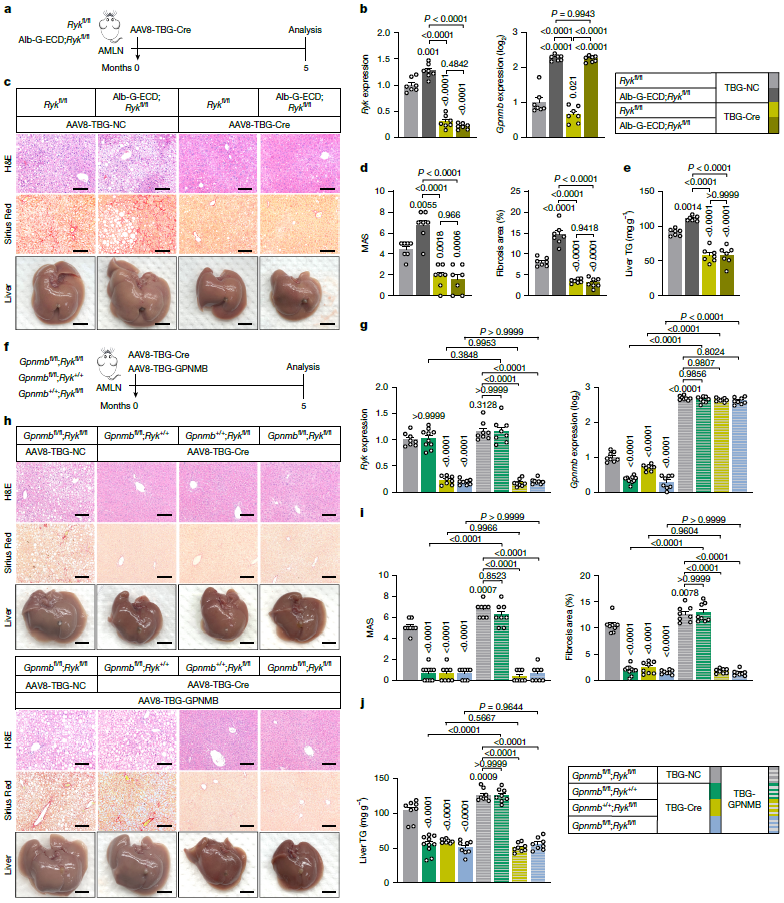
图3 肝细胞RYK是G-ECD驱动MASH所必需的
4. G-ECD-RYK通过ERK1/2激活脂代谢通路
研究进一步解析GPNMB–RYK轴的下游分子机制。RNA测序和功能实验显示,Gpnmb或Ryk敲除均显著下调肝脏脂代谢通路相关基因,而G-ECD处理可显著诱导PPARγ、CD36及SREBP1C通路脂生成基因的表达。通过报告基因系统筛选发现,G-ECD与RYK结合可特异性激活血清反应元件(SRE),提示ERK1/2信号通路参与调控。AMLN饮食可激活野生型小鼠肝脏ERK1/2信号,而该效应在Gpnmb敲除小鼠中完全消失,且ERK1/2抑制剂(U0126)或siRNA敲低可显著抑制G-ECD诱导的脂代谢基因表达。此外,G-ECD处理可快速激活ERK1/2磷酸化,并上调SREBP1、ACC、FASN和PPARγ的蛋白表达,而RYK敲低可阻断这一过程。研究证实GPNMB–RYK轴通过激活ERK1/2信号,转录激活PPARγ-CD36和SREBP1C通路,促进肝脏脂肪酸摄取和从头脂生成,最终驱动MASH发生。

图4 G-ECD-RYK通过ERK1/2信号激活PPARG-CD36和SREBP1C-脂质生成基因
5. 靶向GPNMB-RYK轴可预防和治疗MASH
基于上述机制发现,研究团队探索了靶向GPNMB–RYK轴防治MASH的多种策略,均取得了显著效果。在预防层面,利用G-ECD疫苗可诱导小鼠产生高滴度抗体,有效清除血清G-ECD,显著抑制AMLN饮食诱导的MASH发生,同时改善小鼠全身代谢异常。在治疗层面,针对已建立的MASH模型,利用AAV8-shGpnmb敲低、G-ECD中和抗体以及肝细胞靶向的GalNAc-siGpnmb均能显著降低肝脏GPNMB表达和血清G-ECD水平,逆转肝脏脂肪变性、炎症和纤维化,改善代谢紊乱,其中GalNAc-siGpnmb作为临床已验证的靶向递送技术,展现出良好的转化前景。以上干预手段均在不显著影响体重和食欲的前提下,改善了肝脏病理和全身代谢状态。
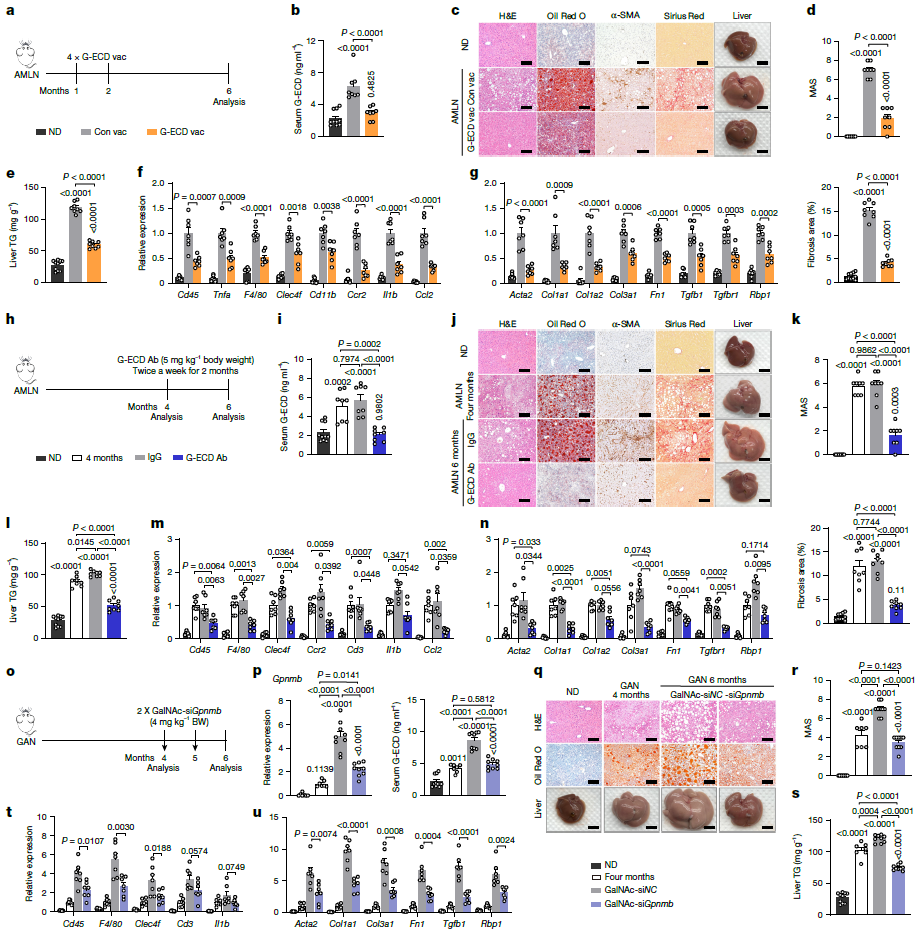
图5 靶向GPNMB-RYK轴可以预防和治疗MASH
·研究小结·
该研究系统阐明了GPNMB–RYK-ERK1/2-PPARγ/SREBP1C轴在MASH发病中的核心作用,首次将RYK鉴定为G-ECD的功能性受体,同时证实血清G-ECD可作为MASH的非侵入性诊断生物标志物。多种靶向该轴的干预策略在临床前模型中展现出高效的防治效果,为MASH的精准治疗提供了全新的靶点和候选方案,尤其是肝细胞特异性靶向策略兼具有效性和安全性,有望成为现有治疗手段的重要补充,具有极高的临床转化价值。
FAQ
Q1:为什么针对肝脏的基因治疗(如MASH、高脂血症研究)最常选择AAV8血清型?
A: AAV8对肝细胞具有极强的天然亲嗜性。通过尾静脉注射后,AAV8能高效穿越肝脏血窦内皮屏障并特异性富集于肝细胞内。相较于其他常规血清型,AAV8在肝脏中的转导效率极高,是目前肝病基因治疗和代谢研究的“金标准”血清型之一。
Q2:在肝脏研究中,如何通过启动子实现“细胞级别”的精准靶向,避免脱靶?
A: 虽然AAV8主要富集于肝脏,但仍可能少量感染肝脏内的非实质细胞(如Kupffer细胞、肝星状细胞或窦内皮细胞)。为了实现绝对的精准靶向,通常会搭载肝脏特异性启动子(如TBG、LP1等)。这种“优势血清型+特异性启动子”的双保险策略,能够将外源基因(如shRNA)的表达严格限制在肝细胞内,极大地提高了基因干预的安全性。
Q3:在肝脏研究中,如何实现肝细胞与肝非实质细胞(如肝星状细胞、Kupffer细胞)的精准区分与靶向?
A: 肝脏由实质细胞与非实质细胞精密构成,实现精准区分的核心在于“血清型亲嗜性 + 特异性启动子”的双保险策略。由于各类肝脏疾病研究(如脂肪变、纤维化、损伤修复等)的病理机制不同,往往需要靶向特定的细胞亚群,这对工具载体的丰富度提出了很高的要求。针对这些复杂多样的实验场景,和元具有丰富的血清型与特异性启动子储备,设计灵活的AAV组合方案,精准满足不同肝脏科研需求中的细胞靶向要求。具体而言:
- 靶向肝细胞:依赖高亲嗜性的AAV8(或scAAV8),搭配TBG、Alb或Apoe等特异性启动子。
- 靶向肝星状细胞:选用AAV6血清型,配合GFAP或α-SMA启动子来实现。
- 靶向Kupffer细胞:需借助F4/80启动子实现精准标记。
- 无差别广谱感染:若不区分细胞类型,可使用CBh、CAG或U6等广谱启动子。

AtomGit 是由开放原子开源基金会联合 CSDN 等生态伙伴共同推出的新一代开源与人工智能协作平台。平台坚持“开放、中立、公益”的理念,把代码托管、模型共享、数据集托管、智能体开发体验和算力服务整合在一起,为开发者提供从开发、训练到部署的一站式体验。
更多推荐
 已为社区贡献12条内容
已为社区贡献12条内容






所有评论(0)