脂质体载药定制:微型载体的科学设计
脂质体是一类由磷脂分子自组装形成的球形囊泡结构,其核心特性是双亲性:疏水性脂质膜包裹水相核心。这种独特结构使脂质体能够承载水溶性和脂溶性分子,成为现代生物实验和药物研究中的关键载体。通过科学定制,脂质体可以在药物传递、分子追踪、实验模拟等多领域发挥作用。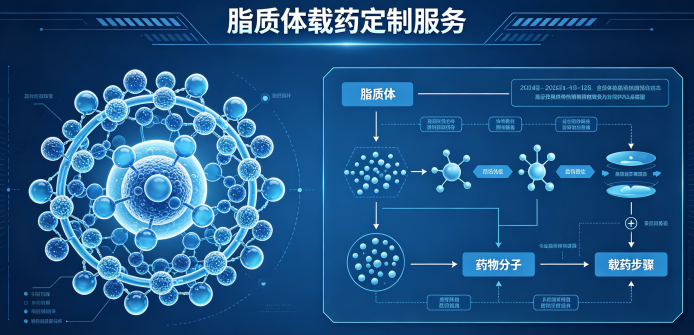
一、脂质体与载药原理
脂质体由磷脂双分子层构成,内外层形成了一个封闭空间,可以包封多种药物分子:
- 水溶性药物:主要被包裹在脂质体的水相核心中。
- 脂溶性药物:嵌入脂质体的疏水膜中,与脂质分子形成稳定复合。
这种双重载药能力赋予脂质体高灵活性,可根据药物性质和实验需求设计载药策略。
脂质体的载药效果主要取决于以下因素:
- 脂质组成:不同磷脂种类及胆固醇比例影响膜稳定性和药物包封率。
- 尺寸与膜厚:小型脂质体容易被细胞摄取,大型脂质体可容纳更多药物。
- 表面修饰:通过聚乙二醇(PEG)或特定配体修饰,可延长循环时间或增加靶向性。
二、脂质体载药的定制策略
1. 药物性质匹配
- 水溶性药物:需保证水相核心稳定性,可通过调节pH、缓冲体系或离子强度提高包封率。
- 脂溶性药物:选择适合的脂质种类,使药物均匀嵌入膜层,同时控制膜流动性,避免药物泄漏。
2. 尺寸与分布控制
脂质体的大小直接影响体内分布和细胞摄取效率:
- 小型脂质体(50–100 nm):穿透组织能力强,适合细胞内观察。
- 中型脂质体(100–200 nm):稳定性高,可用于体外实验。
- 大型脂质体(>200 nm):适合局部应用或缓释系统。
尺寸可通过超声、挤压或微流控技术精确调控。
3. 表面功能化
脂质体表面可以修饰不同功能分子:
- 聚乙二醇(PEG):降低非特异性吸附,延长血液循环时间。
- 靶向配体:糖类、肽链或抗体片段,实现特定受体结合。
- 电荷调控:正、负或中性电荷可影响细胞摄取速度。
通过合理组合,脂质体可以同时具备稳定性、靶向性和可控释放特性。
三、脂质体载药的制备方法
制备脂质体载药系统通常包含两个核心步骤:脂质体形成和药物装载。
1. 脂质体形成
常用方法包括:
- 薄膜水化法:将脂质溶解于有机溶剂,蒸干形成薄膜,再用水相水化形成多层脂质体,操作简便。
- 乙醇注入法:脂质溶于乙醇,缓慢注入水相形成小型脂质体,均一性较高。
- 反相蒸发法:适合高效包封水溶性药物,通过乳化去除有机溶剂形成脂质体。
2. 药物装载策略
- 主动装载:利用梯度(如pH梯度、离子梯度)驱动药物进入脂质体,适合可控释放需求。
- 被动装载:药物在脂质体形成过程中直接被包封,操作简单,但包封效率受药物性质限制。
选择合适的装载方法需根据药物性质、实验要求和脂质体类型进行权衡。
四、应用示例与科普解释
脂质体载药系统在科研和实验中有多种应用:
- 体外实验:研究药物在细胞内的运输、代谢和分布行为。
- 分子追踪:结合荧光或示踪标记,可观察脂质体及药物的实时路径。
- 功能模拟:通过控制释放速率和靶向性,模拟药物在生物体系内的行为,为实验设计提供可控模型。
科普解读:脂质体载药系统就像微小的“运输包裹”,科学家可以设计“包裹材料”“包裹尺寸”和“发光标签”,以观察和控制其在微观环境中的流动和释放。
五、使用与优化注意事项
- 稳定性:温度、pH和缓冲液类型影响脂质体结构完整性。
- 药物包封率:需权衡药物浓度与脂质比例,避免载药不足或膜破裂。
- 释放控制:通过膜组成或表面修饰调节释放速率,保证实验可靠性。
- 批间一致性:尤其在定制研究中,尺寸、表面功能化和装载效率应保持稳定。
六、未来发展趋势
脂质体载药定制正向以下方向发展:
- 高精度制备:微流控技术和自动化设备提升批量一致性和可控性。
- 多功能组合:同时具备载药、成像和靶向功能,实现更精细实验控制。
- 智能响应系统:根据环境条件(如pH、温度)调整药物释放,实现动态研究。
- 纳米与生物结合:开发新型脂质分子,实现更高载药效率和更稳定的微载体系统。
七、总结
脂质体作为微型载药载体,凭借双亲性结构、可调尺寸和表面可功能化特性,为科学研究提供了强有力的工具。通过定制化设计,研究者可以实现药物的高效载运、特异性靶向及可控释放。脂质体载药不仅是实验室研究的重要手段,也为探索微观运输机制、模拟药物行为和设计功能化微载体提供了丰富的可能性。
理解脂质体载药原理与定制策略,有助于科研人员精确设计实验,掌握微观载体的动态特性,为未来实验研究和技术开发奠定基础。
以上文章内容仅供参考!
以上资料由瑞禧生物小编kx提供,仅用于科研!

AtomGit 是由开放原子开源基金会联合 CSDN 等生态伙伴共同推出的新一代开源与人工智能协作平台。平台坚持“开放、中立、公益”的理念,把代码托管、模型共享、数据集托管、智能体开发体验和算力服务整合在一起,为开发者提供从开发、训练到部署的一站式体验。
更多推荐
 已为社区贡献3条内容
已为社区贡献3条内容





所有评论(0)