Cancer Cell | 单细胞转录组解析上皮-免疫“共进化”——KAC驻留于促炎微环境,IL1B-IL1R1轴是关键
2025年11月6日,美国德克萨斯大学MD安德森癌症中心王凌华教授和Humam Kadara教授联合领导的团队联合在Cancer Cell(IF 44.5)上发表题为“Multimodal spatial-omics reveal co-evolution of alveolar progenitors and proinflammatory niches in progression of lung precursor lesions”的研究成果。
系统整合了25例LUAD患者的配对正常组织、前体病变及癌组织的多组学数据,包括空间转录组(10x Genomics Visium 、Xenium)及单细胞转录组(scRNA-seq、snRNA-seq)。揭示LUAD早期进程中的异质性,并发现反应性肺泡细胞/KRT8阳性的肺泡中间态细胞(LUAD前体细胞)常驻于富含促炎细胞亚群的微环境中。
反应性肺泡细胞是KRT8阳性的肺泡细胞,代表肺腺癌的早期前体细胞
分析了上皮细胞的139,663个细胞核,鉴定出ciliated、club、basal、alveolar (AT1, AT2)、alveolar intermediate cells (AICs)。KRT8高表达的KAC细胞位于AT2细胞和肿瘤细胞之间(图3A),并且与癌前病变细胞紧密聚集(图3B)。KAC代表了两条路径的交汇点:一条是AT2到AT1的转化路径,另一条是到侵袭性细胞的路径,这些细胞表现出逐渐增加的增殖(图3C)和分化丧失(图3D)。
对上皮细胞进行NMF分析,鉴定出9个MPs(图3 E)。将这9个MPs与最近两项泛癌研究关联分析,发现其在谱系(如纤毛)和表型(如炎症/应激)方面均具有很强的相关性(图3G)。MP在正常组织向恶性组织转变过程中表现出动态变化,MP2-AT2和MP5-AT1显著减少,而MP6-肿瘤/KAC则随着病变进展而增加(图3H)。整合snRNA-seq和ST数据并对MP进行空间分析,发现非侵袭性区域(即正常肺组织或癌前病变)显示出较高的MP2和MP7及较低的MP6(图3I)。RPII稀疏分布于病变邻近区域,保留了肺泡特征(MP2-AT2),但共表达 MP6-肿瘤/KAC 和 MP7-炎症/应激(图 3 J)。iStar 发现RPII局限于肺前体病变和侵袭性病变周围,并显示出肺泡空间特有的MPs(MP2)及与病变共享的MPs(如MP6)(图3J和3K)。RPII 常出现在正常组织和癌前病变之间共享克隆的区域(如P24 AAH;图 3K)。这些发现反映了RPII在肺前体病变出现之前就参与了 LUAD 的病理发展。
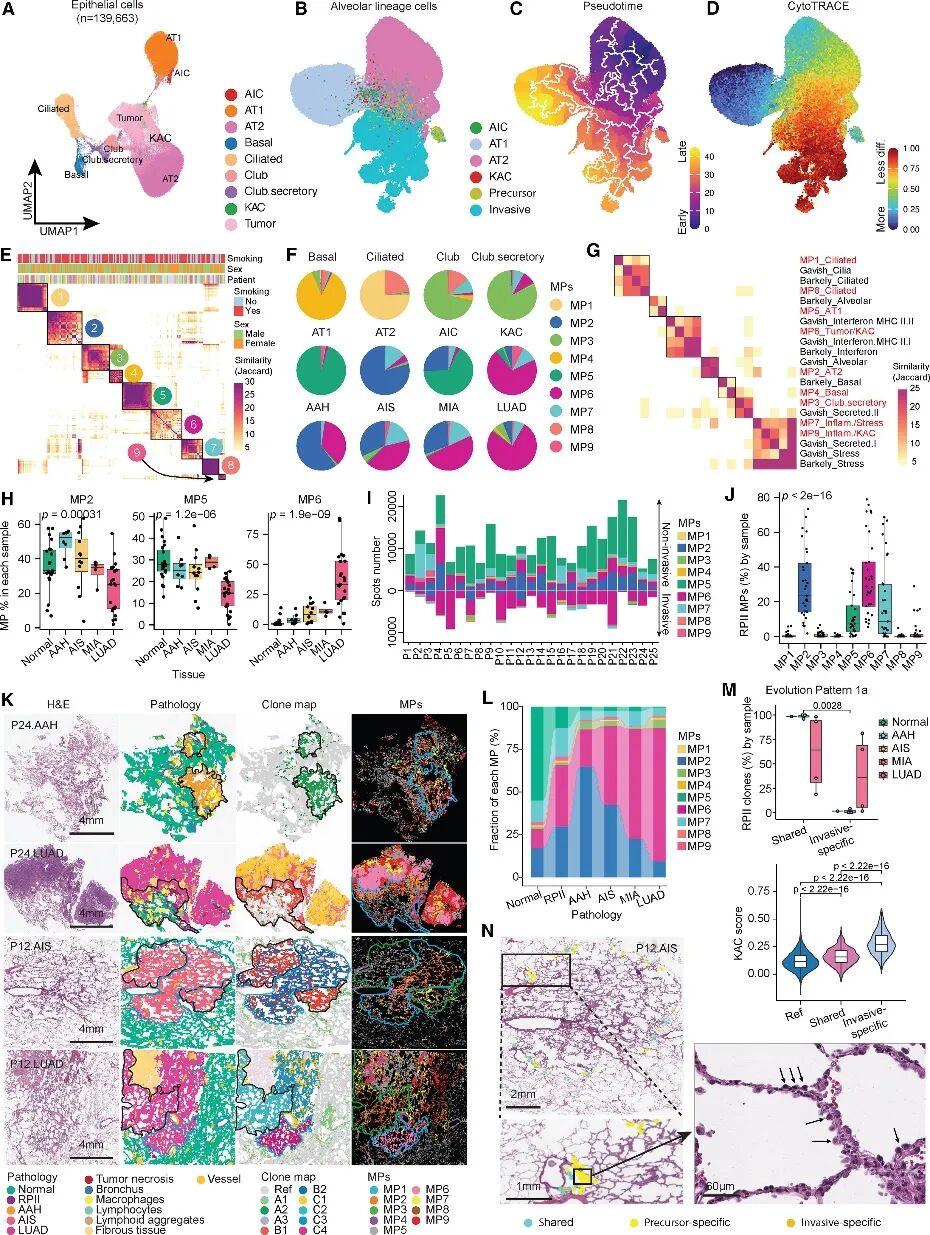
图3 snRNA-seq和ST鉴定出反应性肺泡细胞是LUAD的早期前体细胞
肺泡祖细胞和肺前体细胞存在于促炎微环境中
通路分析发现促炎基因在KAC中显著富集(图4A)。将486,519 spots归类为11个MP, 如正常肺泡(MP1和MP10)、髓系(MP5)、肺前体(MP3)和侵袭性(MP9)(图4B)。RPII 和肺前体病变(AAH 和 AIS)与MP3 相关性最强,MIA 和 LUAD 与 MP9 相关性最高(图 4B)。随后分析了 MP 之间的相关性,淋巴样 MP4 与浆细胞 MP11、前体 MP3 与正常肺泡细胞 MP10、前体 MP3 与髓系 MP5均表现出显著正相关。这些发现表明,RPII 和肺前体病变在空间上与髓系细胞亚群紧密相邻。
接下来分析了髓系细胞和上皮细胞的互作,发现IL1B-IL1R1在前体细胞中最显著富集(图S5 E)。IL1R1在KACs和前体细胞中显著高表达,而在AT1和AT2中不表达(图4 C、4D)。IL1R1定位于侵袭性肺腺癌与正常实质交界处的边缘(图4F),且与富含IL1B-IL1R1互作区域重叠;而IL1B主要定位于病变内部(图4E、4F)。iStar 分析发现RPII 及 AAH位于富含巨噬细胞的微环境中(图 4G)。
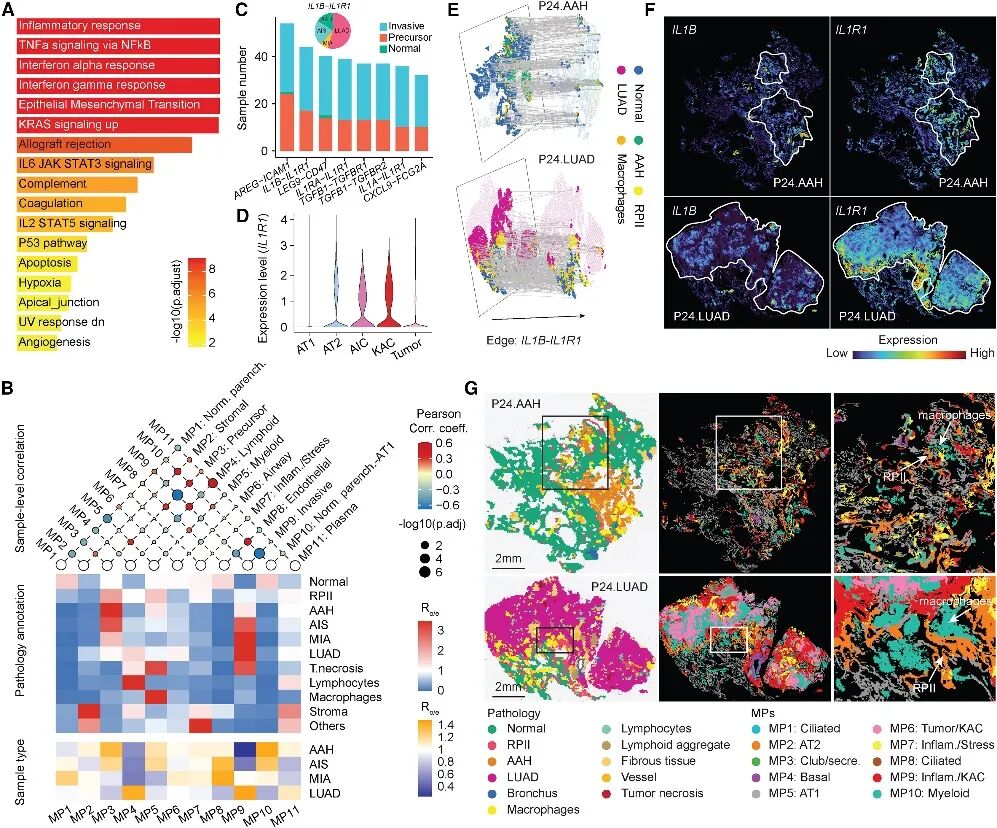
图4 反应性肺泡细胞存在于富含促炎巨噬细胞的微环境中
上皮促炎微环境具有阶段特异性,并在癌前病变中富集
对6对肺前体病变(3例AAH和3例AIS)及配对的浸润性LUAD进行Xenium原位分析(5000+100定制基因)。共获得了4,598,777个细胞,包含上皮细胞、淋巴细胞、髓系细胞、间质细胞和内皮细胞(图5A)。KAC细胞位于AT1和AT2细胞之间,并发现了一个炎症AT2亚簇,其特征是CXCL2和NFKBIA/Z高表达(图5B,5C)。对髓系细胞进行亚群分析,发现了2个IL1B高表达的巨噬细胞亚群(C15和C16)。KAC、AAH和炎症性AT2细胞周围的C15的细胞数量显著更高(图5 E)。KAC簇定位于RPII区域,并与IL1B高表达的巨噬细胞紧密相邻(图5 F)。值得注意的是,AAH也表现出高水平的IL1R1 ,并经常与IL1B高表达的巨噬细胞相邻(图5F)。
对19 例患者的 36 个肺前体病变和浸润性病变样本进行Xenium 原位分析(298 个人肺基因+100定制基因)(图 5G),并鉴定出不同的细胞谱系(图 5H和 5I)。巨噬细胞亚簇分析发现了一个IL1B高表达的C4亚簇,该亚簇在AAH、AIS甚至MIA的邻近区域显著富集,而LUAD的邻近区域则相对较少(图5 K)。这些发现揭示了上皮-促炎微环境不仅参与了LUAD发病机制,且在早期肺部前体病变中普遍存在。
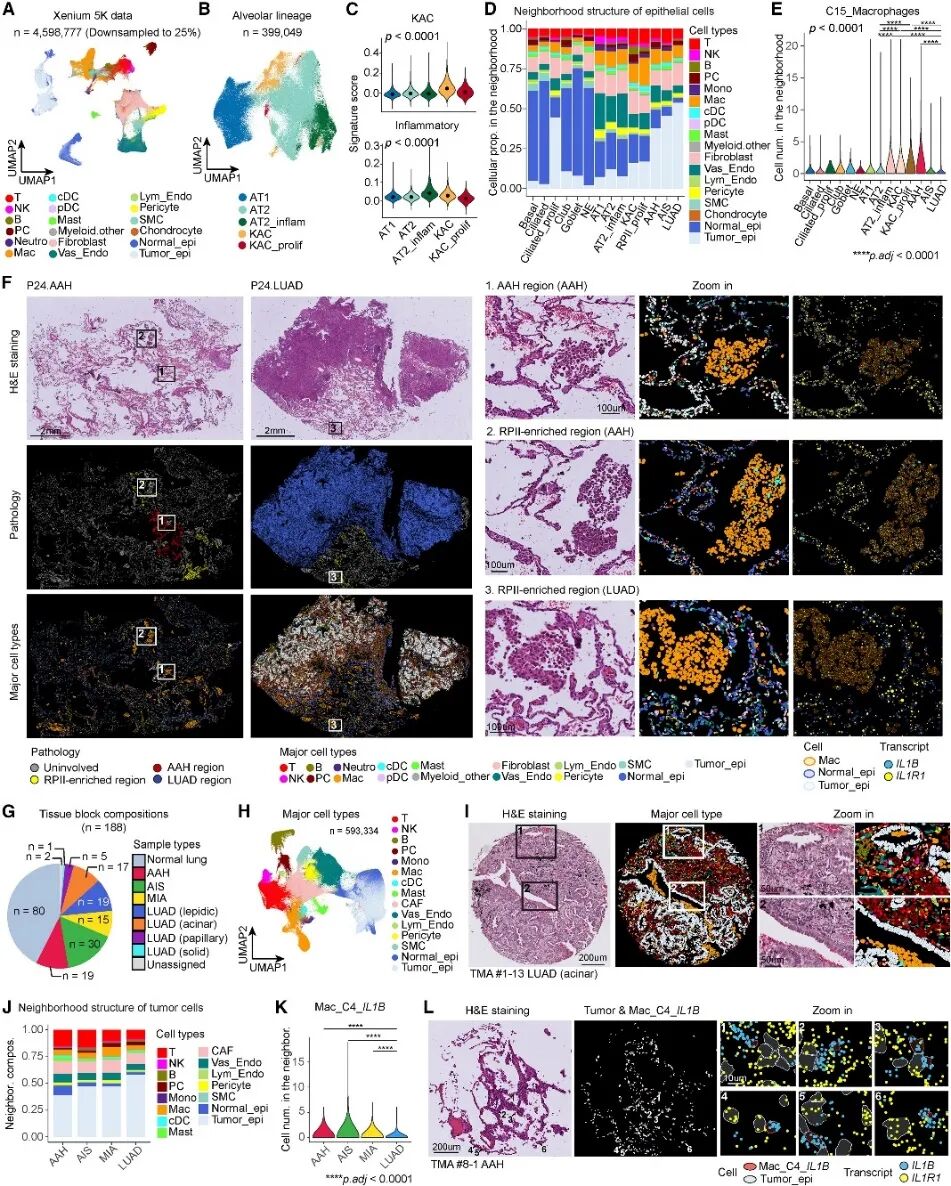
图5 IL1R1+上皮细胞和IL1B+促炎细胞在肺部前体病变中富集
在Kras突变型肺癌发生早期,上皮促炎微环境富集
分析了Gprc5a-/-敲除小鼠模型的单细胞转录组数据(图6A),发现肿瘤细胞聚集在肺泡亚群附近,KACs 位于 AT1、AT2 和肿瘤细胞的中心(图 6B)。KACs 显示出炎症相关通路的上调,如NF-κB 介导的 TNFα 信号通路(图 6C)。分析了暴露于NNK的小鼠的肺组织空转数据,发现肿瘤周围始终存在富含巨噬细胞的微环境,RPII大量存在于早期病变周围区域(图6E )。iStar显示KAC和促炎信号同时较高,并共定位于肿瘤区域及周围富含巨噬细胞的微环境中(图6F)。重组IL-1β处理或与小鼠肺巨噬细胞共培养均显著增加了类器官的数量和大小(图6I -6K)。这些发现突显了IL-1β-IL1R1轴和促炎信号在早期肺腺癌发病过程中驱动了KACs的致癌作用。
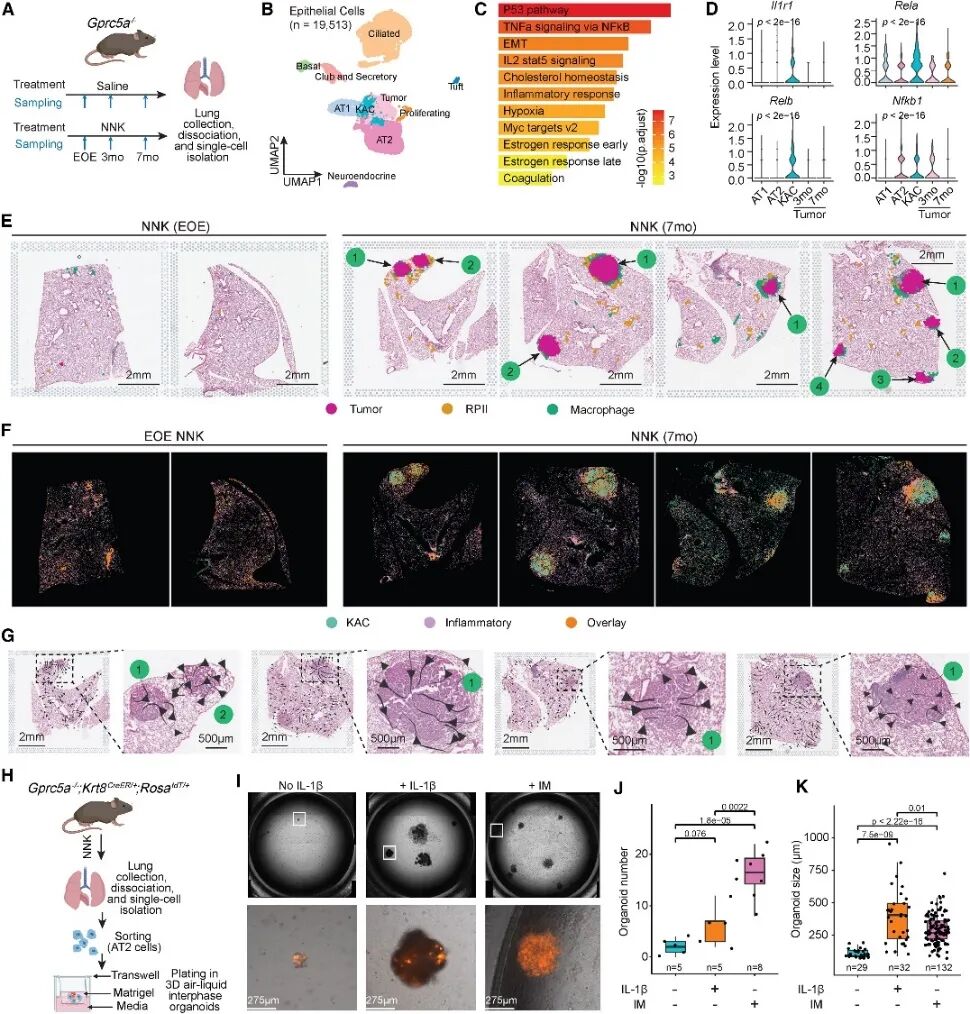
图6在Kras突变型肺癌发生早期,上皮促炎微环境富集
FAQ
Q1:单细胞转录组在解析肿瘤微环境中的细胞互作较传统测序有什么优势?
A: 传统测序测的是组织“均值”,只能知道样本里有IL1B和IL1R1,但无法确定“谁分泌、谁接收”。和元单细胞测序服务通过微流控技术给每个细胞打上独特Barcode,能将肿瘤上皮细胞与周围复杂的免疫细胞精准拆分,从而为配体-受体互作分析提供单细胞分辨率的数据基础。
Q2:胞间互作分析的准确性如何保障?
A: 分析准确度前提是细胞亚群注释必须绝对准确(如精准界定谁是KAC,谁是特定巨噬细胞)。和元具备完善的分析流程和资深生信团队,在完成标准的高质量建库测序后,能够通过精确的降维聚类与差异表达分析,确保后续互作计算不出现“张冠李戴”。

AtomGit 是由开放原子开源基金会联合 CSDN 等生态伙伴共同推出的新一代开源与人工智能协作平台。平台坚持“开放、中立、公益”的理念,把代码托管、模型共享、数据集托管、智能体开发体验和算力服务整合在一起,为开发者提供从开发、训练到部署的一站式体验。
更多推荐
 已为社区贡献12条内容
已为社区贡献12条内容






所有评论(0)