药物筛选“加速器”,AI智算一键速定!
传统药物筛选采用 “实验试错法”,从数百万化合物中逐一进行体外实验,存在效率低、成本高、周期长、命中率低等痛点。而 AI 智算通过 “计算模拟替代前期实验”,显著提升前期筛选效率,降低试错成本,缩小候选范围。后续结合湿实验验证,可实现 “精准筛选 + 高效验证” 的双重优势。
一、原理
AI 智算在药物筛选中的应用,核心是依托机器学习、深度学习、计算生物学等技术,融合分子结构信息、靶点特征、生物活性数据,对小分子与药物靶点的相互作用进行建模与预测,从海量化合物库中快速筛选出具有潜在生物活性的候选分子。
二、流程
1. 构建多维度药物筛选数据库与算法模型
整合海量基础数据,为 AI 计算提供 “学习样本”。核心包括靶点数据(如蛋白晶体结构、氨基酸序列、活性口袋特征,来自 PDB、Uniprot 等数据库)、化合物数据(如分子结构、理化性质、ADME/T 毒性、生物活性,来自 ZINC、PubChem、ChEMBL 等数据库)、实验数据(如既往体外结合验证、酶活性测定、细胞功能实验的结果)。
2、从海量化合物库中快速缩小候选范围
围绕药物靶点的成药需求,利用 AI 算法对海量化合物库进行多轮、分层筛选,快速缩小候选范围,优先保留具有较高成药潜力和靶点匹配度的分子。
3、分析候选分子与靶点的潜在结合模式及关键相互作用位点
对筛选得到的候选分子进一步开展结合模式预测,分析其与靶点之间的潜在相互作用位点、关键结合残基及稳定性特征,为后续实验设计与分子优化提供依据。
4、实验验证与结果反馈
结合生化活性实验、亲和力检测实验(如 SPR、BLI、MST、ITC)及细胞功能实验,对候选分子进行多层次验证。
三、文献案例
案例一

PRMT5 被识别为膀胱癌的潜在治疗靶点。来源于卡瓦的天然小分子 FKA 具有抗膀胱癌活性,但其机制此前尚不明确。本研究结合临床样本分析、细胞实验以及计算模拟与实验验证,表明 FKA 可靶向 PRMT5,并与其 Y304 和 F580 关键残基相互作用,抑制 PRMT5 介导的组蛋白 H2A/H4 Arg3 对称性精氨酸二甲基化,从而在体内外发挥抗膀胱癌作用,为 PRMT5 作为膀胱癌干预靶点及 FKA 作为候选天然抑制剂提供了依据。
AI虚拟筛选与优化流程
1分子对接:以 PRMT5:MEP50 复合物晶体结构(PDB ID: 4X60)为模板,采用 Schrödinger 的 Glide 方法预测候选化合物与 PRMT5 的结合模式。
2打分排序:
初筛与验证:对候选化合物按 docking score 排序,其中 FKB 的对接评分最高;随后结合细胞活性、PRMT5 相关效应及后续实验验证,最终聚焦 FKA。
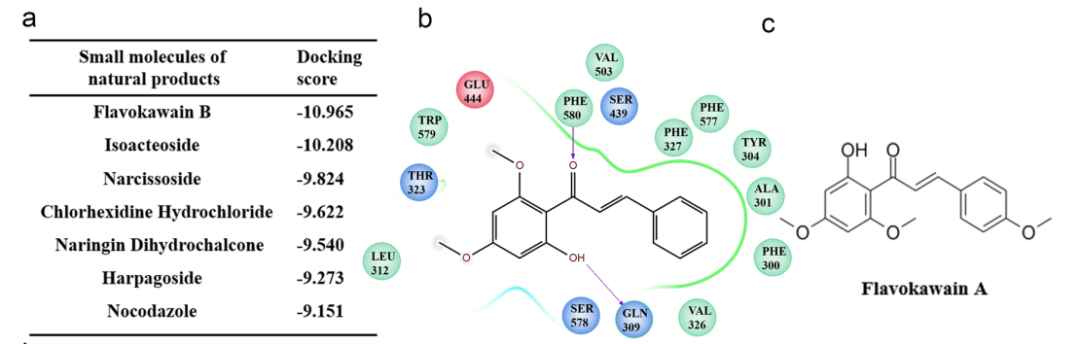
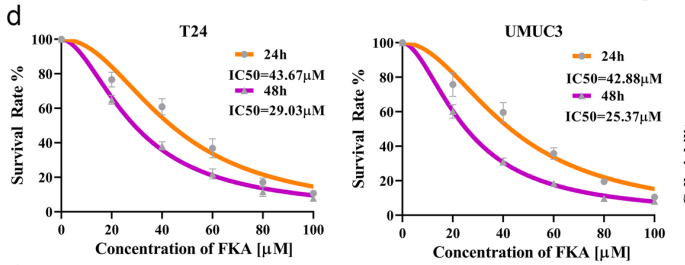
图:评估FKA作为靶向PRMT5的候选药物
3以 PRMT5:MEP50 复合物晶体结构(PDB: 4X60)为模板进行分子对接。
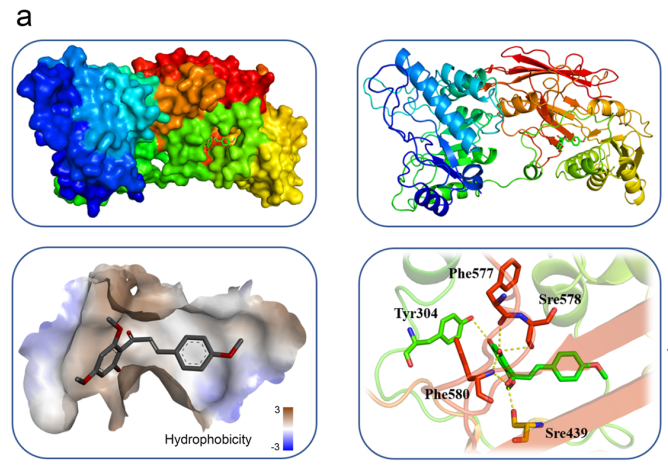
图:结合位点分析结果
4采用 Gaussian09 对 FKA 进行量化计算与参数化处理,随后使用 Amber 对 FKA 与 PRMT5 复合物进行分子动力学模拟,并计算其 RMSD(上)和 RMSF(下),以评估复合物的结构稳定性和局部柔性变化。
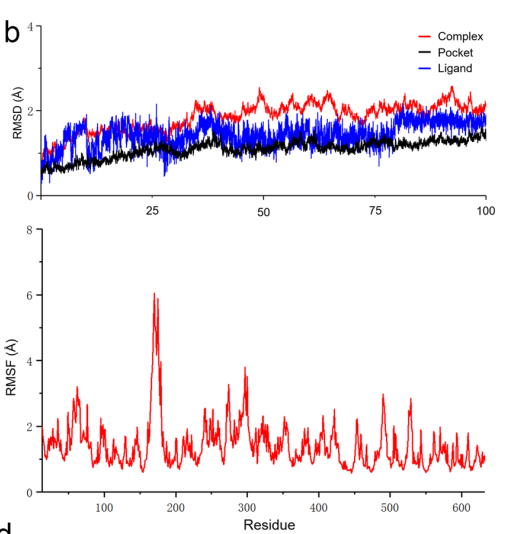
图:分子动力学模拟结果
案例二

本研究为发掘新型降血脂药物,通过虚拟分子对接对含 3200 种天然产物的文库进行筛选,以靶向胆固醇合成关键酶 ACLY,从排名靠前的化合物中选定异银杏双黄酮(ISOGK)开展研究。实验证实 ISOGK 可直接结合并抑制 ACLY 活性,在高脂血症小鼠、仓鼠模型中显著降低血脂、减轻动脉粥样硬化,且其降脂抗动脉粥样硬化作用依赖于 ACLY。该研究首次证实 ISOGK 作为天然 ACLY 抑制剂的降脂与抗动脉粥样硬化作用,为心血管疾病治疗提供了新的候选药物。
AI虚拟筛选流程
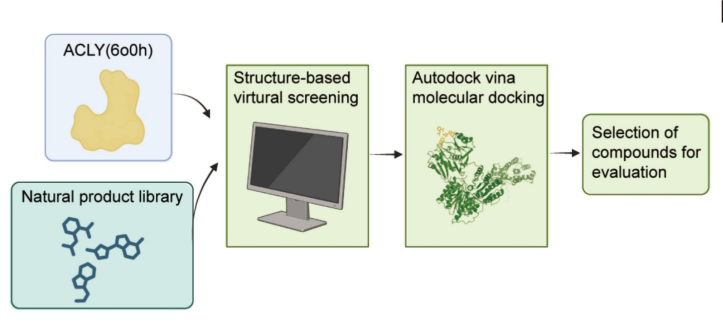
1受体与文库准备:获取 ACLY 蛋白结构(PDB ID: 6O0H)并进行受体预处理,作为分子对接受体;构建含 3200 种天然产物的文库,完成候选化合物的结构准备、加氢及优化。
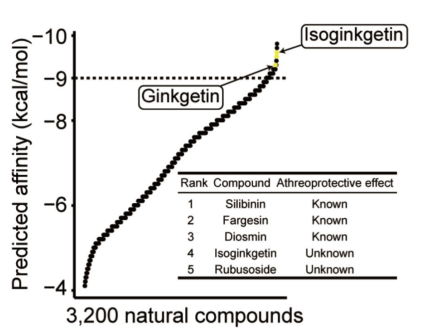
图:预测结合亲和力/对接评分结果
2分子对接筛选:采用 Autodock Vina 1.2.0 软件,将对接框设定在 ACLY 活性位点,对天然产物文库进行基于结构的虚拟分子对接。
3候选物筛选:依据对接评分排序,并结合体外 ACLY 酶活抑制实验(ADP-Glo 法)及“尚未报道抗动脉粥样硬化作用”的筛选标准,最终确定 isoginkgetin(ISOGK)为后续研究对象。
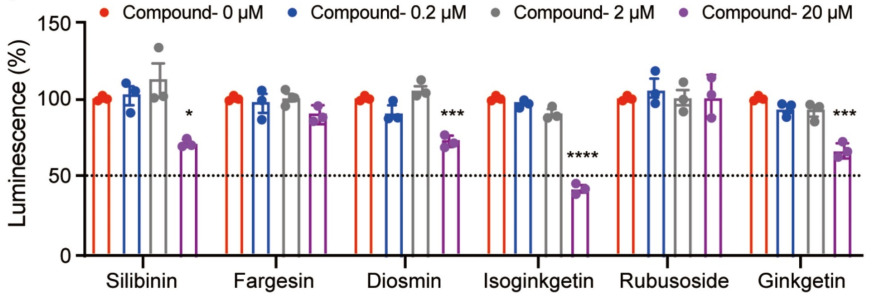
图:体外评价最佳候选物对ACLY酶活性的抑制作用
四、瑞源医学AI 数字化技术
01 AI多模态文库筛选服务(蛋白-化合物)
随着结构生物学与计算化学方法的成熟,基于结构的虚拟筛选(Virtual Screening, VS)已成为小分子先导发现与分子优化的重要手段。通过分子对接在计算机上高通量评估配体与蛋白的结合模式与相对亲和力能显著降低实验成本、提高筛选效率。
以目标蛋白(化合物)为驱动,瑞源采用Smina(优化版小分子-蛋白对接工具,支持柔性残基,适合药物虚拟筛选)对外部提供或自建的化合物(蛋白)库进行两阶段虚拟筛选,系统评估候选分子的结合模式与打分,为后续的分子优化与功能验证提供依据。
筛选流程
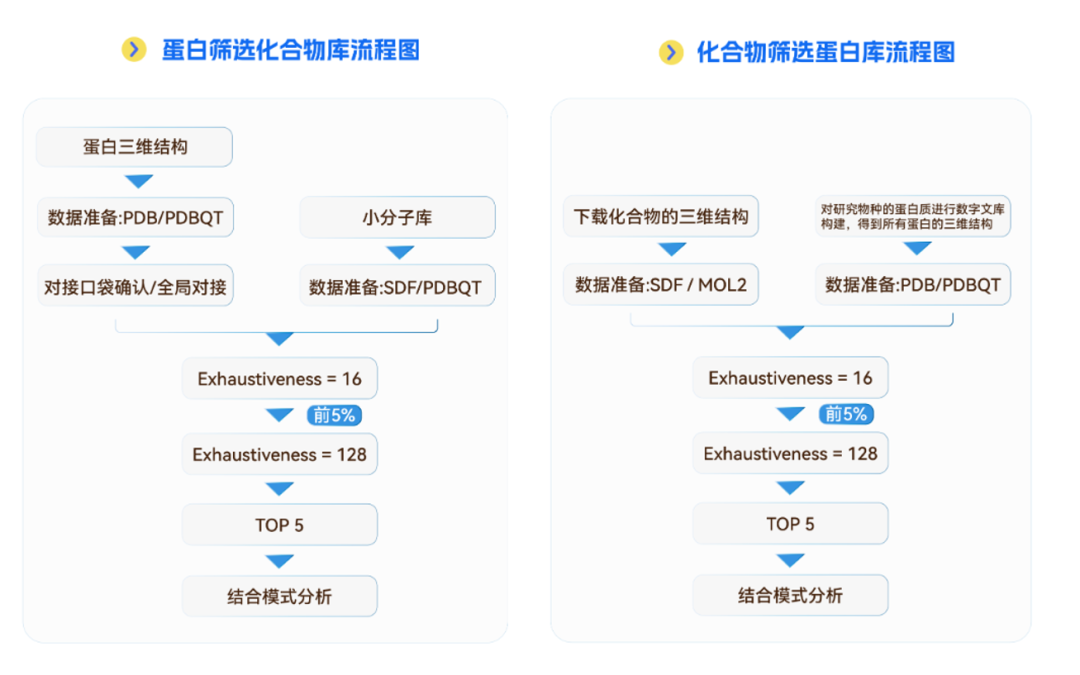
技术优势
✅ 高通量筛选:基于Smina软件进行分子对接,每小时可完成1W+次对接任务,高效实现大规模化合物库筛选
✅ 可靠性结果:提供每对蛋白-化合物的最低结合自由能,确保数据准确性
✅ 高质量图片:提供五组互作对的2D/3D模型结合位点分析图,清晰展示结合位点、氢键及距离信息,提供全面的互作细节
✅ 全链路实验保障:依托自有实验平台,提供SPR、BLI、MST、ITC体外仪器互作类湿实验,实现从数字化筛选到一对一验证的全流程服务
案例展示
蛋白筛选化合物
1目标蛋白三维结构
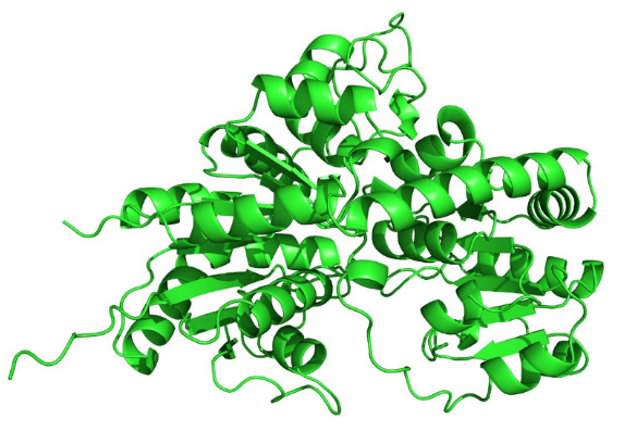
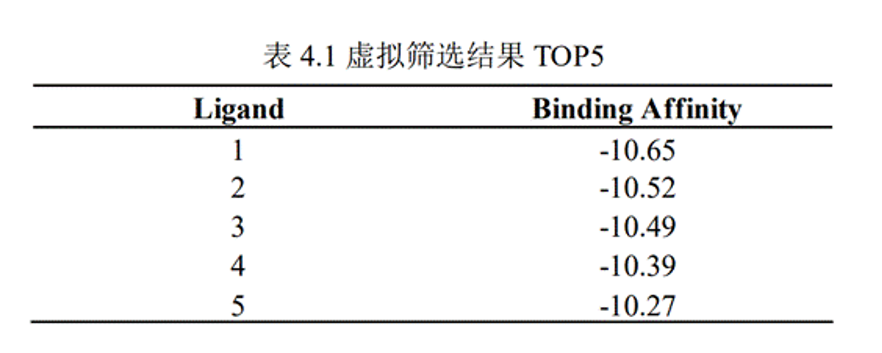
2Smina筛选结果:其中Ligand列为化合物的ID;Binding Affinity列为最低结合能,越低表明对接构象越稳定
3互作分析作图(仅限精品版)
取前五对具有最低结合能的蛋白-化合物进行分析作图
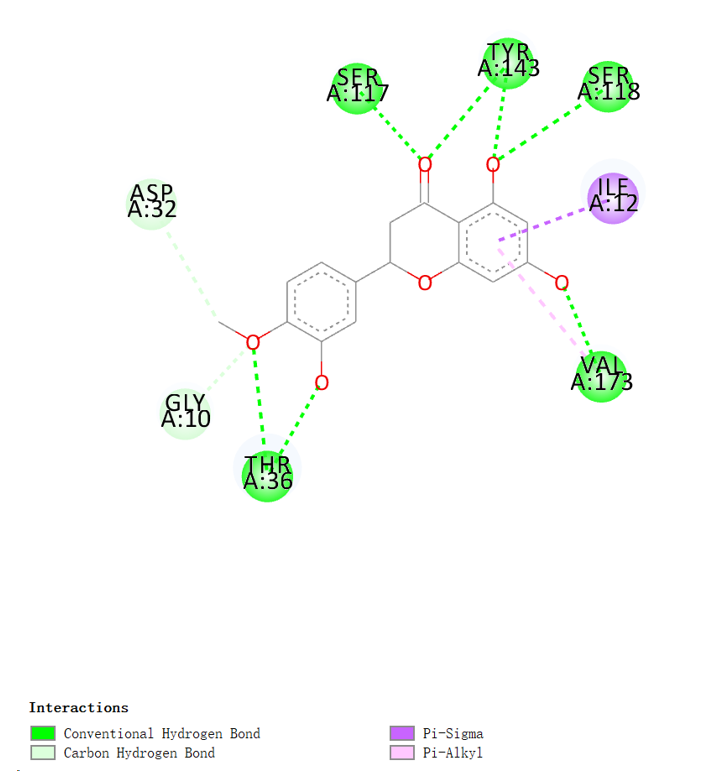
图 :蛋白与化合物的二维互作图
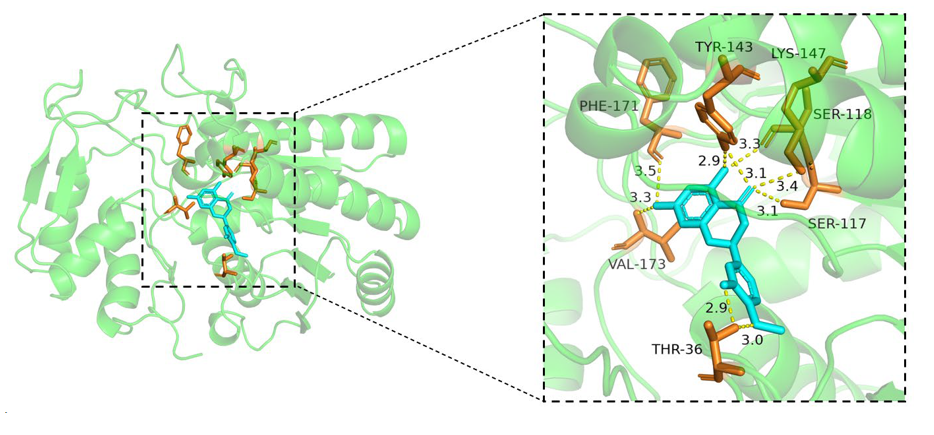
图 :蛋白与化合物的三维互作图
化合物筛选蛋白
1目标化合物的三维结构
图 :化合物的三维结构
2Smina筛选结果
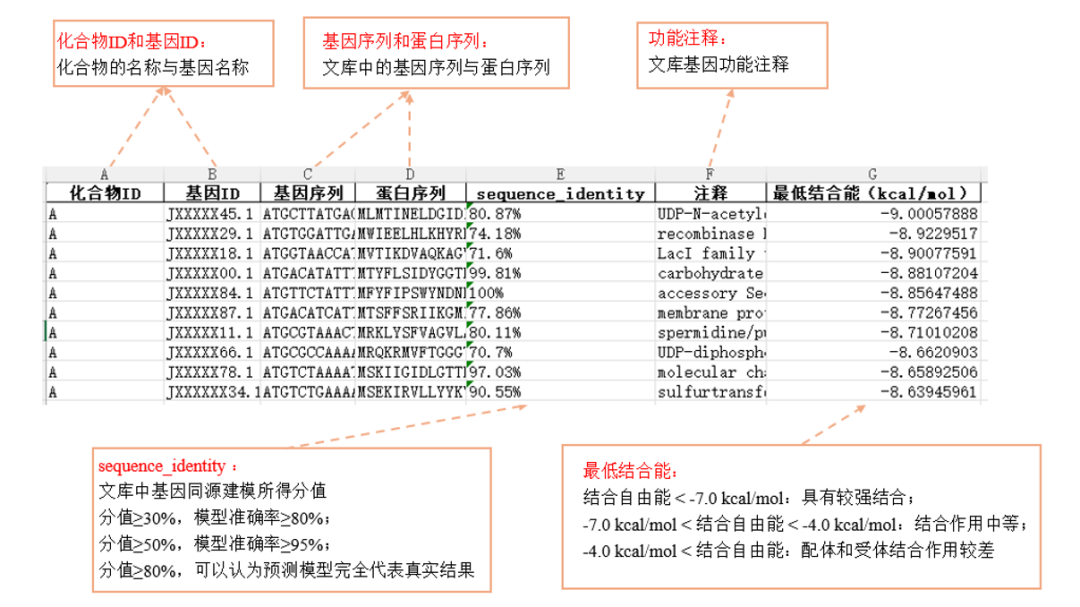
图 :AI多模态化合物筛选蛋白结果
3互作分析作图(仅限精品版)
取前五对具有最低结合能的化合物-蛋白进行分析作图
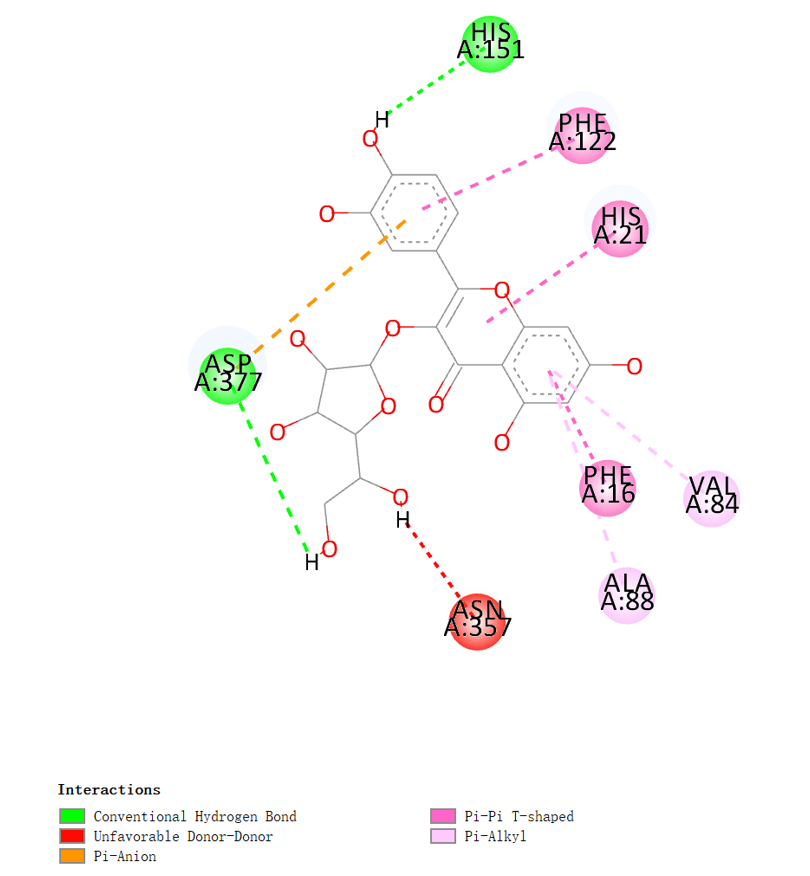
图 :化合物与蛋白的二维互作图
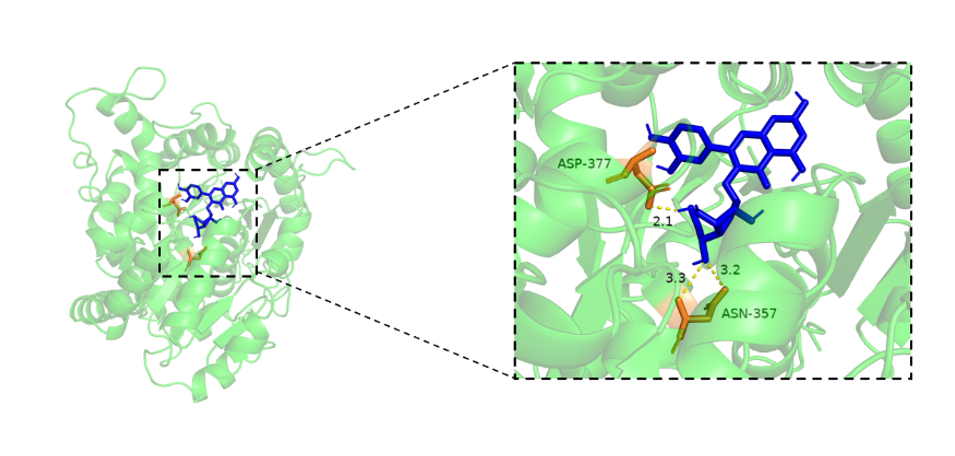
图 :化合物与蛋白的三维互作图
02 分子动力学模拟(蛋白-小分子)
分子动力学模拟(Molecular Dynamics Simulation, MD)是研究生物大分子运动行为及相互作用机制的重要工具。相较于静态结构分析,MD 可在原子尺度上动态观察蛋白复合物的构象演化、结合界面稳定性及其对环境变化的响应,为机制解析与结构优化提供更丰富的信息。
瑞源医学提供蛋白-小分子复合物的分子动力学模拟服务,可根据研究需求在设定条件下开展体系模拟,分析复合物的结构稳定性、相互作用模式及动态行为,为后续结构优化、机制研究和功能验证提供支持。
原理
以复合物的三维结构为初始模型,采用经典力场对分子间的相互作用进行精确描述。在模拟过程中,动态追踪体系中每个原子的轨迹,细致再现相互作用过程中结合、解离、界面重构及构象变化等分子层面的复杂现象。
应用领域
主要用于药物发现与设计、酶学与生物催化、疾病机制研究、材料科学与纳米技术等领域。
蛋白-小分子动力学模拟案例
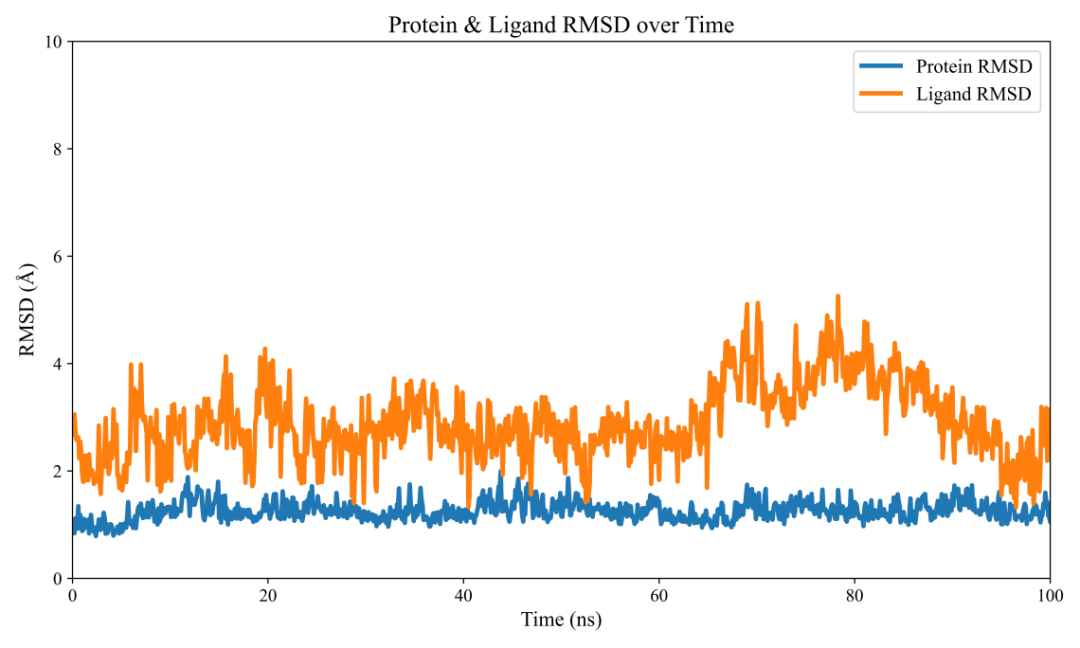
图1 Protein与Ligand复合物100 ns动力学过程中的RMSD
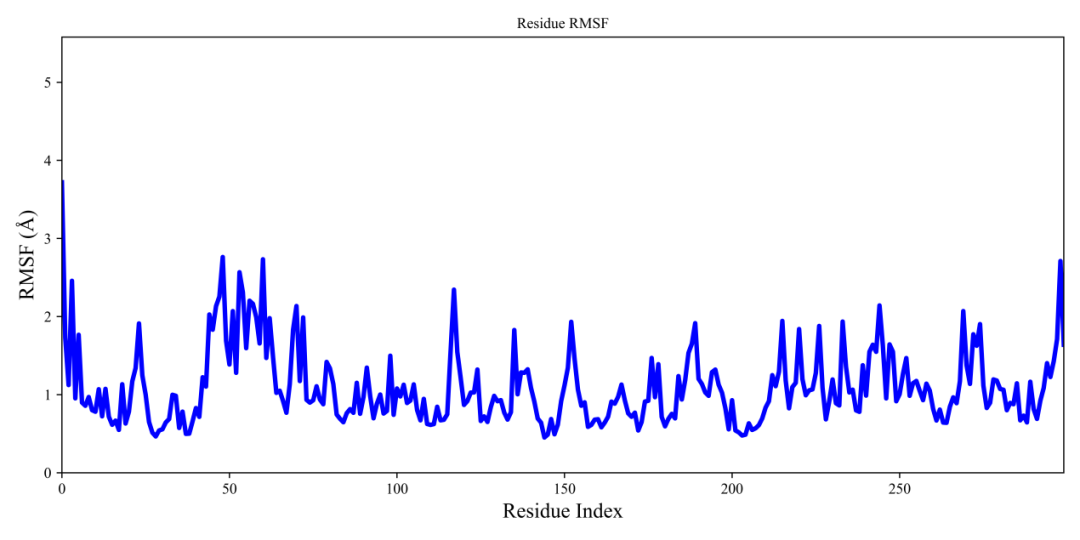
图2 Protein与Ligand复合物100 ns动力学过程中的RMSF
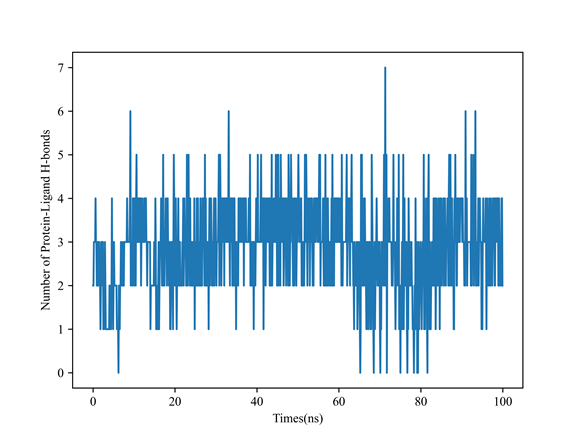
图3 Protein与Ligand复合物100 ns动力学过程中的氢键数目变化
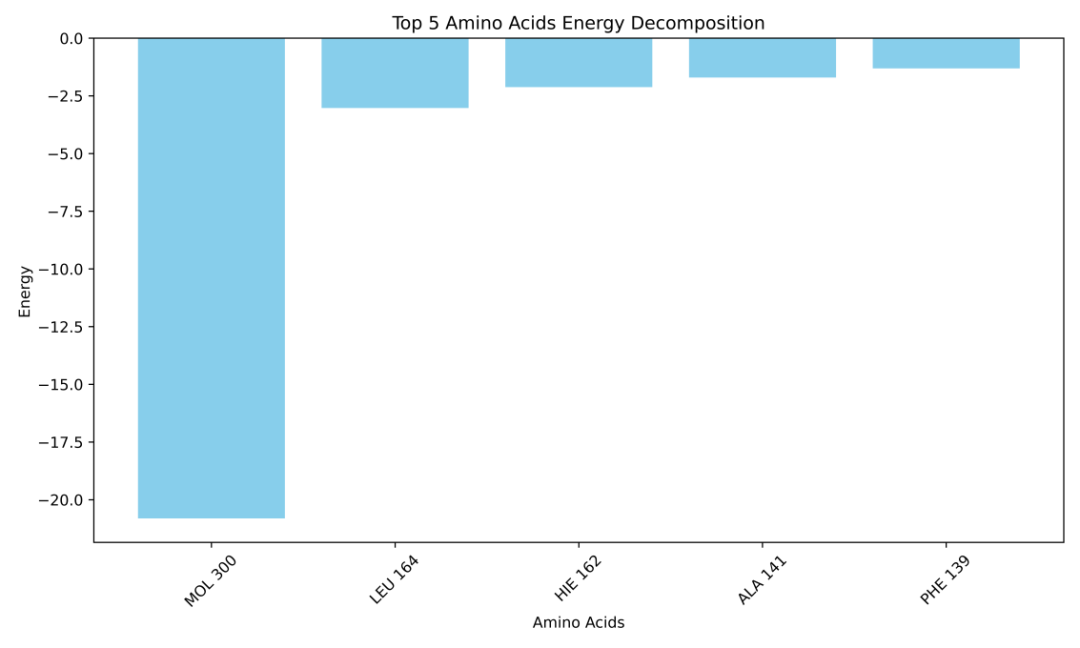
图4 Protein与Ligand复合物100 ns动力学过程中的各残基结合自由能贡献
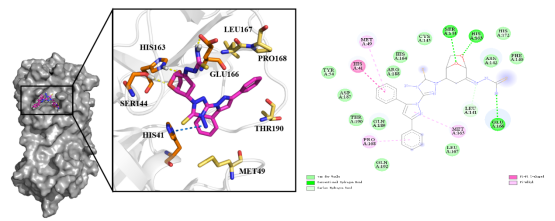
图5 Protein与Ligand复合物在100 ns模拟后的构象与相互作用展示的
03 互作与结合位点分析AOS
瑞源医学自主研发蛋白互作置信度分值智能系统,用于衡量蛋白质与小分子等相互作用可靠性的指标。研究互作的置信度,并给出置信度分值为后续实验提供参考依据。
技术优势
✅ 高精度建模:基于AlphaFold3 + 小分子对接工具,构建蛋白质与小分子的高精度三维模型蛋白
✅ 可靠的置信度分析:针对建模结果进行评分,保障高质量交付
✅ 结合位点分析:提供蛋白小分子复合物(远景+近景)结合位点分析图,清晰展示结合位点、氢键及距离信息,提供全面的互作细节
案例展示
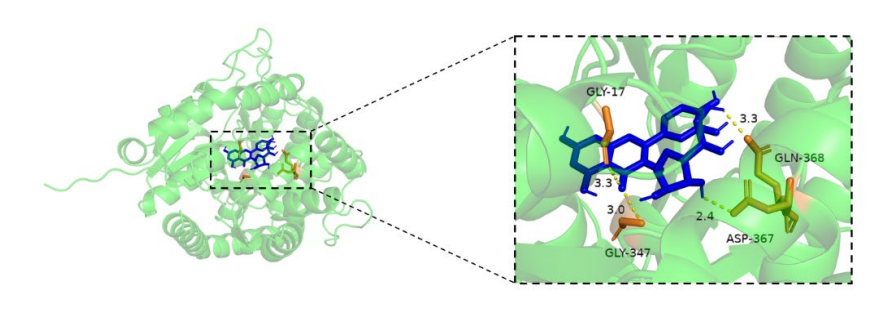
图 蛋白与小分子结合位点标注图

AtomGit 是由开放原子开源基金会联合 CSDN 等生态伙伴共同推出的新一代开源与人工智能协作平台。平台坚持“开放、中立、公益”的理念,把代码托管、模型共享、数据集托管、智能体开发体验和算力服务整合在一起,为开发者提供从开发、训练到部署的一站式体验。
更多推荐
 已为社区贡献1条内容
已为社区贡献1条内容






所有评论(0)