深度解析T细胞信号枢纽:CD3(分化簇3)的分子机制、抗体药物研发与技术演进
CD3(分化簇3)作为T细胞受体(TCR)复合物的核心组成部分,是连接抗原识别与免疫效应的关键信号转导分子。本文将从生物化学角度解析其四链复合物结构与ITAM信号通路,梳理单抗与双抗药物的研发逻辑,并探讨双特异性抗体精准化改造、Fc段工程化修饰及AI辅助设计等前沿技术趋势,为免疫治疗领域的研发人员提供技术参考。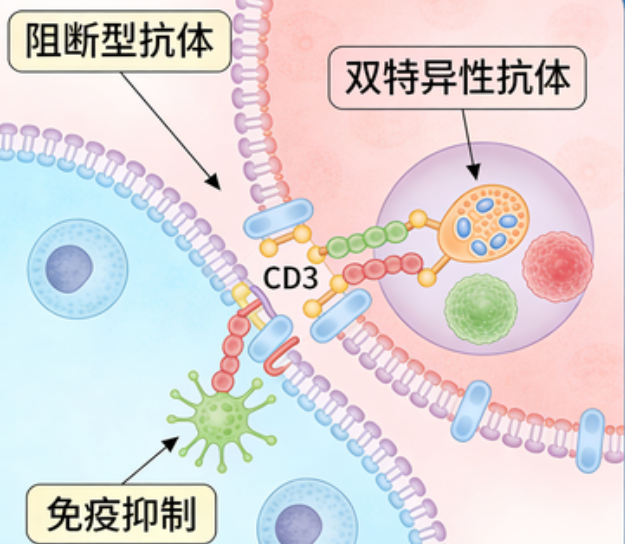
一、 分子结构与信号转导机制
CD3并非单一蛋白,而是由CD3ε、CD3δ、CD3γ及CD3ζ四条多肽链组成的复合物。它与TCR通过非共价键结合,形成TCR-CD3复合物,锚定在T细胞表面,核心功能是将“抗原识别”信号转化为“细胞内响应”。
1. 复合物组装与抗原感知
T细胞无法直接识别游离抗原。在#实验室日常 中,抗原提呈细胞(APC)处理后的抗原-MHC复合物被TCR识别,TCR作为“传感器”结合抗原,而CD3则作为“信号转换器”接收构象变化。这一过程是#生物实验 中研究T细胞激活的起点。
2. ITAM介导的级联磷酸化
CD3胞内区含有免疫受体酪氨酸活化基序(ITAM)。当TCR结合抗原后,ITAM发生磷酸化,招募ZAP-70蛋白酪氨酸激酶。这是信号放大的关键节点,ZAP-70进一步激活下游的IRAK家族激酶与TRAF6,启动两条核心通路:
- MAPK通路:调控细胞增殖与分化。
- NF-κB通路:调控炎症因子(如IL-2、IFN-γ)的转录。
在#科研干货 层面,检测该通路的常用技术包括:利用Western Blot检测ZAP-70及NF-κB的磷酸化水平,以及利用ELISA检测IL-2的分泌量,以验证T细胞是否被成功激活。
二、 抗体药物研发的技术路径
基于CD3的信号阻断或重定向功能,目前的抗体药物主要分为单克隆抗体和双特异性抗体两大技术流派。
1. 单克隆抗体:免疫抑制的基石
早期的鼠源单抗(如OKT3)通过特异性结合CD3ε链,阻断TCR-CD3信号传导,抑制T细胞增殖,曾广泛用于预防器官移植后的急性排斥反应。然而,鼠源抗体的高免疫原性限制了其长期使用。
技术演进方向:人源化改造。通过基因工程技术将鼠源抗体人源化,大幅降低了免疫原性,目前主要应用于自身免疫性疾病的治疗,通过适度抑制T细胞过度激活来缓解炎症。
2. 双特异性抗体(BsAb):精准重定向
双抗技术是当前的主流趋势,其核心逻辑是“一端抓CD3,一端抓靶标”,强制形成免疫突触。
- BCMA×CD3双抗:一端结合T细胞表面的CD3,另一端结合异常浆细胞表面的BCMA,激活T细胞定向清除异常细胞。
- CD3×CD19双抗:通过结合B细胞表面的CD19,激活T细胞调控异常B细胞活性。
此类药物多采用IgG4骨架,以降低Fc段介导的非特异性效应,提升安全性。
三、 技术演进:精准化与智能化趋势
随着抗体工程与计算生物学的发展,CD3靶点的研发正面临深刻的技术迭代,主要体现在以下三个维度:
1. 双抗的精准化改造
传统双抗易引发细胞因子释放综合征(CRS),即“细胞因子风暴”。解决这一问题的核心技术是亲和力优化:降低CD3结合臂的亲和力,使其仅在高密度靶抗原环境下(如病灶部位)才激活T细胞,从而减少全身性炎症反应。此外,条件性激活(Probody)技术也是研究热点,旨在实现仅在肿瘤微环境或炎症部位激活药物。
2. 抗体结构工程与新型抗体
- Fc段改造:通过糖基化工程或点突变延长药物半衰期,减少给药频次。
- 纳米抗体(Nanobody):利用骆驼源或工程化改造的纳米抗体,分子量小、组织穿透力强,甚至能突破血脑屏障,为神经炎症等领域的治疗提供了新的技术手段。
3. AI辅助药物设计(AIDD)
利用深度学习模型模拟CD3与抗体的结合构象,预测ITAM磷酸化的动力学变化,可以在计算机辅助下快速筛选出亲和力适中、信号调控精准的候选分子,大幅缩短从靶点验证到先导化合物筛选的周期。
结语
CD3作为T细胞免疫应答的“总开关”,其复杂的信号网络为药物研发提供了丰富的切入点。从早期的单抗阻断到前沿的AI设计与双抗重定向,技术的每一次进步都在试图平衡“疗效”与“安全性”。对于科研人员而言,深入理解其分子机制与技术演进逻辑,是开展创新药物研发的基石。

AtomGit 是由开放原子开源基金会联合 CSDN 等生态伙伴共同推出的新一代开源与人工智能协作平台。平台坚持“开放、中立、公益”的理念,把代码托管、模型共享、数据集托管、智能体开发体验和算力服务整合在一起,为开发者提供从开发、训练到部署的一站式体验。
更多推荐
 已为社区贡献6条内容
已为社区贡献6条内容






所有评论(0)