生物制药前沿:CD262 (TRAILR2/DR5) 靶点技术解析与应用
CD262(又称TRAILR2、DR5、TNFRSF10B)是肿瘤坏死因子受体超家族(TNFRSF)的关键成员。作为一种单次跨膜I型膜蛋白,其核心定位于细胞表面,广泛表达于免疫细胞、内皮细胞及多种组织细胞中。本文将从分子机制、药物研发现状及未来技术趋势三个维度,系统解析CD262靶点在调控细胞稳态、组织损伤修复及免疫调节中的技术原理与应用价值。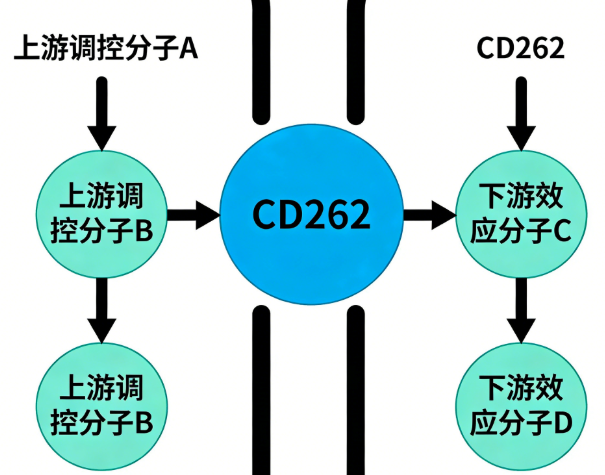
1. CD262靶点的作用机制
CD262的核心功能在于介导细胞凋亡信号传导以及非凋亡性的细胞调控。其作用机制遵循“配体-受体结合—信号复合物组装—下游通路激活”的经典模式,核心分子事件清晰可辨。
配体识别与受体激活
CD262的天然配体为TRAIL(TNF相关凋亡诱导配体,TNFSF10),属于TNF家族细胞因子。TRAIL通常以同源三聚体形式存在,能够特异性结合CD262胞外区的配体结合域。这一结合诱导CD262发生构象变化,使其胞内段的死亡结构域(DD)暴露并活化,这是信号启动的关键步骤。值得注意的是,CD262在静息细胞中表达水平较低,而在组织损伤、炎症应激或细胞稳态失衡时表达显著上调,体现了其“应激响应型”的表达特性。
死亡诱导信号复合物(DISC)组装
活化的CD262通过死亡结构域招募FADD(Fas相关死亡结构域蛋白)接头分子,FADD进一步募集caspase-8(半胱天冬酶-8),三者共同组装形成DISC复合物。DISC是CD262信号传导的核心平台,其组装效率直接决定了下游信号的强度。在DISC中,caspase-8发生自剪切激活,形成活性形式的caspase-8,从而启动caspase级联反应,最终介导细胞凋亡。
下游信号通路的双重调控
除了经典的凋亡通路,CD262还可激活NF-κB、MAPK等非凋亡通路,参与细胞增殖、迁移及炎症反应的调控。
- 凋亡通路:激活的caspase-8直接切割并激活下游的caspase-3和caspase-7,执行细胞凋亡程序,清除异常或受损细胞,维持机体组织稳态。
- 非凋亡通路:CD262可通过招募TRADD、RIPK1等接头蛋白,激活NF-κB通路,调控炎症因子的表达;同时激活MAPK通路,参与细胞迁移与组织修复。这种“凋亡+非凋亡”的双重调控机制,使CD262成为机体平衡细胞生死、应对应激的核心靶点。
2. CD262对应的上市抗体药物
目前全球已上市多款靶向CD262的单克隆抗体药物,主要分为激动型抗体(激活CD262凋亡信号)与阻断型抗体(抑制CD262异常信号)两类。这些药物均通过精准靶向CD262,实现对细胞信号的精准调控。
康尼珠单抗(Conatumumab)
- 药物类型:全人源IgG1型激动型单克隆抗体
- 作用机制:特异性结合CD262胞外区,模拟TRAIL的配体作用,诱导CD262构象变化并激活DISC复合物,启动caspase凋亡级联,从而清除异常增殖细胞。
- 应用场景:用于调控细胞异常增殖相关疾病。临床研究中展现出良好的靶向性与安全性,可单独或联合其他药物使用。
替妥木单抗(Tigatuzumab)
- 药物类型:人源化IgG1型激动型单克隆抗体
- 作用机制:以高亲和力结合CD262,优先激活CD262介导的凋亡通路,对正常细胞影响较小,具备“选择性调控”的优势。
- 应用场景:适用于细胞稳态失衡相关疾病的治疗。临床数据显示其耐受性良好,能有效调控异常细胞信号。
抗CD262阻断型单克隆抗体
- 药物类型:人源化IgG2型阻断型单克隆抗体
- 作用机制:特异性结合CD262的配体结合域,竞争性阻断TRAIL与CD262的结合,从而抑制CD262下游凋亡与炎症信号的过度激活。
- 应用场景:用于治疗因CD262信号异常亢进导致的组织损伤、慢性炎症等疾病,通过平衡信号通路,恢复机体稳态。
3. CD262靶点的未来发展趋势
随着抗体工程技术、精准医疗与多组学研究的深入,CD262靶点的研发正从单一抗体向多元化、精准化、协同化方向发展。结合当前生物制药领域的前沿进展,其未来趋势主要体现在以下四方面:
双特异性抗体(BsAb)研发突破
研发人员正积极开发CD262×免疫调节靶点双特异性抗体,如CD262×CD3、CD262×PD-L1双抗。这类抗体一方面通过CD262调控细胞凋亡信号,另一方面通过免疫调节靶点激活机体免疫应答,实现“信号调控+免疫激活”的双重作用,以提升对复杂疾病的治疗效果。目前,多款CD262双抗已进入临床前研究阶段,展现出优于单一抗体的疗效潜力。
抗体偶联药物(ADC)创新拓展
将CD262抗体与非细胞毒性调控载荷偶联,利用CD262的靶向性,将调控物质精准递送至靶细胞内。这种方式可以在低剂量下实现高效信号调控,同时降低全身毒性。与传统ADC聚焦于细胞杀伤不同,CD262-ADC聚焦于“信号精准调控”,适用于慢性炎症、组织损伤修复等场景,目前已进入临床前验证阶段。
联合治疗策略优化
探索CD262抗体与小分子靶向药、抗炎药物、细胞因子的联合治疗方案,形成协同效应。例如,CD262激动型抗体与抗炎药物联合,可协同清除异常细胞并抑制炎症反应;CD262阻断型抗体与组织修复药物联合,可加速受损组织修复。联合治疗可降低单一药物剂量,提升疗效与安全性,是未来CD262靶向治疗的重要方向。
精准化与个体化应用升级
通过单细胞测序、蛋白质组学技术,检测患者体内CD262表达水平、TRAIL通路关键分子状态及细胞敏感性,筛选出适合CD262靶向治疗的人群,实现“个体化用药”。同时,开发CD262特异性诊断试剂,实现对相关疾病的早期诊断、病情监测与疗效评估,推动CD262靶向治疗从“广谱应用”向“精准医疗”转型。

AtomGit 是由开放原子开源基金会联合 CSDN 等生态伙伴共同推出的新一代开源与人工智能协作平台。平台坚持“开放、中立、公益”的理念,把代码托管、模型共享、数据集托管、智能体开发体验和算力服务整合在一起,为开发者提供从开发、训练到部署的一站式体验。
更多推荐
 已为社区贡献6条内容
已为社区贡献6条内容





所有评论(0)