AI破局抗体发现:科晶生物IgGM与AlphaFold3联合设计高亲和scFv抗体全流程解析

在当今的创新药研发与诊断试剂开发中,单链抗体(scFv)凭借其分子量小、组织穿透力强、体内清除快及免疫原性低等独特优势,正成为CAR-T疗法、双特异性抗体及ADC药物开发的核心基石。
然而,传统的抗体发现过程往往面临周期漫长、成本高昂、筛选盲目性大等痛点。如何在没有已知完美结构的条件下,快速、精准地设计出针对特定表位的高亲和力scFv抗体?
科晶生物依托前沿的人工智能与结构生物学算法,为您提供了一套高效的破局方案——高亲和scFv抗体设计服务。今天,我们将通过一份真实的实战结题报告——《靶向B7H3高亲和scFv抗体设计》,带您沉浸式体验计算生物学是如何为抗体研发装上“加速器”的。
实战拆解:四步“算”出高亲和潜力分子B7H3(CD276)是一种在多种实体瘤中高度表达的重要免疫检查点蛋白,是当前肿瘤靶向治疗的热门研究方向。为了获得针对该靶点的高互作抗体,科晶生物技术团队打出了一套“AI生成+高通量初筛+精细建模验证”的数字化组合拳:
Step 1:精准锚定,锁定诱饵结合位点 抗体设计的成败,很大程度上取决于“瞄靶”的精准度。团队首先对B7H3蛋白的三维结构进行了深度解析,精准提取了关键的残基片段(黄色区域)作为诱饵蛋白。这一步就像是为后续的定向生成绘制了清晰的空间坐标,确保抗体设计有的放矢。
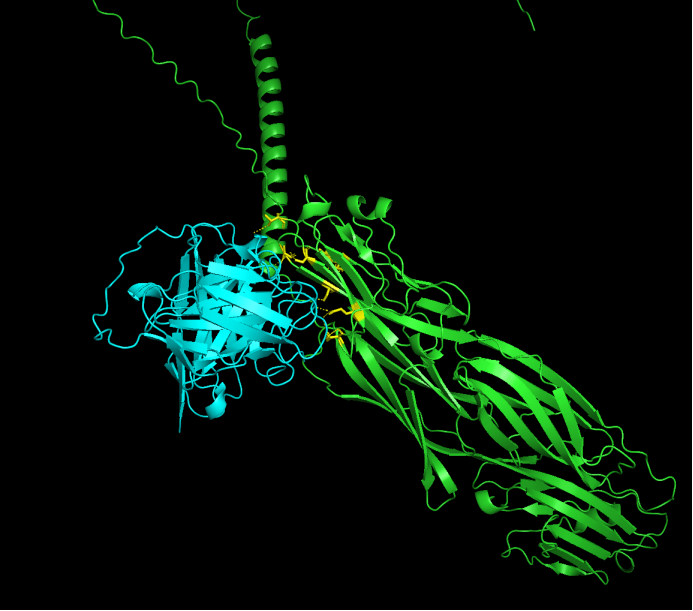
Step 2:海量生成,IgGM算法从头设计 锁定靶区后,科晶生物引入了专为抗体设计的生成大模型——IgGM算法。 不同于常规的序列突变检索,IgGM不仅能根据特定表位从头生成(De novo design)全新的抗体序列,还支持亲和力定向进化与预测。此外,它能为人源化提供强大支持,使得非人类抗体能够通过修改变得更适合人类使用,显著降低免疫原性风险。在此次任务中,IgGM算法基于诱饵蛋白的特定构象,迅速且高质量地生成了500个scFv候选抗体序列,极大地扩充了优质候选库的丰度。
Step 3:大浪淘沙,HDOCK高通量分子对接 面对500个候选序列,如何挑选出结合最紧密的“潜力股”?团队采用了结合模板匹配与自由对接算法的高效蛋白互作工具HDOCK进行严苛的虚拟筛选。 精筛结果令人振奋:所有500个scFv候选抗体均成功达到了-200的优秀结合阈值(置信度得分>0.7,提示具备极大概率的高效结合),且结合位点区域呈现出大量密集的氢键网络,空间构象极其稳定。
Step 4:金标准验证,AlphaFold3一对一精细建模 为了让计算结果更可靠地向湿实验转化,团队将HDOCK初筛出的Top 30候选数据,转入目前结构预测领域的明星模型——AlphaFold3中进行一对一的精细建模分析。 通过严密计算评估整体蛋白质三维结构准确性的 pTM,以及评估复合体接触界面预测准确性的 ipTM,科晶生物对结果进行了全方位的深度验证。
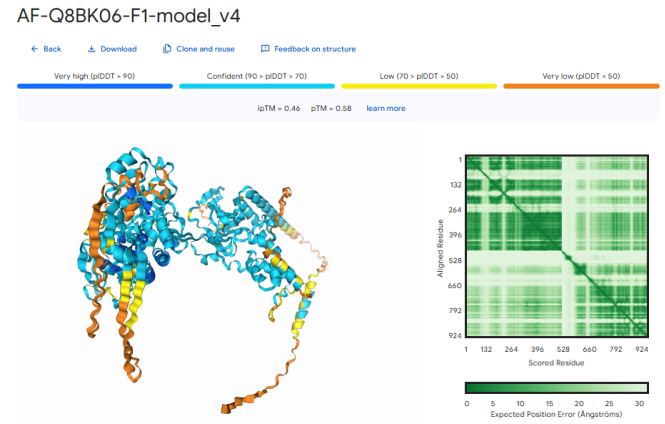
交付成果:高质量数据赋能高效研发 经过上述严苛的AI计算管线,科晶生物最终向客户交付了详尽的筛选数据总表。在报告中,多条对接分值极低、且ipTM与pTM分数双高的高优序列(数据表中标红序列)脱颖而出,且未出现脱靶现象。
这些经过数字化精筛的“金标准”候选者,将直接作为客户后续优先进行细胞学验证的极佳参照。这不仅大幅缩短了早期的研发周期,更为管线推进节省了高昂的试错成本。

携手科晶生物,加速您的研发管线 从海量生成到精细验证,科晶生物的“高亲和scFv抗体设计”服务,是将前沿AI算法转化为切实可行研发生产力的生动体现。
作为一家探索数字化生物的创新型技术服务商,我们不仅提供高精度scFv抗体设计,还能满足您对大分子对接评估、抗体人源化改造及亲和力成熟等多维度的定制化需求。
不再苦等传统筛选结果,让优质抗体“算”出来! 如果您正在开展靶向治疗或诊断试剂研发,且面临靶点难筛选、抗体亲和力不佳的瓶颈,欢迎随时与我们联系。让我们用尖端算法,为您的科研提速!
参考文献:
1.IgGM: A Generative Model for Functional Antibody and Nanobody Design.
2.Wang, R., Wu, F., Shi, J., Song, Y., Kong, Y., Ma, J., He, B., Yan, Q., Ying, T., Zhao, P., Gao, X., & Yao, J. (2025). A Generative Foundation Model for Antibody Design. bioRxiv..
3.Cohen, Tomer et al. “NanoNet: Rapid and accurate end-to-end nanobody modeling by deep learning.” Frontiers in immunology vol. 13 958584. 12 Aug. 2022, doi:10.3389/fimmu.2022.958584.
4.Baek, M., DiMaio, F., Anishchenko, I., Dauparas, J., Ovchinnikov, S., Lee, G. R., ... & Jumper, J. (2021). Accurate prediction of protein structures and interactions using a three-track neural network. Science, 373(6557), 871-876.
5.Lin, Z., Rigden, D. J., & McGuffin, L. J. (2023). Language models of protein sequences at the scale of evolution enable accurate structure prediction. Science, 379(6631), 1123-1130.
6.Yan Y , Tao H , He J ,et al.The HDOCK server for integrated protein–protein docking[J].Nature Protocols, 2020, 15(Suppl 25):1-24.DOI:10.1038/s41596-020-0312-x.
7.Abramson, J., Adler, J., Dunger, J. et al. Accurate structure prediction of biomolecular interactions with AlphaFold 3. Nature 630, 493–500 (2024). https://doi.org/10.1038/s41586-024-07487-w.

AtomGit 是由开放原子开源基金会联合 CSDN 等生态伙伴共同推出的新一代开源与人工智能协作平台。平台坚持“开放、中立、公益”的理念,把代码托管、模型共享、数据集托管、智能体开发体验和算力服务整合在一起,为开发者提供从开发、训练到部署的一站式体验。
更多推荐
 已为社区贡献19条内容
已为社区贡献19条内容







所有评论(0)