告别漫长动物免疫!科晶生物基于AI的“从头设计纳米抗体”全流程解析
在创新药研发与体外诊断试剂开发的浪潮中,纳米抗体(Nanobody/VHH)凭借其分子量小、组织穿透力强、结构稳定性高及易于工程化改造等诸多优势,正成为生物医药领域备受瞩目的“明星分子”。
然而,传统的纳米抗体发现往往高度依赖羊驼等动物的免疫、全血提取及庞大的噬菌体展示文库筛选。这种模式不仅研发周期长、成本高昂,且在面对高同源蛋白、有毒抗原等“困难靶点”时,常常陷入“盲盒式”筛选的困境,成功率难以把控。
如何打破传统湿实验的效率瓶颈? 随着人工智能与结构生物学的深度融合,“从头设计(De novo design)”技术为大分子药物开发开辟了全新路径。
今天,我们将结合科晶生物为您硬核揭秘:如何依托前沿的AI计算生物学平台,无需动物免疫,直接在计算机中为靶标蛋白“量身定制”高特异性、高亲和力的互作纳米抗体!
第一步:火眼金睛,精准锁定结合位点
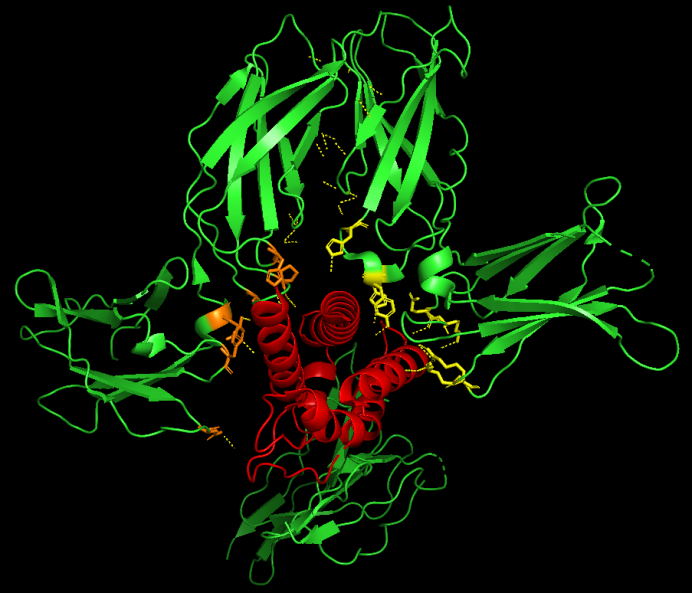
一切卓越的靶向设计,都始于对靶标空间结构的深刻理解。 在本次技术服务项目中,客户的核心需求是针对特定的诱饵蛋白(BETA与GAMMA靶点)开发互作纳米抗体。科晶生物技术团队首先利用 Uniprot 等权威数据库提供的晶体结构(2B5I),精准定位了BETA(橙色区域)与GAMMA(黄色区域)的核心结合位点。明确了靶蛋白的活性区域,就相当于为后续的AI定向生成画好了“靶心”。
第二步:无中生有,RFdiffusion定制核心结合物
锁定靶区后,核心生成环节正式登场。团队调用了当前在蛋白质设计领域极具优势的生成式AI大模型——RFdiffusion。 RFdiffusion擅长在指定的空间约束下,利用先进的扩散模型生成具有高特异性的全新蛋白质结构。为了完美契合纳米抗体发挥核心识别作用的CDR3(互补决定区3),团队将生成结合物的氨基酸长度精准设定为7、11和15。系统为每个靶点快速生成了上百个定制化的高潜力短肽(Binder),彻底拓宽了抗体的序列空间。
第三步:高通量初筛,HDOCK 大浪淘沙
海量AI生成序列中,谁结合得最稳?严谨的计算学验证必不可少。 团队引入了高效的蛋白互作对接工具 HDOCK,对生成的短肽进行高通量虚拟初筛。通过计算诱饵蛋白与候选短肽的结合自由能(Docking Score),团队优中选优,将得分最高、结合潜力最大的 Top 10 短肽挑选出来,顺利进入下一阶段的抗体工程化组装。(注:在HDOCK的评价体系中,对接分数越低代表结合越稳定,当置信度得分 > 0.7时,表示两者结合的可能性极大。)
第四步:骨架融合与定向进化,重塑纳米抗体
从“多肽”向“抗体”的跨越,这是展现技术壁垒的关键一步。 科晶生物将这10个优选短肽,精准嵌合(替换)到高稳定性纳米抗体骨架的 CDR3 区域。为了进一步优化抗体的整体构象与亲和力,团队在保持 CDR3 固定的同时,对负责辅助识别的 CDR1 和 CDR2 区域进行了高频的智能模拟突变(每个抗体突变100次)。这一定向进化策略,瞬间构建出了包含上千个全新纳米抗体序列的专属突变库。
第五步:双重验证,AlphaFold3的终极校验
为了确保交付给客户的每一个序列都具备高度的成药潜力与实验可行性,科晶生物特设了严苛的“干实验双重验证”机制:
- HDOCK 二次精筛: 对上千个突变后的纳米抗体再次计算结合能。数据显示,突变库中绝大多数候选者轻松达到了优异的结合阈值(< -200),且在结合区域形成了致密的氢键网络,呈现出高度稳定的构象。
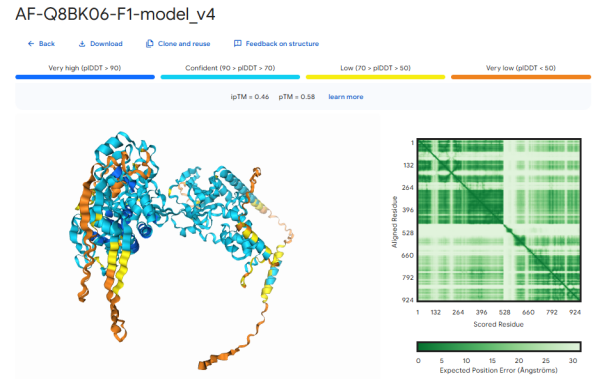
- AlphaFold3 精细建模: 提取 HDOCK 筛选出的 Top 20 纳米抗体,导入目前的“结构预测天花板”——AlphaFold3 (AF3) 进行一对一精准复合体建模。团队重点考量两个硬核指标:pTM(评估整体三维结构折叠准确性)与 ipTM(专项评估抗原-抗体接触界面的结构预测准确性)。
成果交付:让研发少走弯路,用数据理性决策
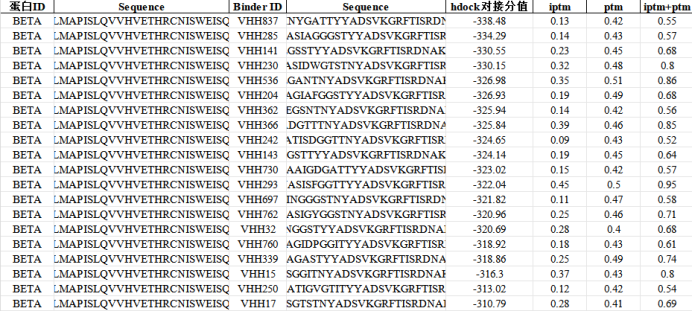
通过最终交付的数据矩阵可以看出:针对双靶点,科晶生物交付的候选纳米抗体不仅在 HDOCK 对接分值上表现极其优异(如低于-330乃至-380),且其在 AlphaFold3 验证下的 ipTM+pTM 综合得分也展现了极高的可信度。
客户无需再盲目试错,只需根据这些直观的量化指标与复合体构象,即可精准挑选出最具潜力的候选纳米抗体进入下游的湿实验验证(如SPR亲和力测定),大幅缩短了研发周期,显著降低了试错成本!
结语:携手科晶,探索数字化生物
从数据库靶点空间解析,到 RFdiffusion 的创新生成;从定向智能突变,再到 AlphaFold3 的精准预测,科晶生物已为您打通了一条成熟、高效、具备严谨物理逻辑的计算介导大分子发现闭环链路。
无论您是进行创新药物研发、靶点机制验证,还是体外诊断试剂开发,科晶生物都将为您提供专业的数字化生物计算支持。摆脱免疫限制,挑战困难靶点,让前沿AI技术为您装上科研与研发的加速引擎!
参考文献背书:
1.Watson, J. L., et al. (2023). De novo design of protein structure and function with RFdiffusion. Nature, 620, 1089-1099.
2.Haley, O. C., Harding, S., Sen, T. Z., Woodhouse, M. R., Kim, H.-S., Andorf, C. (2024). Application of RFdiffusion to predict interspecies protein-protein interactions between fungal pathogens and cereal crops. bioRxiv, doi: 10.1101/2024.09.17.613523.
3.Watson, J. L., Juergens, D., Bennett, N. R., Trippe, B. L., Yim, J., Eisenach, H. E., ... & Baker, D. (2023). De novo design of protein structure and function with RFdiffusion. Nature, 620(7685), 1089-1098.
4.Baek, M., DiMaio, F., Anishchenko, I., Dauparas, J., Ovchinnikov, S., Lee, G. R., ... & Jumper, J. (2021). Accurate prediction of protein structures and interactions using a three-track neural network. Science, 373(6557), 871-876.
5.Lin, Z., Rigden, D. J., & McGuffin, L. J. (2023). Language models of protein sequences at the scale of evolution enable accurate structure prediction. Science, 379(6631), 1123-1130.
6.Dauparas, J., Anishchenko, I., Bennett, N. R., Bai, H., Ragotte, R. J., Milles, L. F., ... & Baker, D. (2022). Robust deep learning-based protein sequence design using ProteinMPNN. Science, 378(6615), 49-56.
7.Yan Y , Tao H , He J ,et al.The HDOCK server for integrated protein–protein docking[J].Nature Protocols, 2020, 15(Suppl 25):1-24.DOI:10.1038/s41596-020-0312-x.
8.Abramson, J., Adler, J., Dunger, J. et al. Accurate structure prediction of biomolecular interactions with AlphaFold 3. Nature 630, 493–500 (2024). https://doi.org/10.1038/s41586-024-07487-w.

AtomGit 是由开放原子开源基金会联合 CSDN 等生态伙伴共同推出的新一代开源与人工智能协作平台。平台坚持“开放、中立、公益”的理念,把代码托管、模型共享、数据集托管、智能体开发体验和算力服务整合在一起,为开发者提供从开发、训练到部署的一站式体验。
更多推荐
 已为社区贡献16条内容
已为社区贡献16条内容





所有评论(0)