ADC肺毒性评估新方法:人源肺泡体外模型的实验研究与分析【曼博生物官方代理Epithelix 人原代肺细胞】
一、问题提出:为什么ADC肺毒性难以预测?
抗体药物偶联物(ADC)近年来在肿瘤治疗中发展迅速,其通过“抗体+毒素”的组合,实现精准杀伤肿瘤细胞。
但在实际临床应用中,一个关键问题逐渐凸显:
👉 部分ADC会引发肺毒性,甚至发展为间质性肺病(ILD)
以T-DXd为例,其在临床中表现出良好的抗肿瘤效果,但同时也存在一定比例的肺毒性风险。
问题在于:
- 传统动物模型难以复现该类毒性
- 单一体外模型无法反映“器官间相互作用”
因此,如何建立更接近人体真实环境的模型,成为研究重点。
二、解决思路:构建“肺-肿瘤”共培养体系
为解决上述问题,研究人员设计了一种多组织联动的体外模型:
👉 人源肺泡模型 + 肿瘤球状体共培养系统
其核心思路是:
- 利用肺泡上皮与内皮细胞构建气液界面模型
- 通过微囊技术引入HER2阳性肿瘤球
- 在同一体系中模拟药物在不同组织间的作用
三、实验体系与检测指标
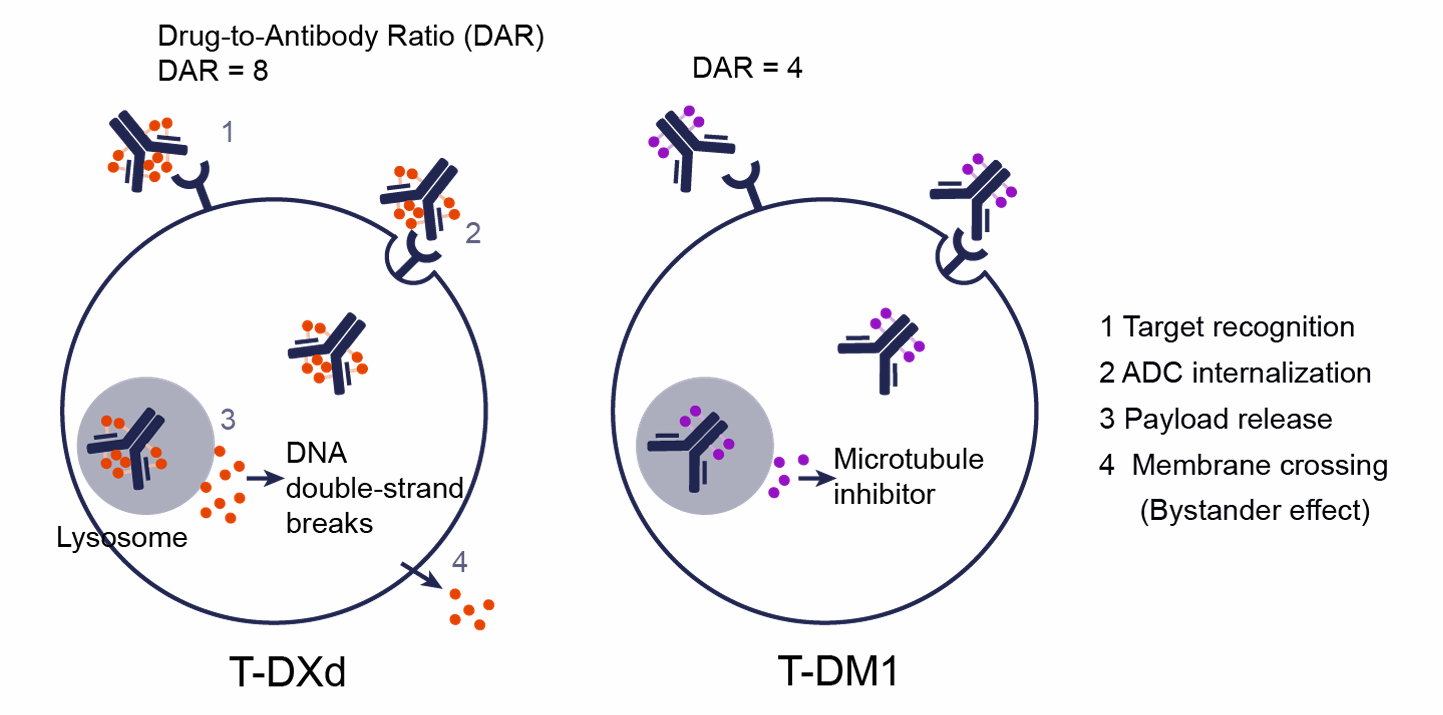
图1:ADC作用机制示意
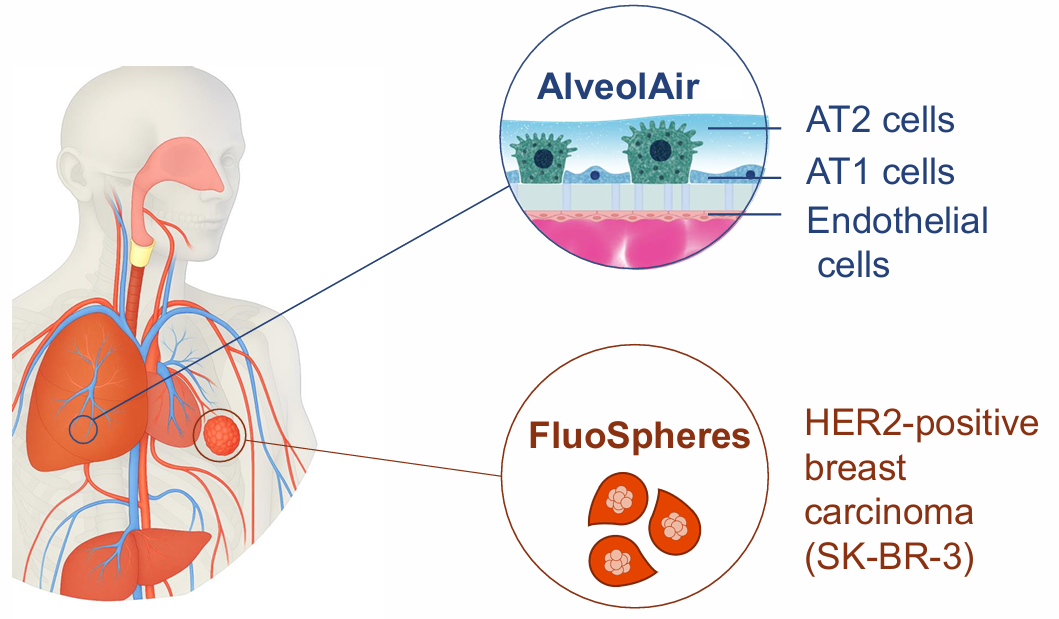
图2:肺泡模型与肿瘤球共培养体系
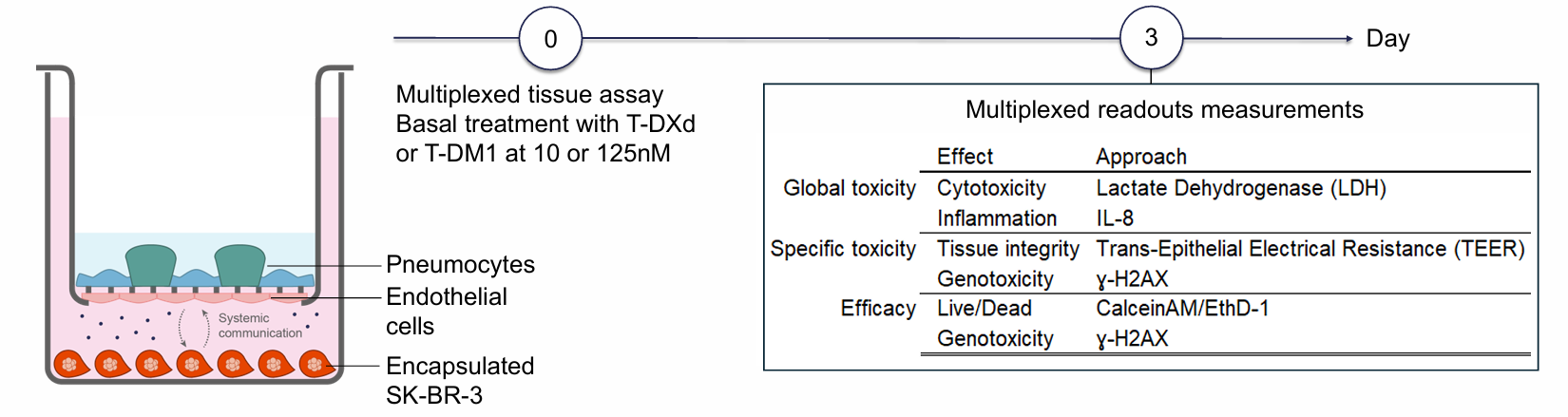
图3:实验流程与指标
实验主要评估:
- 细胞毒性
- 炎症反应(IL-8)
- 屏障功能(TEER)
- DNA损伤(γ-H2AX)
四、实验结果解析
1. 不同ADC的肺毒性差异
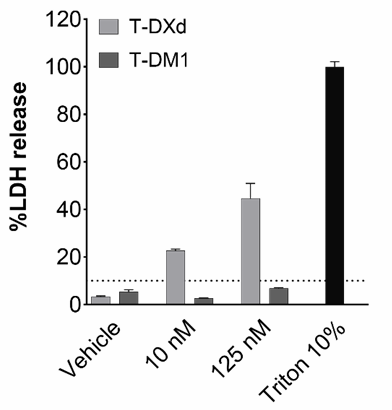
结果显示:
- T-DM1基本未表现明显毒性
- T-DXd表现出明显剂量依赖毒性
👉 说明:不同ADC在脱靶器官中的安全性差异显著
2. 炎症反应机制
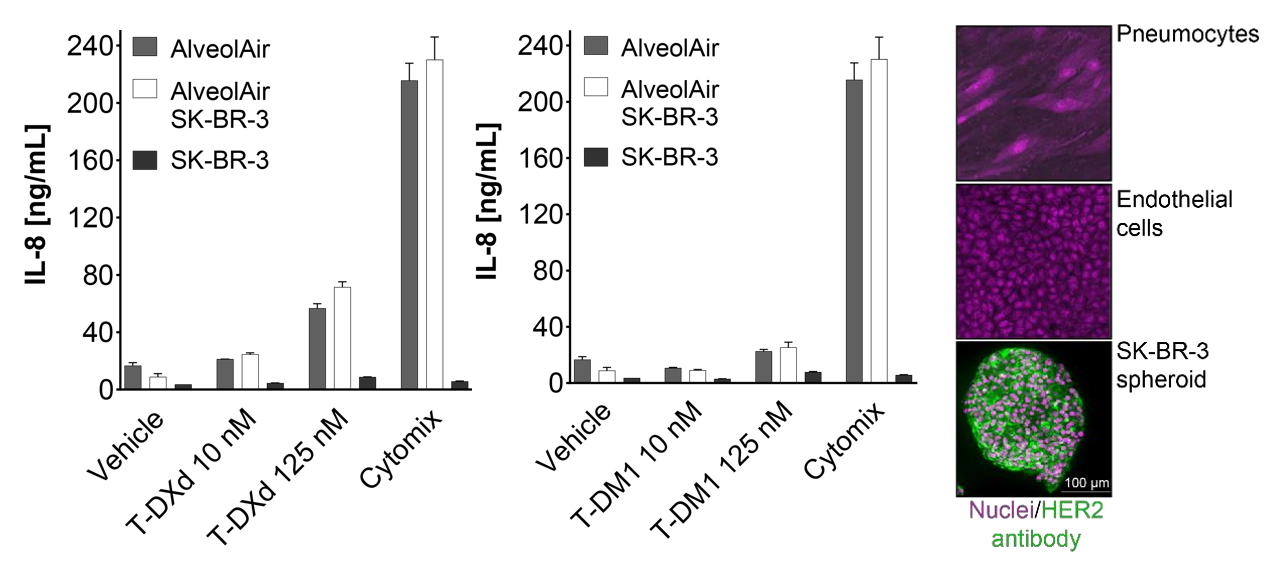
观察到:
- T-DXd可诱导IL-8释放
- 即使无肿瘤存在,仍会发生
👉 提示:存在非靶向直接毒性
3. 肺组织结构损伤
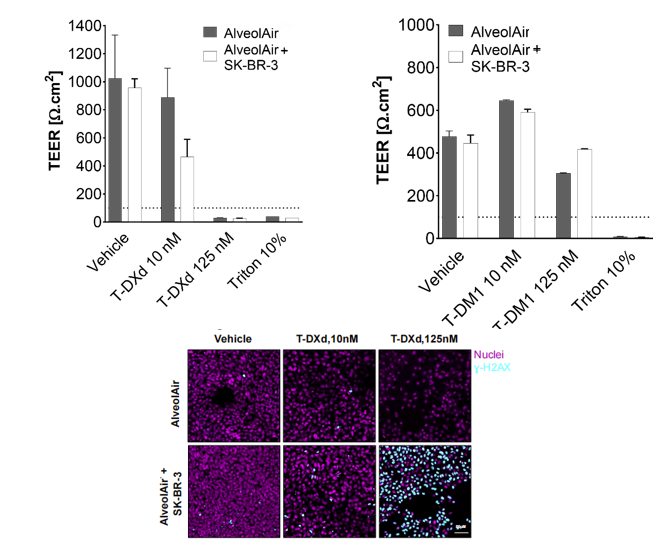
实验表明:
- 肺泡结构完整性下降
- DNA双链断裂增加
👉 且在共培养体系中损伤更明显
4. 抗肿瘤效果对比
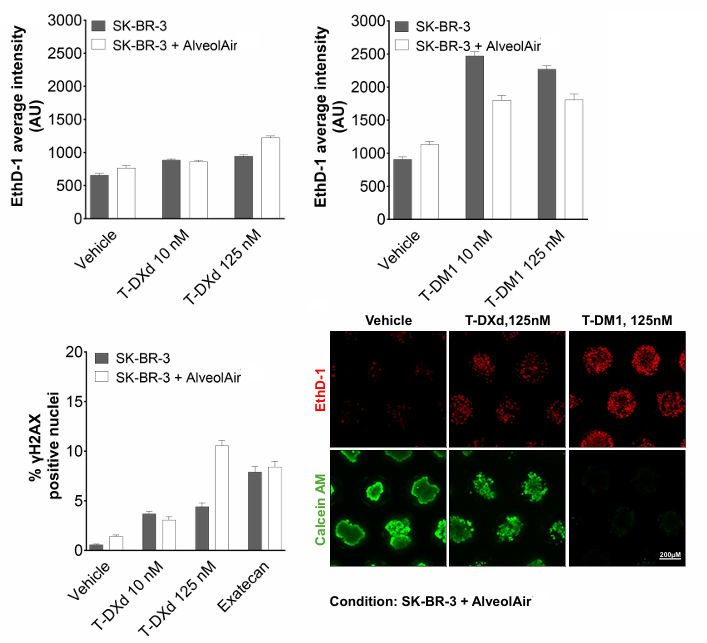
结果分析:
- T-DM1:诱导细胞凋亡
- T-DXd:主要抑制细胞增殖
👉 特别发现:
肺模型存在时,T-DXd抗癌效果增强
五、机制总结
该研究揭示了三类关键机制:
1. 旁观者效应
肿瘤细胞释放毒性分子影响肺组织
2. 直接肺毒性
药物可直接作用于肺细胞
3. 疗效差异机制
不同ADC作用模式存在本质区别
六、FAQ(关键问题解读)
Q1:为什么需要共培养模型?
单一组织模型无法反映药物在不同器官间的相互作用。
Q2:该模型的最大价值是什么?
可以在同一体系中同时评估:
- 药效
- 毒性
Q3:适用于哪些研究方向?
- ADC药物开发
- 器官毒性评估
- 体外模型优化
七、总结
人源肺泡共培养模型为ADC研究提供了一种更接近人体真实反应的技术路径:
- 可识别传统模型难以捕捉的毒性
- 能揭示复杂的跨组织作用机制
- 有助于提高药物安全性评估的可靠性
参考资料
[1] Ferreira Lopes et al., 2025
[2] Nature Communications, 2025
[3] Toxicology and Applied Pharmacology, 2024
(更多相关资料可参考)
https://www.mine-bio.com/EpitheliX-Sarl/?utm_source=csdn&utm_medium=referral&utm_campaign=epithelix_article

AtomGit 是由开放原子开源基金会联合 CSDN 等生态伙伴共同推出的新一代开源与人工智能协作平台。平台坚持“开放、中立、公益”的理念,把代码托管、模型共享、数据集托管、智能体开发体验和算力服务整合在一起,为开发者提供从开发、训练到部署的一站式体验。
更多推荐
 已为社区贡献34条内容
已为社区贡献34条内容





所有评论(0)