NPJ Precis Oncol(IF=8)海军军医大学附属长海医院:胰腺神经内分泌肿瘤精确分级的病理组学模型的开发与验证
01
文献学习

今天分享的文献是由海军军医大学附属长海医院等团队于2025年7月在肿瘤学领域顶刊《npj Precision Oncology》(中科院1区top,IF=8)上发表的研究”Development and validation of a pathomics model for accurate grading of pancreatic neuroendocrine tumors“即胰腺神经内分泌肿瘤精确分级的病理组学模型的开发与验证,该研究构建并验证了一种基于H&E染色全切片图像(WSIs)的病理组学模型,用于胰腺神经内分泌肿瘤(PanNETs)的精确分级。模型通过深度学习分割肿瘤区域,提取427个病理组学特征,经LASSO回归筛选出6个关键特征构建“病理组学评分”。该评分与肿瘤分级显著相关,并能有效区分高风险与低风险患者。结合临床特征后,模型在验证集和测试集中的AUC分别达到0.85和0.93,优于传统临床模型。
创新点:①首次实现PanNETs H&E全切片图像自动精准分割与量化,提取人眼无法识别的病理特征。②提出“病理组学评分”新指标,整合形态、纹理与拓扑特征,全面评估肿瘤异质性与风险分层。③构建融合病理组学评分与临床特征的模型,显著提升G分级预测准确性(AUC达0.93)。
临床价值:①辅助医生精准分级,为患者提供个体化治疗方案,改善预后管理。②避免耗时且昂贵的Ki-67免疫组化染色,仅用常规H&E切片即可高效诊断。③有效预测患者无进展生存期(PFS),识别高风险人群,指导术后随访与治疗决策。
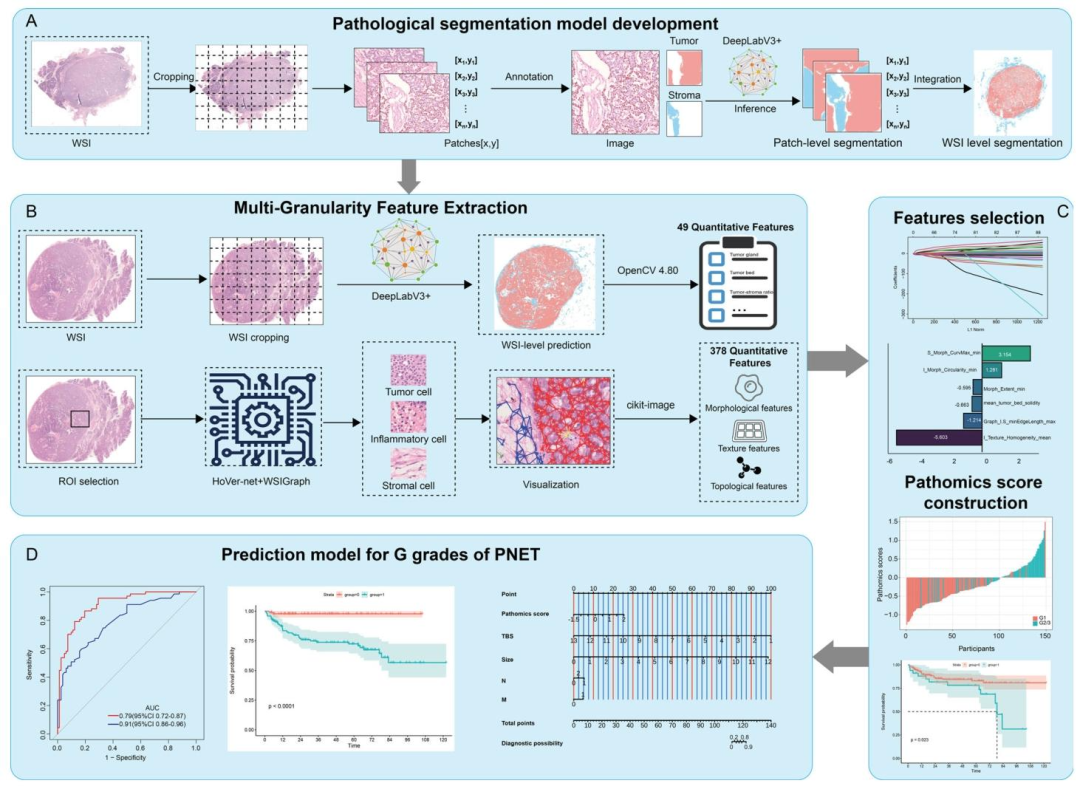
图 6:病理组学模型开发的工作流图
A:病理分割模型的开发
核心步骤:WSI→切割为256×256像素Patch→病理医生标注(Labelme工具)→DeepLabv3+模型训练→Patch级分割→WSI级分割整合→肿瘤/基质精准分割;
关键技术:数据增强(随机翻转、缩放、裁剪)、SGD优化器、交叉熵损失函数、IoU评估。
B:多粒度特征提取
基于分割结果提取两类特征:
定量特征(49个):肿瘤、肿瘤床、肿瘤-基质比相关的面积、体积等;
单细胞特征(378个):基于HoVer-Net的核分割和分类,提取形态学、纹理、拓扑特征;
关键工具:OpenCV 4.8.0、WSI Graph、sc_MTOP。
C:特征选择与病理组学评分构建
核心步骤:427个初始特征→去除近零方差特征(189个)→剔除高度相关特征(63个)→10折交叉验证LASSO回归→6个核心特征→基于特征系数构建病理组学评分公式。
D:PanNETsG分级预测模型的开发
分两个模型开发:
临床模型:纳入肿瘤大小、T/N/M分期、TBS→多因素逻辑回归;
病理组学模型:在临床模型基础上加入病理组学评分→多因素逻辑回归;
模型验证:ROC、DCA、KM曲线、成本效益分析。
02
研究背景和目的
研究背景
胰腺神经内分泌肿瘤(PanNETs)作为消化系统恶性肿瘤的重要组成部分,其发病率随着影像学技术的进步和高分辨率体检的普及而显著上升。根据2019年世界卫生组织(WHO)分类,PanNETs被细分为G1、G2和G3三个级别,其病理分级与患者的治疗策略及预后密切相关,不同级别患者的5年总生存率差异显著。然而,当前临床分级主要依赖病理医生对核分裂象和Ki-67指数的人工计数,这一方法不仅耗时费力、成本高昂,而且由于免疫组化染色的差异和观察者间的主观性,可重复性和准确性难以保证,尤其是在G1与G2交界处的微小差异(1-5%)可能导致分级错误,进而影响治疗决策。近年来,数字病理学的快速发展催生了“病理组学”这一新兴领域,其通过从全切片图像(WSIs)中高通量提取定量特征,能够揭示肉眼无法识别的组织表型异质性。因此,亟需一种基于常规H&E染色切片的、自动化且客观的病理组学方法,以实现对PanNETs的精准分级,弥补传统病理评估的不足。
研究目的
本研究旨在开发并验证一种基于病理组学的精准分级模型,用于区分胰腺神经内分泌肿瘤(PanNETs)的G1与G2/3级别。研究团队通过整合来自两个中心、共计272名患者的H&E染色全切片图像(WSIs),首先利用深度学习模型(DeepLabv3+)对肿瘤区域、间质及肿瘤床进行自动化精确分割,随后从分割区域及单细胞层面提取了涵盖形态学、纹理学和拓扑学特征的427个病理组学特征。通过LASSO回归筛选出6个最具代表性的特征并构建了病理组学评分。该评分不仅用于评估其与病理分级的相关性,还被用于结合临床病理特征(如TNM分期、肿瘤负荷评分)建立综合预测模型。研究的核心目标是验证该病理组学模型在内部验证集和外部测试集中的分级效能,并进一步评估其与患者无进展生存期(PFS)的关联性。最终,该研究期望通过提供一种经济、高效且客观的分级工具,辅助临床进行个体化治疗决策和风险分层。
03
数据和方法
研究数据
样本量:共272例患者,来自两家医院
时间范围:2014年4月至2024年1月
分组:训练集(149例)、验证集(65例)、测试集(58例)
数据内容:H&E染色全切片图像、临床病理特征、随访数据(PFS)
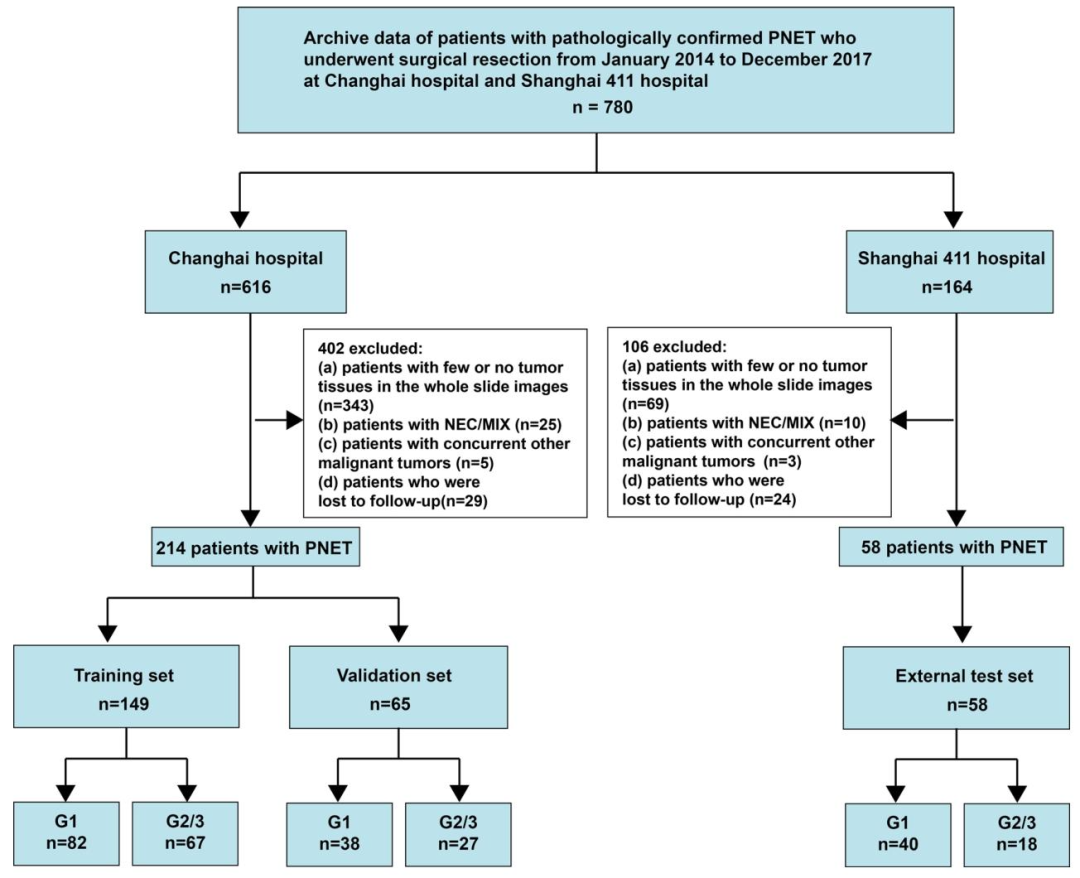
图 1:患者选择流程流程图
技术方法
图像分割:使用DeepLabv3+模型对肿瘤、基质进行语义分割(IoU > 0.88)
特征提取:提取427个病理组学特征,包括形态、纹理、拓扑特征
特征筛选与建模:LASSO回归筛选6个特征,构建“病理组学评分”
模型构建:
临床模型:基于TBS、TNM分期等
病理组学模型:临床特征 + 病理组学评分
评估指标:AUC、准确性、灵敏度、特异性、DCA、Kaplan-Meier曲线、Cox回归
成本效益分析:对比AI辅助诊断与传统病理诊断的时间和费用
04
实验结果
-
病理组学评分与G1/G2/3分级显著相关(P < 0.05)
-
病理组学模型在训练集、验证集、测试集中的AUC分别为0.91、0.85、0.93
-
模型预测的G2/3患者PFS显著更短(HR = 17.59,P = 0.01)
-
病理组学评分在生存预测中与WHO分级相当(C-index:0.88 vs 0.90)
-
AI辅助诊断时间更短(4.99 min vs 12.5 min),成本更低($17,634 vs $25,071)
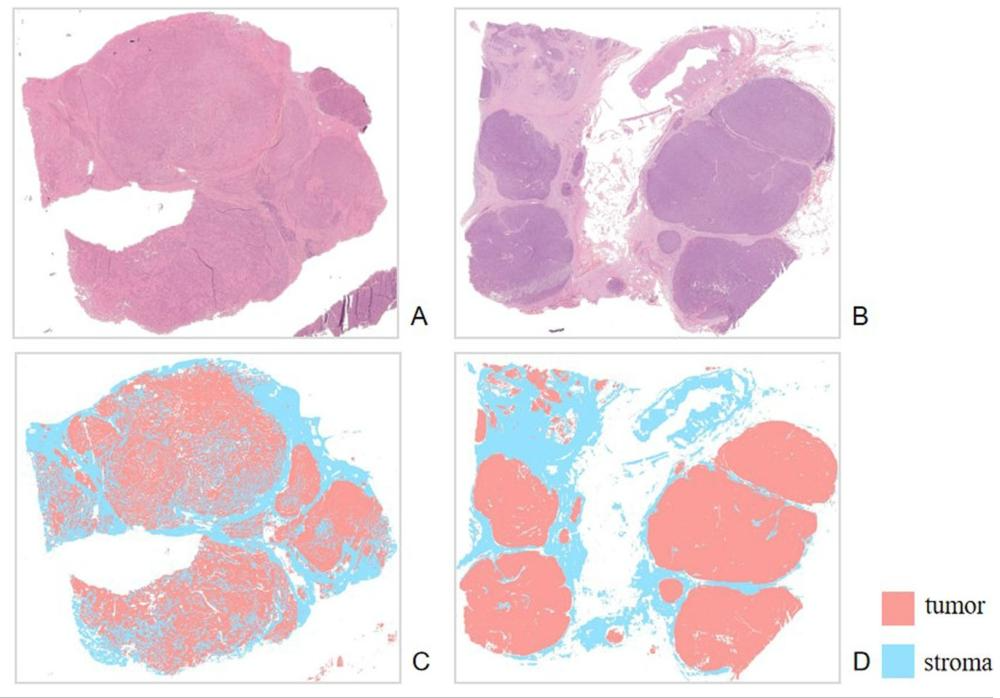
图 2:分割模型性能代表性示例
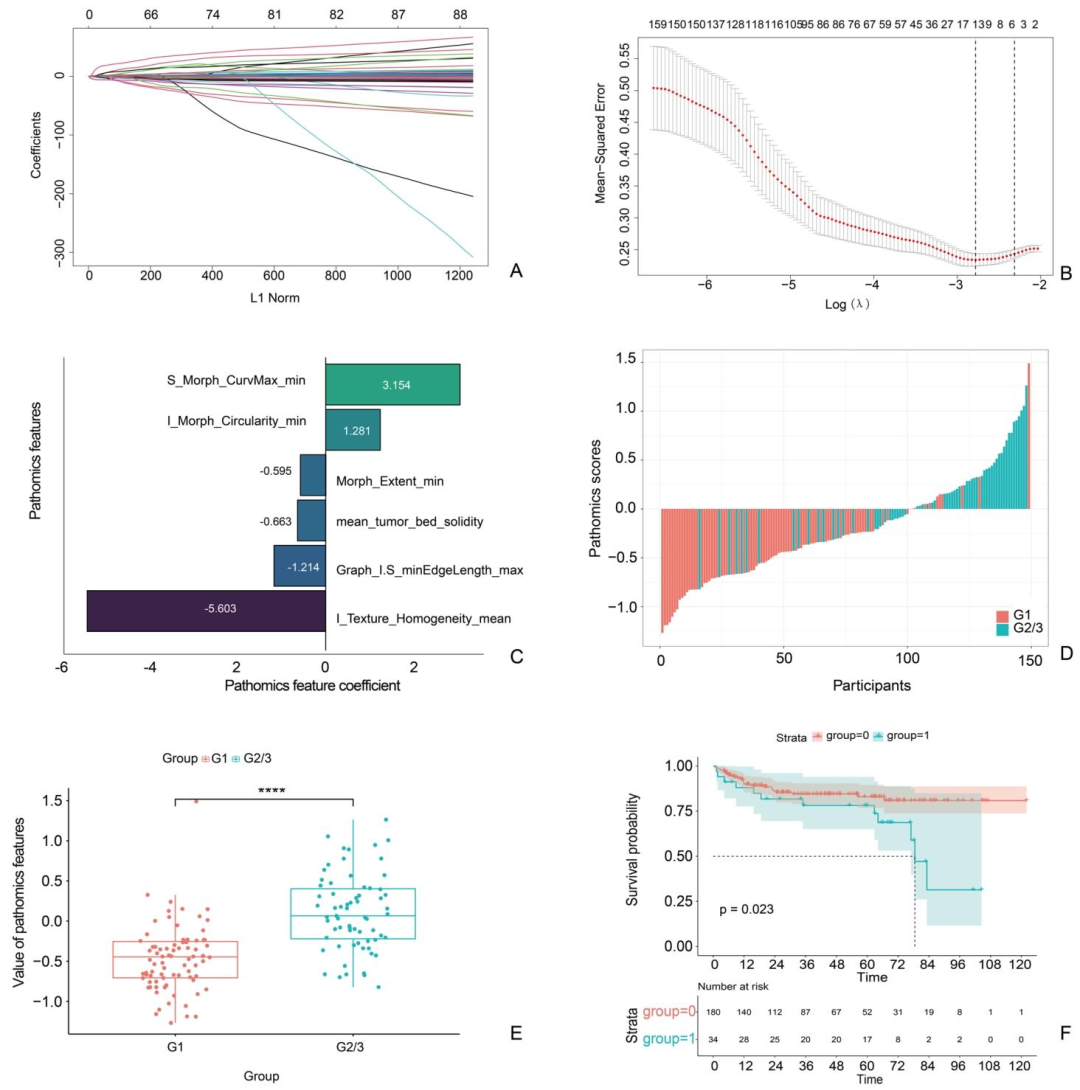
图 3:病理组学评分的开发与验证
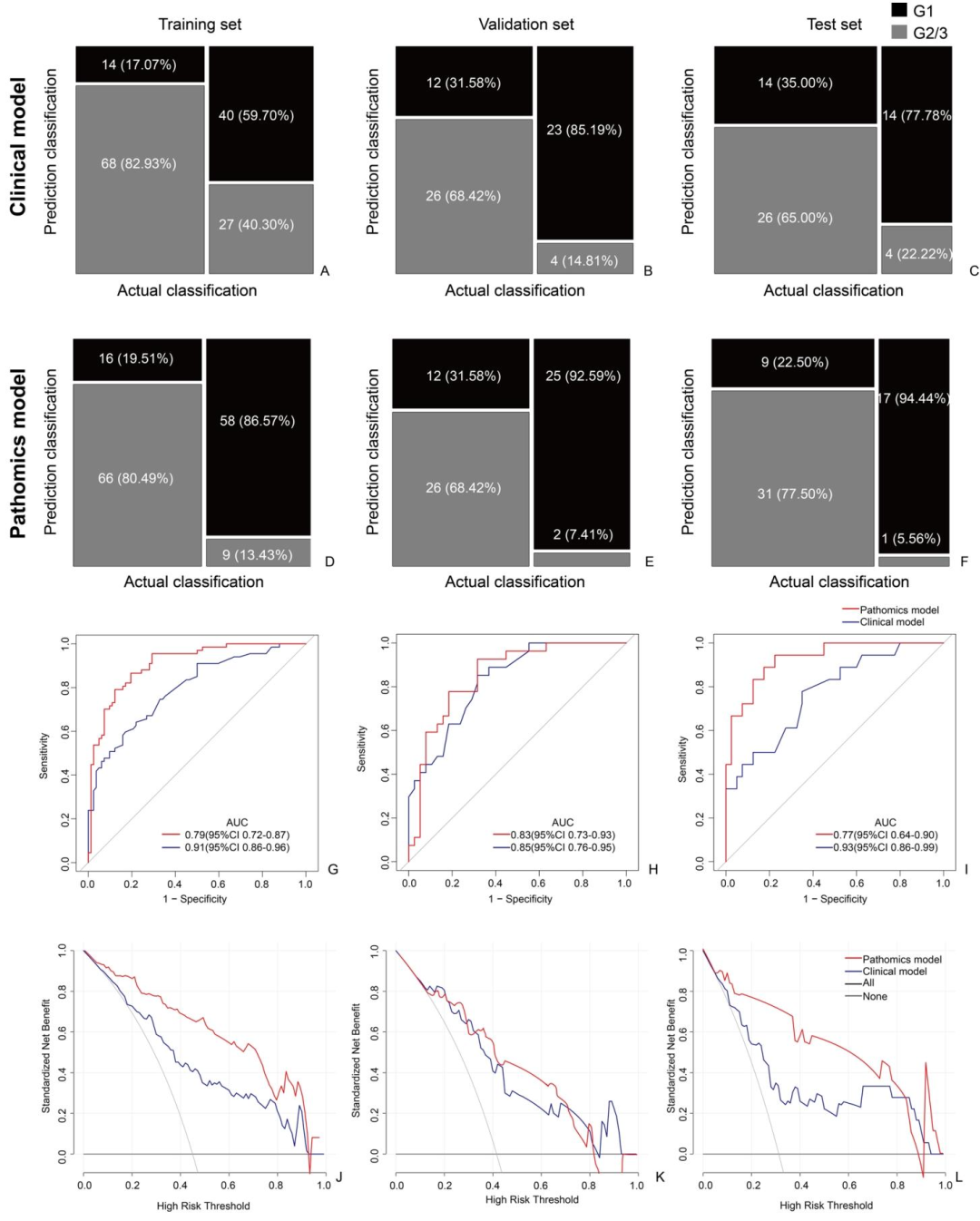
图 4:临床模型与病理组学模型的性能对比
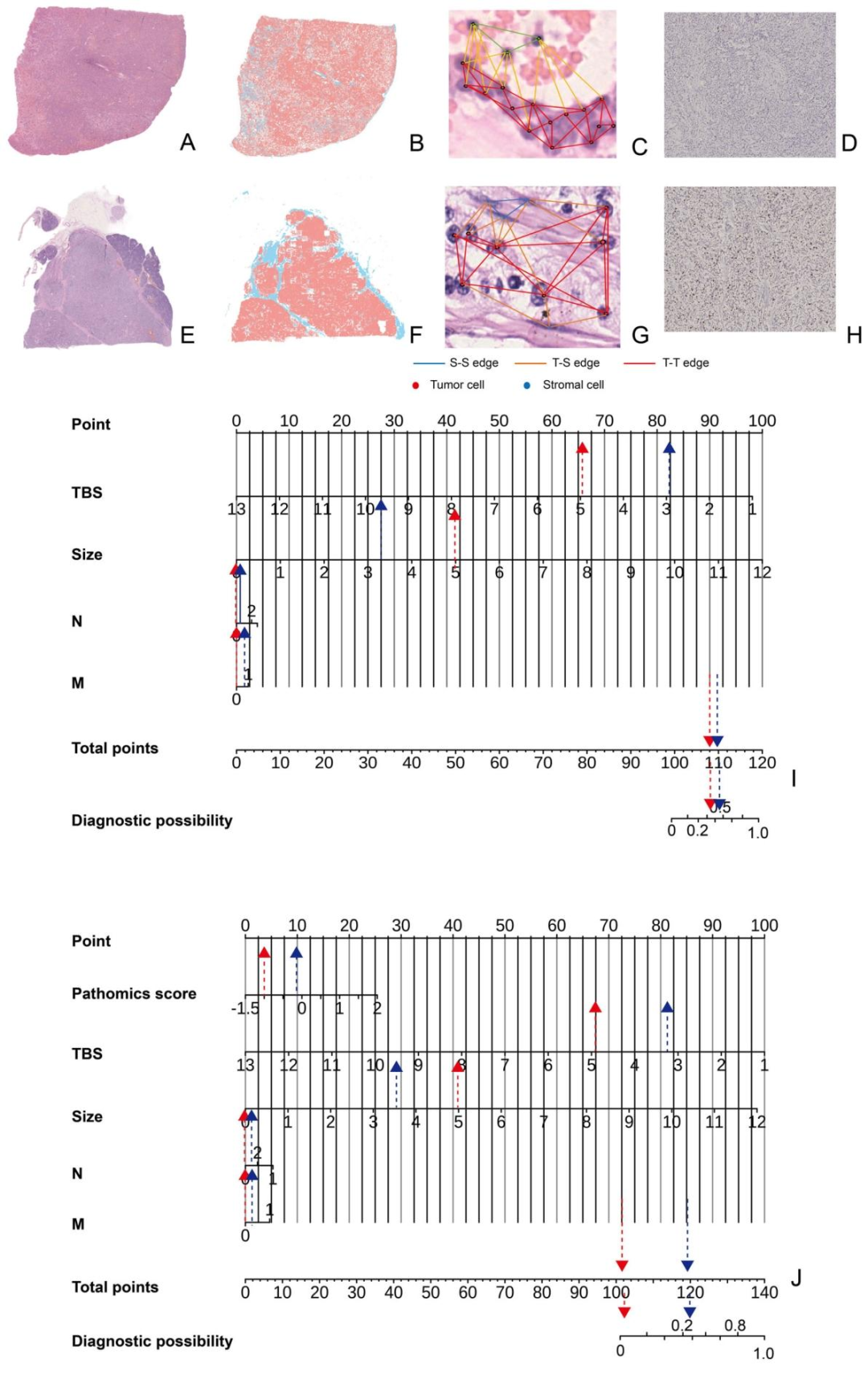
图 5:两个病例的模型诊断示例
05
研究结论
本研究成功构建并验证了一种基于H&E染色全切片图像的胰腺神经内分泌肿瘤(PanNETs)病理组学分级模型。通过对272例患者(来自两个中心)的病理图像进行精准分割与特征提取,结合LASSO回归筛选出6个关键特征构建病理组学评分。该评分与肿瘤分级显著相关,并能有效区分高风险与低风险人群(PFS差异显著)。融合病理组学评分与临床特征的联合模型在训练集、验证集和测试集中均表现出优异的区分效能(AUC分别达0.91、0.85和0.93),显著优于传统临床模型。该模型不仅可替代耗时且成本高昂的Ki-67免疫组化染色,还能提供更全面的肿瘤异质性信息,并实现实时、客观、可重复的病理分级。在生存预测方面,病理组学模型的表现与传统WHO分级相当,且在成本-效益分析中显著降低了诊断时间和费用(每例节省约7.5分钟,总成本降低约30%)。研究表明,该病理组学模型作为一种高效、经济、精准的辅助工具,有望优化PanNETs的个体化治疗决策与风险分层,尤其适用于资源有限的临床环境或形态学不明确的临界病例。
参考文献:Li Y, Chen C, Zhang Y, Yu J, Fang X, Liu F, Wang T, Li J, Wang L, Lu J, Jiang H, Shao C, Bian Y. Development and validation of a pathomics model for accurate grading of pancreatic neuroendocrine tumors. NPJ Precis Oncol. 2025 Jul 10;9(1):235. doi: 10.1038/s41698-025-01032-2.

AtomGit 是由开放原子开源基金会联合 CSDN 等生态伙伴共同推出的新一代开源与人工智能协作平台。平台坚持“开放、中立、公益”的理念,把代码托管、模型共享、数据集托管、智能体开发体验和算力服务整合在一起,为开发者提供从开发、训练到部署的一站式体验。
更多推荐
 已为社区贡献76条内容
已为社区贡献76条内容







所有评论(0)