Radiology(IF=19.7)广东省人民医院放射科刘再毅教授等团队:基于MRI的瘤内异质性定量分析预测乳腺癌新辅助化疗治疗反应
01
文献学习

今天分享的文献是由广东省人民医院放射科刘再毅教授团队联合南方医科大学南方医院、中山大学孙逸仙纪念医院、山西医科大学山西省肿瘤医院、郑州大学附属肿瘤医院等团队于2023年7月在放射学领域顶刊《Radiology》(中科院1区top,IF=19.7)上发表的研究”MRI-based Quantification of Intratumoral Heterogeneity for Predicting Treatment Response to Neoadjuvant Chemotherapy in Breast Cancer“即基于MRI的瘤内异质性定量分析预测乳腺癌新辅助化疗治疗反应,该研究为多中心回顾性研究,针对乳腺癌肿瘤内异质性(ITH)导致新辅助化疗(NAC)疗效差异大的临床问题,基于乳腺癌患者NAC前的MRI影像,提取肿瘤内生态多样性特征和传统放射组学特征,开发了ITH定量指标,并结合临床病理变量构建了7类预测模型。
创新点:①首次提出基于MRI的瘤内异质性量化指标(ITH index),通过肿瘤亚区影像特征反映肿瘤生态系统多样性。②构建融合ITH指数、常规影像组学与临床病理变量的多模态预测模型,显著提升pCR预测效能。③采用多中心大样本(1254例)及公开数据集验证模型,增强模型的泛化能力与临床转化潜力。
临床价值:①实现无创预测乳腺癌新辅助化疗疗效,辅助个体化治疗方案制定,避免无效治疗。②提供高精度pCR预测(AUC 0.83–0.90),助力患者分层管理与手术决策优化。③模型适用于不同MRI设备与协议,具备良好的临床推广性与实际应用前景。
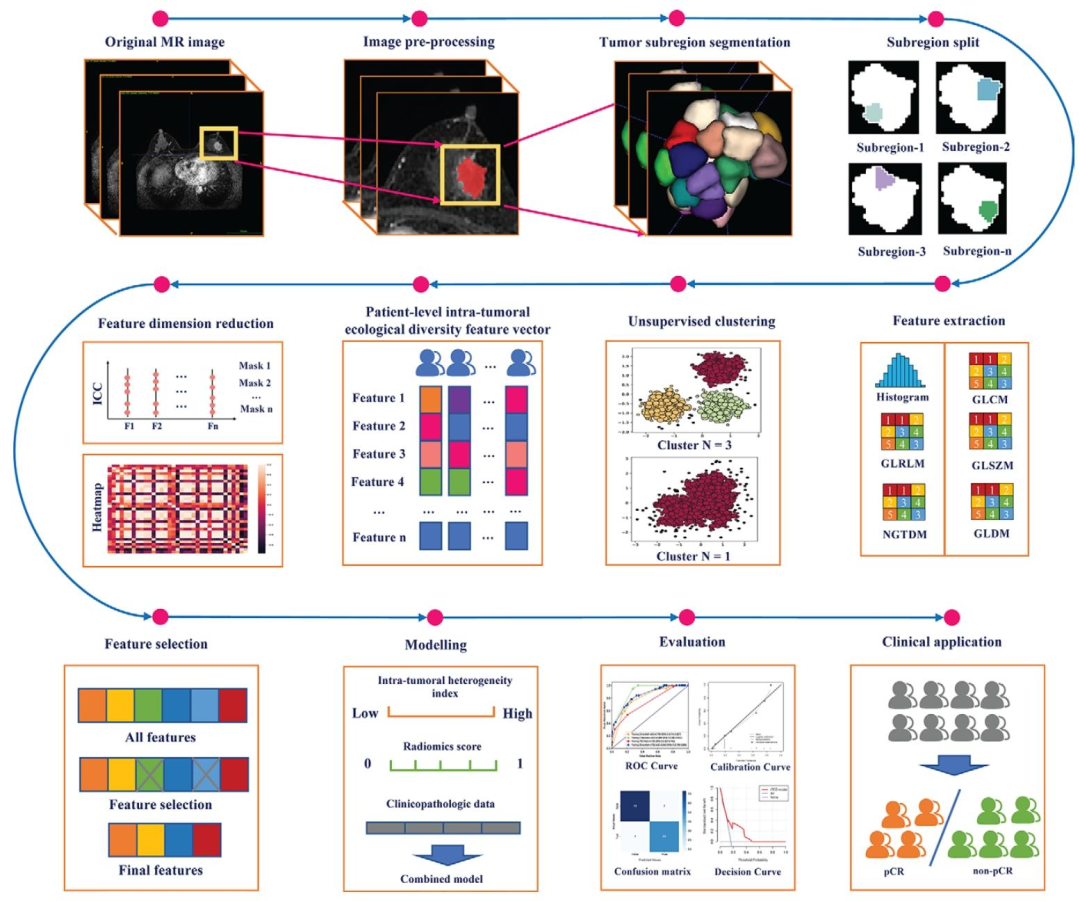
图 2:乳腺癌ITH定量评估方法的整体工作流程图
影像预处理:原始MRI影像→偏置场校正、重采样、直方图标准化等预处理,保证影像质量一致性;
肿瘤亚区分割:手动勾画肿瘤三维区域→线性交互聚类法分割肿瘤内亚区,得到多个亚区(Subregion-1~n);
特征提取与聚类:从全肿瘤/亚区提取传统放射组学(C-radiomics)特征(直方图、GLCM、GLRLM等矩阵特征)→高斯混合模型无监督聚类(聚类数1~5)→生成肿瘤内生态多样性特征向量;
特征降维与选择:通过组内相关系数(ICC)、方差分析、相关性分析、统计检验筛选高重复性、高预测性的特征;
模型构建与评分生成:分别构建ITH模型、C-radiomics模型→生成患者水平的ITH指数和C-radiomics评分→结合临床病理变量构建联合预测模型;
模型评估与临床应用:通过ROC曲线、混淆矩阵、决策曲线评估模型→最终实现乳腺癌NAC后病理完全缓解(pCR)/非pCR的分类预测,同时可对ITH进行低/高分层。
02
研究背景和目的
研究背景
乳腺癌具有高度异质性,这是导致患者对新辅助化疗(NAC)疗效差异显著的核心生物学基础。临床数据显示,仅19%-30%的患者在NAC后能达到病理完全缓解(pCR),而5%-20%的患者可能出现疾病进展。pCR是实现降阶梯手术、改善远期预后的关键指标,但目前临床实践中缺乏能够准确预测NAC疗效的标准方法或影像生物标志物。传统肿瘤标志物(如临床分期、分子分型)主要反映肿瘤整体特征,无法充分评估肿瘤内部异质性(ITH),因此预测价值有限。MRI是评估乳腺癌治疗反应最敏感的影像学手段,基于MRI的影像组学分析可提供更多肿瘤微观信息,但既往研究或未能实现ITH的定量评估,或局限于组织病理学图像。因此,开发一种无创、可重复的定量ITH评估方法,对于实现治疗前精准筛选获益人群、指导个体化治疗具有重要临床意义。
研究目的
本研究旨在开发一种基于治疗前MRI图像的肿瘤内异质性定量评估指标(ITH指数),用于预测乳腺癌患者接受NAC后能否达到pCR。研究首先通过简单线性迭代聚类(SLIC)算法对MRI肿瘤区域进行亚区域分割,提取各亚区域的常规影像组学特征后,采用高斯混合模型聚类模拟肿瘤内部“生态系统多样性”,生成反映ITH的生态多样性特征。进一步将ITH特征与常规影像组学特征及临床病理学变量(如分子分型、激素受体状态等)整合,通过多变量逻辑回归构建综合预测模型。最终在多个独立外部测试数据集(共1254例患者)中验证模型性能,评估其区分pCR的受试者工作特征曲线下面积(AUC),并明确ITH指数是否为预测pCR的独立影响因素,旨在为临床提供一种稳健、无创的疗效预测工具。
03
数据和方法
研究数据:
训练集:来自A、B两个中心的335例患者(中位年龄48岁)
外部测试集:共1254例患者,包括C中心590例、Duke公开数据集280例、I-SPY2试验数据集384例(中位年龄48岁)
时间跨度: 2000年1月至2020年9月
纳入标准:经活检证实的浸润性乳腺癌、治疗前1个月内行MRI检查、术后有NAC疗效病理评估
pCR定义:乳腺及腋窝淋巴结无浸润癌残留(允许原位癌存在,即ypT0/Tis ypN0)
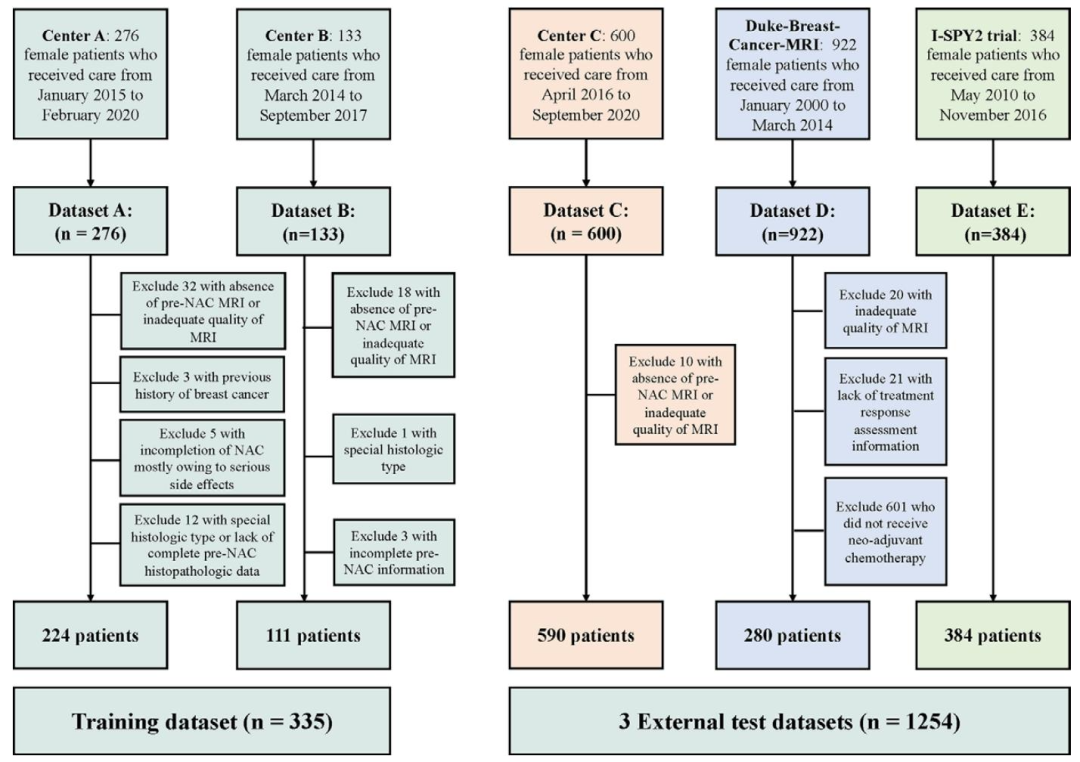
图 1:患者筛选流程图
技术方法:
肿瘤分割与亚区识别:四位放射科医师手动勾画三维肿瘤区域,采用简单线性迭代聚类(SLIC)方法将肿瘤分割为多个子区域
特征提取:
常规影像组学特征(C-radiomics):105个符合IBSI标准的特征(18个直方图特征、14个形状特征、73个纹理特征)
瘤内生态多样性特征:通过高斯混合模型对子区域聚类,基于贝叶斯信息准则确定最佳聚类数(1-5类),量化肿瘤生态系统的多样性
特征筛选:采用组内相关系数(ICC)评估观察者间重复性(生态多样性特征要求ICC>0.90,常规影像组学特征要求ICC>0.75),结合方差过滤、Pearson相关分析和假设检验进行多步降维
模型构建:建立7种预测模型(临床模型、ITH模型、C-radiomics模型、ITH-radiomics模型、临床-ITH模型、临床-radiomics模型、联合模型),采用多变量逻辑回归和决策树算法
模型评估:使用AUC、校准曲线、决策曲线分析评估模型性能,并在不同亚组(年龄、T分期、N分期、月经状态)中进行验证
可解释性分析:采用SHAP(Shapley加法解释)方法量化各特征对模型预测的贡献
04
实验结果
独立预测因子:多变量分析显示,分子亚型(OR范围:4.76-8.39)、ITH指数(OR=30.05,95%CI:8.43-122.64,P<0.001)和C-radiomics评分(OR=29.90,95%CI:12.04-81.70,P<0.001)是pCR的独立预测因子
模型性能:
ITH模型:训练集AUC=0.77,三个外部测试集AUC分别为0.76、0.74、0.75
联合模型(临床+ITH指数+C-radiomics):训练集AUC=0.90,外部测试集AUC分别为0.87、0.85、0.83
亚组分析:联合模型在各亚组中均表现稳健(AUC范围0.78-0.88)
临床效用:决策曲线分析显示,联合模型在广泛的阈值概率范围内(5%-88%)具有更高的净收益
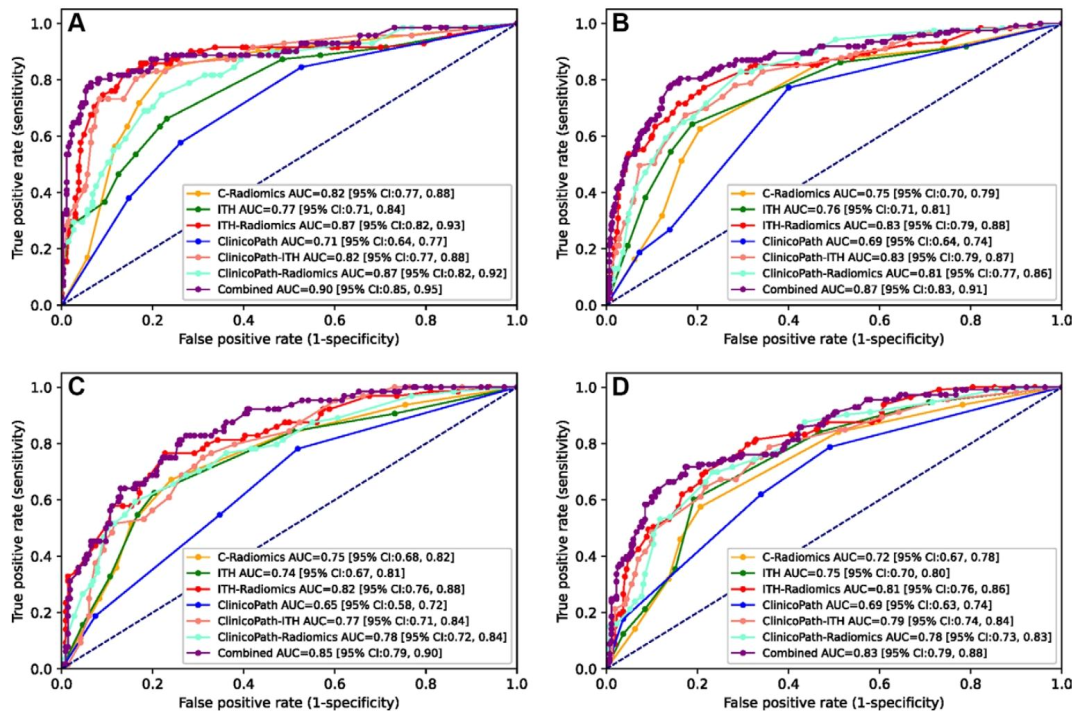
图 3:7个预测模型在训练集及外部验证集的ROC曲线对比图
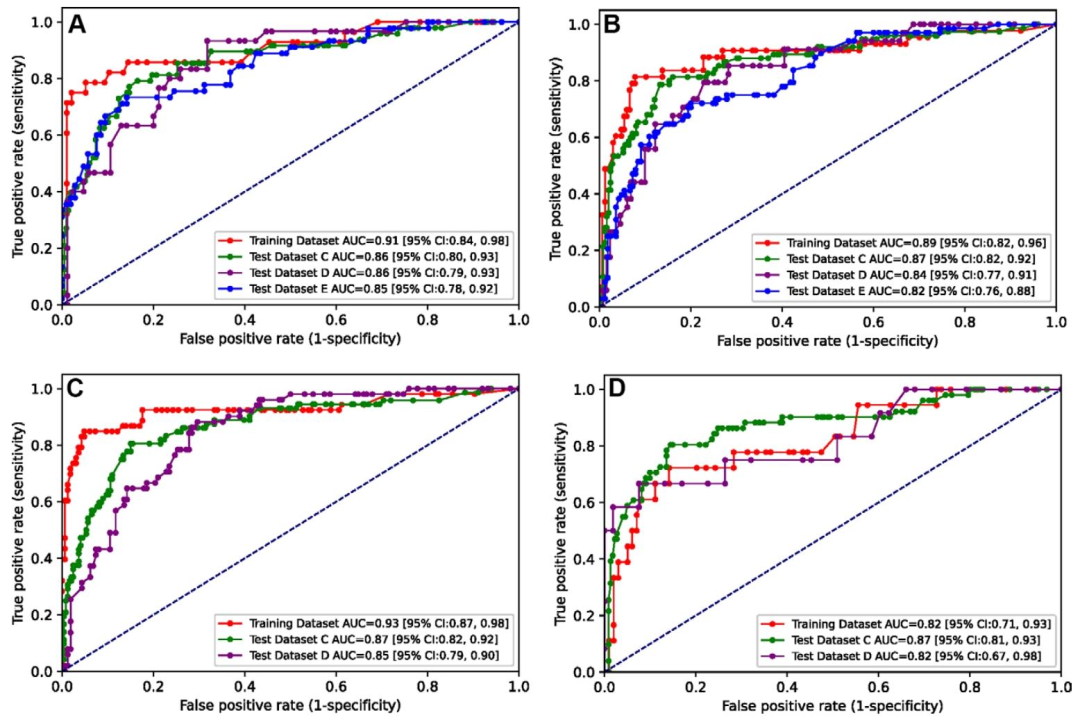
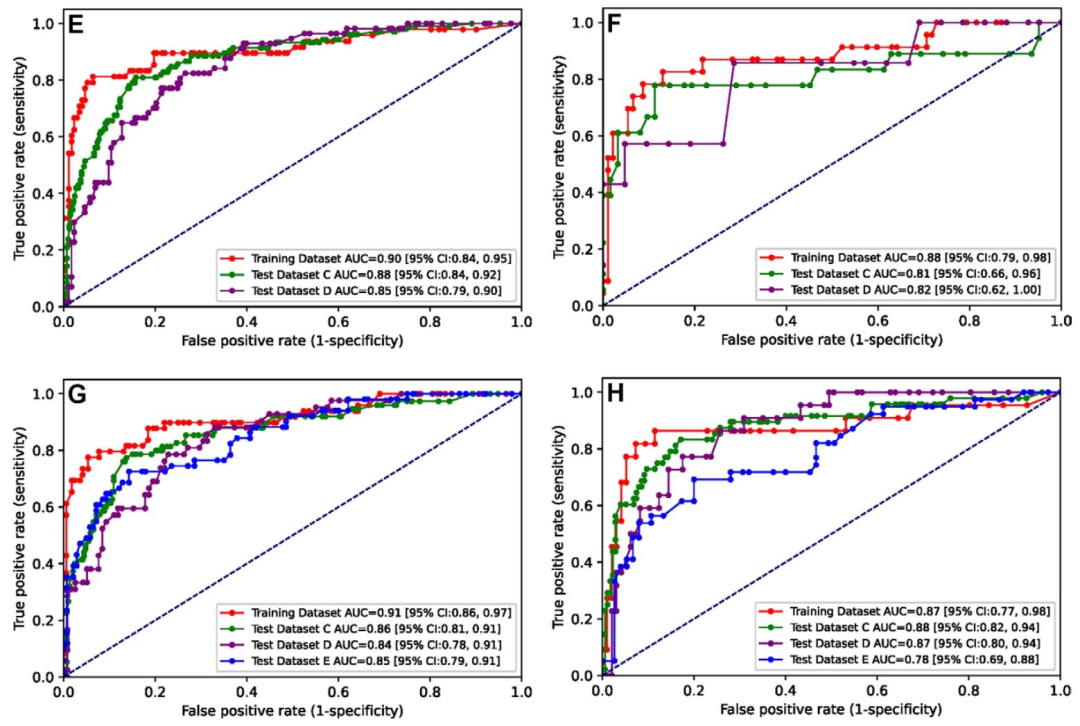
图 4:联合模型在不同患者亚组中的ROC曲线对比图
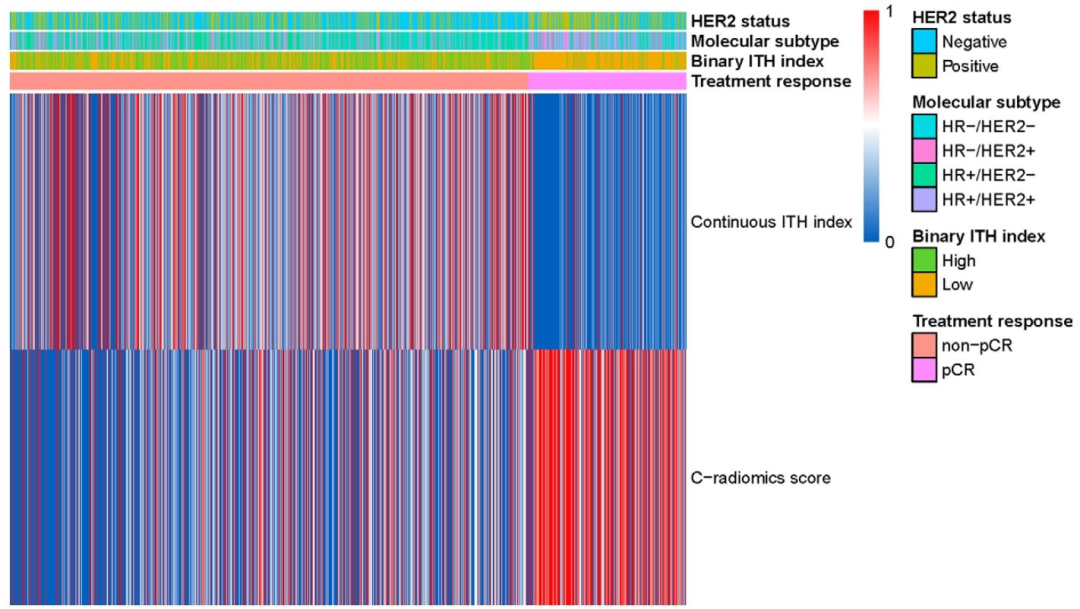
图 5:临床病理变量、MRI特征与pCR疗效的关联热图
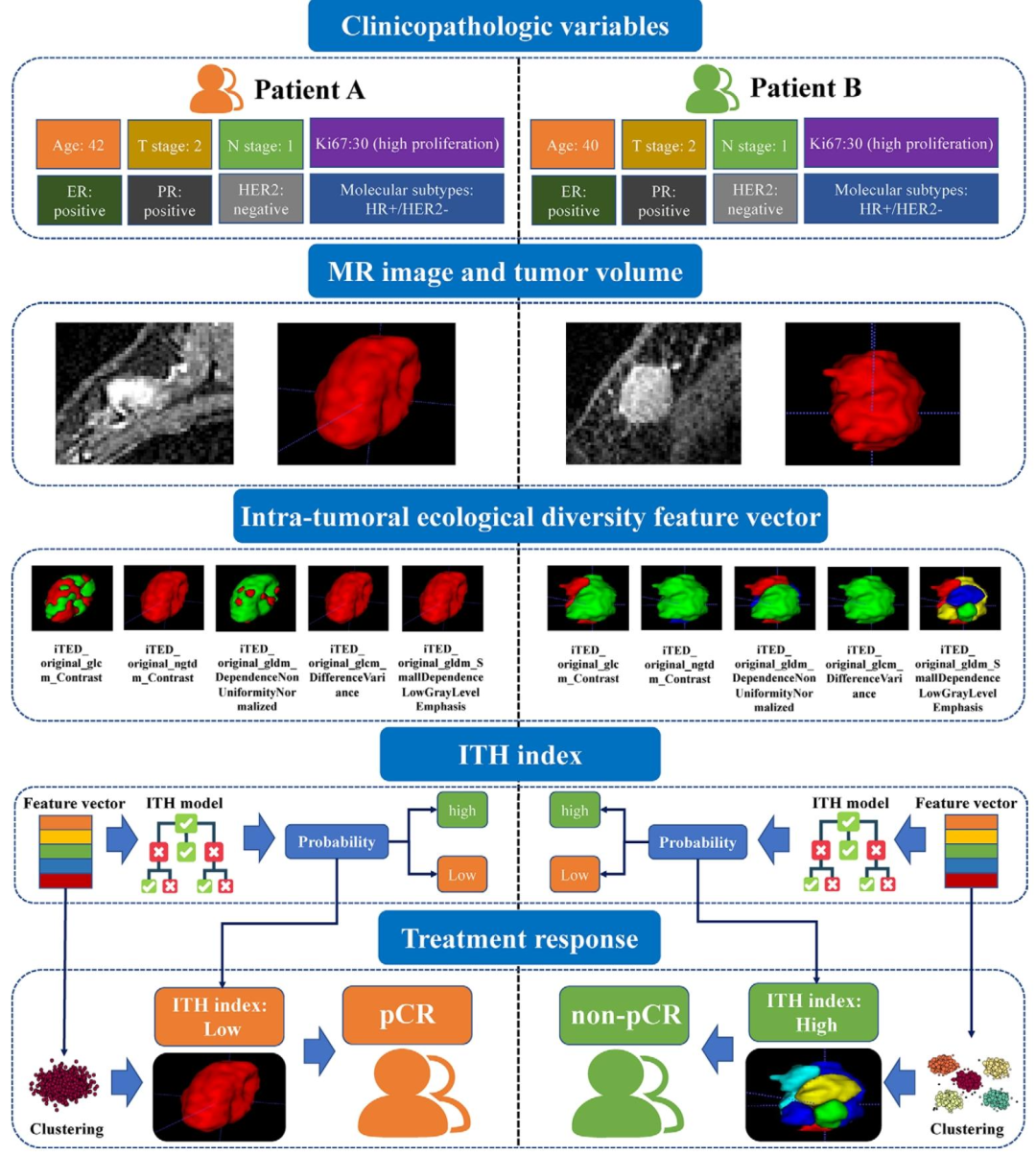
图 6:临床特征相似但ITH指数不同的乳腺癌患者案例示意图
05
研究结论
该研究通过定量分析乳腺癌新辅助化疗前MRI图像的瘤内异质性(ITH),成功构建并验证了一个预测病理完全缓解(pCR)的综合模型。研究团队从多中心及公共数据集中纳入1589例患者,基于瘤内亚区域的影像组学特征,创新性地开发了ITH指数。结果表明,ITH指数、传统影像组学评分及分子分型均是pCR的独立预测因子。单独使用ITH指数模型在三个外部测试数据集中即表现出良好的预测效能(AUC为0.74-0.76)。而将临床病理变量、传统影像组学评分与ITH指数相结合的联合模型,预测性能最佳,在训练集和三个外部测试集中的AUC分别达到0.90和0.83-0.87,显著优于单一模型。该研究证实,基于MRI的瘤内异质性量化指标能够有效捕捉肿瘤的生物学差异,将其与现有临床及影像特征融合,可显著提升对新辅助化疗疗效的预测能力,为乳腺癌的精准治疗决策提供了有力的无创性工具。
参考文献:Shi Z, Huang X, Cheng Z, Xu Z, Lin H, Liu C, Chen X, Liu C, Liang C, Lu C, Cui Y, Han C, Qu J, Shen J, Liu Z. MRI-based Quantification of Intratumoral Heterogeneity for Predicting Treatment Response to Neoadjuvant Chemotherapy in Breast Cancer. Radiology. 2023 Jul;308(1):e222830. doi: 10.1148/radiol.222830. Erratum in: Radiology. 2023 Jul;308(1):e239021. doi: 10.1148/radiol.239021.

AtomGit 是由开放原子开源基金会联合 CSDN 等生态伙伴共同推出的新一代开源与人工智能协作平台。平台坚持“开放、中立、公益”的理念,把代码托管、模型共享、数据集托管、智能体开发体验和算力服务整合在一起,为开发者提供从开发、训练到部署的一站式体验。
更多推荐
 已为社区贡献15条内容
已为社区贡献15条内容





所有评论(0)