Nature正刊论文:诺奖团队揭开触觉感知的分子密码
触觉作为人类五大核心感官之一,不仅是个体与外界进行情感交互(如握手、轻抚)的重要媒介,更是人体操控工具、维持机体平衡与空间定位的基础。然而,长期以来,触觉感知的底层分子机制始终是生命科学领域悬而未决的核心谜题,阻碍了人类对机械力信号转导过程的深入理解。
这一僵局直至2010年被打破:斯克利普斯研究所的Ardem Patapoutian教授团队通过一系列分子生物学与电生理学实验,首次鉴定出PIEZO基因家族编码的哺乳动物机械门控阳离子通道——PIEZO1与PIEZO2,明确其作为机械力受体的核心功能:能够感知细胞膜受到的机械力变化,并将这种物理信号高效转化为细胞可识别的电信号或化学信号,进而调控包括人类在内的哺乳动物的触觉、痛觉、本体感觉等多种机械力感知相关的信号转导过程。该发现成功填补了哺乳动物力学感知领域的分子空白,Ardem Patapoutian教授也因此项突破性成果,荣获2021年诺贝尔生理学或医学奖。
尽管PIEZO家族的发现为触觉机制研究奠定了基础,但PIEZO2的功能与结构关联性仍处于未知状态。已有研究证实,PIEZO2的基因突变会导致广泛的机械力感知缺陷,甚至引发多种衰弱性神经系统疾病;即便近年来科研界对PIEZO2的生理作用已有诸多探索,但其如何精确感知并响应机械力、实现触觉特异性识别的核心机制,仍是亟待破解的科学难题。
2026年3月4日,Ardem Patapoutian教授作为通讯作者,在国际顶级期刊《Nature》发表题为《The molecular basis of force selectivity by PIEZO2》的研究论文,首次揭示了PIEZO2通过独特分子机制专门感知细胞压痕刺激、成为触觉“专用传感器”的核心原理,同时为解析细胞如何解码跨组织、跨器官系统的多种机械力刺激,提供了清晰的分子蓝图,推动触觉分子机制研究进入全新阶段。
同源不同功:PIEZO家族的结构共性与功能分化
在脊椎动物体内,PIEZO基因家族主要包含两个核心成员——PIEZO1与PIEZO2,二者在分子结构上具有高度同源性:均为由三个相同亚基组装形成的同源三聚体膜蛋白,整体呈三脚架结构,每个亚基均含有36个跨膜结构域,这些结构域相互折叠形成类似“叶片”的空间构象,为机械力感知提供了结构基础。
尽管结构高度相似,PIEZO1与PIEZO2的功能却存在显著分化。其中,PIEZO1主要表达于非神经元细胞(如红细胞、血管内皮细胞等),对细胞膜张力、剪切应力等多种广谱机械刺激具有敏感性,参与调控红细胞变形、血管张力调节等生理过程;而PIEZO2则主要定位于初级感觉神经元中,具有极强的功能特异性——专门感知细胞压痕刺激,这种刺激模式正是皮肤中多种机械力感受器神经元的核心检测对象,也是触觉感知的关键起始信号。
核心谜题:结构相似为何功能迥异?
PIEZO1与PIEZO2的结构同源性与功能特异性之间的矛盾,长期困扰着科研人员:为何二者具有高度相似的空间结构,却对不同类型的机械力刺激表现出截然不同的敏感性?这种“力选择性”的分子基础是什么?
原子力显微镜实验结果为这一谜题提供了初步线索:在异源细胞表达体系中,PIEZO2对压痕刺激的敏感性约为PIEZO1的3倍;但在细胞贴附式膜片钳或剥离式膜片钳记录中,PIEZO2对膜张力的敏感性却显著降低,与PIEZO1形成鲜明对比。更令人困惑的是,在细胞贴附记录中,仅有极少数表达PIEZO2的细胞能检测到机械敏感电流,且该电流强度始终处于较低水平。这些实验现象表明,PIEZO2的激活机制可能不完全依赖于经典的“源于脂质的力机制”(force-from-lipid mechanism)——即细胞膜脂质分子的机械张力或曲率变化作用于膜蛋白,引发其构象改变进而激活通道。这一推测,为后续研究指明了方向。
关键突破:PIEZO2的独特刚性与构象特性
为破解PIEZO家族的力选择性谜题,研究团队整合了多种前沿技术手段,包括单分子MINFLUX荧光纳米显微镜、全细胞膜片钳电生理学、蛋白质交联质谱等,首次在完整细胞内精准测量了PIEZO2的构象状态。这些技术的联合应用,实现了对单个PIEZO通道远端叶片结构域之间三维距离的精准检测,进而建立起PIEZO2构象变化与通道门控之间的直接关联,为解析其力感知机制提供了关键实验依据。
研究团队发现,与PIEZO1相比,PIEZO2在无机械刺激的静息状态下,其叶片结构的扩张程度显著更低;更重要的是,PIEZO2的叶片结构域具有更强的构象刚性——这种刚性差异,正是二者力敏感性不同的核心原因之一:在剥离膜片中,激活PIEZO2需要更大的机械力,推测其原因是需要额外能量来弯曲刚性更强的叶片结构,使其达到通道激活所需的构象变化幅度。
进一步实验证实,膜张力刺激对PIEZO1与PIEZO2的影响存在本质差异:膜张力会显著扩张PIEZO1的叶片结构,进而激活通道;但相同强度的膜张力刺激,不仅不会激活PIEZO2,反而会使其实叶片结构平均收缩1.9纳米,这一独特现象进一步印证了PIEZO2具有区别于PIEZO1的力感知机制。
机制解析:“系绳耦合膜门控”模型的提出
该研究最具突破性的发现,是鉴定出filamin-B(FLNB)作为PIEZO2与肌动蛋白细胞骨架之间的分子锚定物。FLNB是一种经典的肌动蛋白结合支架蛋白,其核心功能是结合皮质肌动蛋白丝,并将膜蛋白稳定锚定到细胞骨架上,从而实现膜蛋白与细胞内部结构的功能联动。
基于这一发现,研究团队提出了PIEZO2力选择性的“系绳耦合膜门控”模型:PIEZO2通过FLNB与肌动蛋白细胞骨架形成紧密的连接的“系绳”结构;当细胞受到压痕刺激时,这种局部机械力会同时引发细胞膜变形和底层肌动蛋白细胞骨架的应变,由于PIEZO2与细胞骨架的紧密连接,机械力可通过细胞骨架高效传递至PIEZO2通道,使其对压痕刺激产生高度敏感性;相反,均匀的膜张力刺激无法通过这种“系绳”机制向PIEZO2传递有效信号,因此难以激活该通道——这一模型完美解释了PIEZO2对压痕刺激的特异性感知能力。
结构调控:IDR5结构域的核心作用
研究团队进一步探究了PIEZO2与FLNB、肌动蛋白细胞骨架相互作用的分子基础,发现PIEZO2的细胞内无序结构域5(IDR5)发挥着关键调控作用。实验证实,删除IDR5结构域后,PIEZO2与肌动蛋白细胞骨架的连接会被彻底破坏,其力感知特性发生显著改变,行为模式更接近PIEZO1——这一结果表明,IDR5是PIEZO2维持其力选择性的核心结构,通过介导与FLNB的结合,实现对自身构象和功能的精准调控。
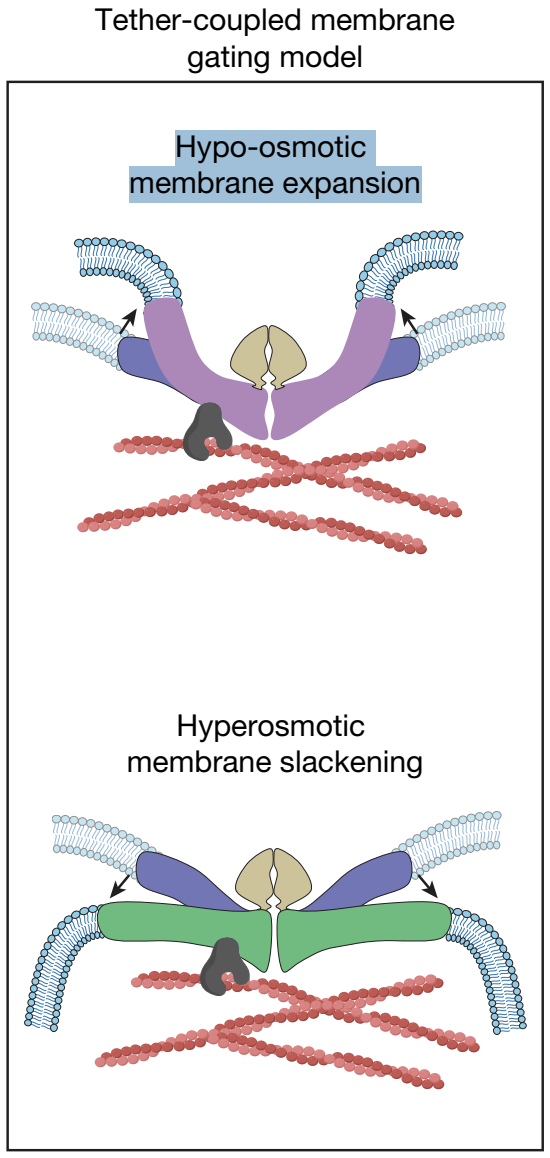
与肌动蛋白细胞骨架的连接,调控PIEZO2的结构力学
生理验证:触觉神经元中的特异性定位
为验证“系绳耦合膜门控”模型在生理环境中的适用性,研究团队针对PIEZO2与FLNB在体感神经元中的表达与定位进行了系统检测。结果显示,在小鼠背根神经节神经元细胞体中,PIEZO2与FLNB的共表达率高达95%-96%,表明二者在功能上具有高度协同性。
更关键的是,在皮肤组织中,PIEZO2与FLNB在两种专门的机械力感受器末端实现共同定位:一种是迈斯纳小体,主要负责检测触觉和低频振动;另一种是矛状末端,环绕在毛囊周围,负责感知毛囊偏转带来的机械刺激——这两种结构均是哺乳动物触觉感知的核心功能单元,进一步印证了PIEZO2与FLNB的相互作用在触觉感知中的生理必要性。
超分辨率STED成像技术的检测结果进一步提供了直接证据:PIEZO2与FLNB之间的空间距离仅为数十纳米,这一距离范围符合蛋白质直接相互作用的空间特征,为“系绳耦合膜门控”模型提供了坚实的生理依据。
应用前景:从基础研究到临床与产业转化
PIEZO2的功能异常与多种人类疾病密切相关,其功能丧失型突变会导致广泛的机械力感觉缺陷,表现为触觉、本体感觉丧失等症状;而功能增益型突变则会引发多种遗传性疾病,包括戈登综合征、马登-沃克综合征、5型远端关节挛缩症等——这些疾病的发生,进一步凸显了PIEZO2在人类生理功能调控中的核心地位。
此次研究不仅深化了人类对触觉分子机制的认知,更为相关疾病的治疗提供了潜在的药物靶点。未来,通过靶向PIEZO2与FLNB相互作用的关键节点,可设计特异性小分子调节剂:例如,增强PIEZO2的功能可用于治疗本体感觉障碍等疾病;抑制PIEZO2的过度激活,则有望缓解机械性疼痛,为慢性疼痛的治疗提供新的思路。
除临床应用外,该研究揭示的PIEZO2“发条式”能量积累机制,还可为仿生技术的发展提供重要灵感。基于这一机制,可构建高灵敏度的人工力传感器,应用于软体机器人、可穿戴设备等领域,模拟生物体内的机械力感知系统,实现对微弱机械信号的精准检测,推动仿生工程技术的升级。
总体而言,Ardem Patapoutian教授团队的这项研究,不仅破解了触觉感知的核心分子谜题,搭建起PIEZO2结构与功能之间的桥梁,更实现了基础研究与临床应用、产业转化的有机衔接,为后续机械力感知相关领域的研究开辟了全新路径。
阅读 233
PIEZO1与PIEZO2结构差异

AtomGit 是由开放原子开源基金会联合 CSDN 等生态伙伴共同推出的新一代开源与人工智能协作平台。平台坚持“开放、中立、公益”的理念,把代码托管、模型共享、数据集托管、智能体开发体验和算力服务整合在一起,为开发者提供从开发、训练到部署的一站式体验。
更多推荐
 已为社区贡献6条内容
已为社区贡献6条内容





所有评论(0)