Lancet Digit Health 中山大学附属第六医院等团队:基于放射病理组学模型预测局部晚期直肠癌新辅助放化疗后病理完全缓解的开发和验证
01
文献学习

今天分享的文献是由中山大学附属第六医院万香波、中国科学院自动化研究所田捷教授等团队于2022年在《The Lancet Digital Health》(中科院1区top,IF=24.1)上发表的研究“Development and validation of a radiopathomics model to predict pathological complete response to neoadjuvant chemoradiotherapy in locally advanced rectal cancer: a multicentre observational study”即基于放射病理组学模型预测局部晚期直肠癌新辅助放化疗后病理完全缓解的开发和验证:一项多中心观察性研究,该研究开发并验证了一个名为 RAPIDS 的人工智能模型,整合治疗前 MRI 影像组学特征和活检组织病理组学特征,用于预测局部晚期直肠癌患者在新辅助放化疗后是否达到病理完全缓解。研究基于多中心回顾性数据进行模型训练与验证,并进一步在前瞻性观察性研究中验证其临床适用性。结果显示,RAPIDS 在多个数据集中均表现出较高的预测准确性和稳健性,优于单一模态模型。
创新点:①首次构建并前瞻性验证融合MRI影像与病理活检切片的多模态人工智能预测模型。②整合宏观影像组学与微观病理组学特征,全面捕捉肿瘤异质性,显著提升预测性能。③公开算法代码并遵循TRIPOD、CONSORT-AI等规范,增强模型透明性、可重复性与临床可信度。
临床价值:①治疗前精准预测病理完全缓解,为患者个性化选择新辅助治疗方案提供依据。②高阴性预测值可有效筛选非响应者,避免无效治疗与不必要毒性,优化医疗资源利用。③预测结果与生存预后显著相关,可作为早期预后替代指标,指导术后辅助治疗策略。
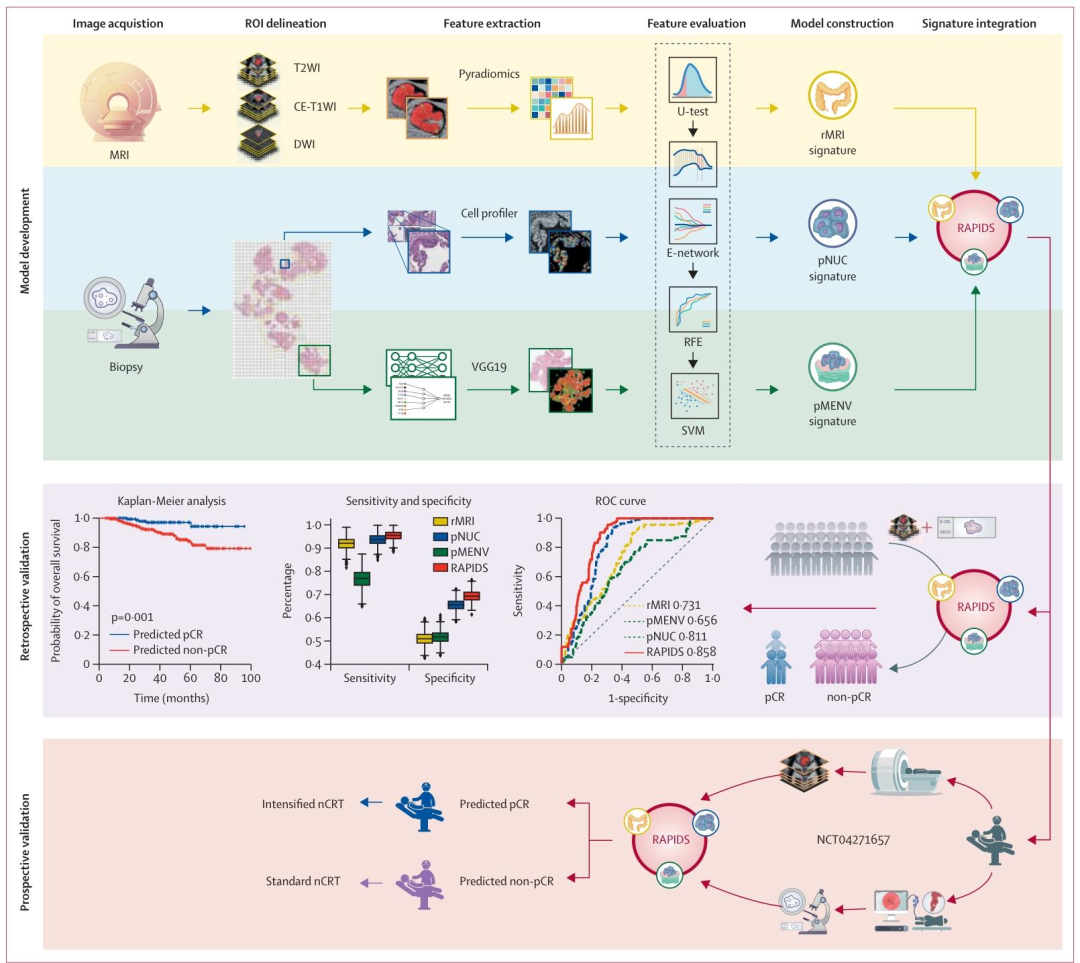
图 1:研究整体工作流程图
影像数据获取:收集患者预处理盆腔MRI(含T2WI=T2加权成像、CE-T1WI=增强T1加权成像、DWI=弥散加权成像)和活检组织H&E染色切片的全切片图像,为模型的基础数据来源。
影像分割:对MRI和病理切片进行人工勾画感兴趣区(ROI=region of interest),确定肿瘤区域,为后续特征提取划定范围。
特征提取与筛选:
从分割后的影像中提取三大类特征:rMRI(放射组学MRI特征)、pNUC(病理组学肿瘤细胞核特征)、pMENV(病理组学微环境特征);
经RFE=递归特征消除进行特征筛选,剔除冗余特征,保留与pCR(病理完全缓解)显著相关的最优特征集。
模型构建:
以最优特征集为基础,采用SVM=支持向量机算法分别构建3个单模态预测模型;
整合三大特征集的预测特征,构建RAPIDS(放射病理组学整合预测系统),输出二分类结果(预测pCR/预测非pCR)。
模型验证(研究核心验证体系,分两大阶段):
回顾性验证:将RAPIDS在两个独立的外部回顾性验证队列中进行性能测试;
前瞻性验证:将RAPIDS部署为云平台,在多中心前瞻性观察性研究(NCT04271657)中完成盲法验证,以nCRT=新辅助放化疗后手术的病理报告为金标准,评估模型预测准确性。
核心评价指标:以ROC=受试者工作特征曲线及AUC(曲线下面积)为核心指标,判断模型预测性能。
02
研究背景和目的
研究背景
局部晚期直肠癌的标准治疗方案通常为新辅助放化疗联合全直肠系膜切除术,该方案虽能实现肿瘤降期,但仅15%-27%的患者可获得病理完全缓解。病理完全缓解与良好的生存预后密切相关,此类患者或可受益于器官保留策略(如局部切除或“观察等待”),从而避免根治性手术带来的功能损害。然而,如何在治疗前准确识别出对放化疗高度敏感、有望达到病理完全缓解的患者,仍是临床亟待解决的难题。既往研究探索了血清学或基因标志物,但因成本高、缺乏前瞻性验证而未能广泛应用。近年来,基于人工智能的影像组学与病理组学在肿瘤精准诊疗中展现出潜力,影像组学可从MRI中提取肿瘤宏观异质性信息,而病理组学则能反映细胞核与微环境的微观特征。尽管已有研究分别探索了单一模态的预测价值,但将影像组学与病理组学深度融合并进行前瞻性验证的研究尚属空白。此外,既往研究多存在样本量小、回顾性设计、缺乏外部验证等问题,限制了模型的临床转化与普适性。
研究目的
本研究旨在开发并验证一个名为RAPIDS的人工智能驱动的放射病理组学整合模型,用于在治疗前精准预测局部晚期直肠癌患者接受新辅助放化疗后的病理完全缓解状态。研究团队基于回顾性队列,从患者治疗前的盆腔多参数MRI(包括T2加权成像、增强T1加权成像和弥散加权成像)以及活检组织的HE染色全切片图像中,分别提取影像组学特征、细胞核病理组学特征和微环境病理组学特征,利用机器学习方法构建多模态融合模型。为评估模型的泛化能力与临床适用性,研究在两个大型回顾性外部队列中验证其预测性能,并进一步开展多中心前瞻性观察研究,在真实临床场景中测试模型的准确性、灵敏度、特异度及阴性预测值等关键指标。通过该研究,团队期望为临床提供一种可靠、可重复且无创的预测工具,助力实现局部晚期直肠癌的个体化治疗决策,优化治疗获益与风险平衡。
03
数据和方法
研究数据
训练队列:303例(2009–2017年,中山六院)
外部验证队列1:480例(中山大学肿瘤防治中心)
外部验证队列2:150例(云南省肿瘤医院)
前瞻性验证队列:100例(2020年,四家医院)
总样本量:1033例
技术方法
特征提取:
影像组学:从 T2WI、CE-T1WI、DWI 中提取2106个特征
病理组学:提取770个细胞核特征(CellProfiler)和220个微环境特征(VGG-19)
特征筛选:通过统计检验和递归特征消除筛选出39个关键特征
模型构建:使用支持向量机构建 RAPIDS,整合三类特征
验证:回顾性外部验证 + 前瞻性多中心观察性研究
评估指标:AUC、灵敏度、特异度、PPV、NPV、NRI、IDI 等
04
实验结果
-
RAPIDS 在训练队列、验证队列1、验证队列2 的 AUC 分别为 0.868、0.860、0.872
-
在前瞻性队列中,AUC 为 0.812,灵敏度 0.888,特异度 0.740,NPV高达 0.929
-
RAPIDS 在预测性能上显著优于单一模态模型(p < 0.0001)
-
预测为 pCR 的患者预后显著更好(OS、DFS 等)
-
RAPIDS 预测标签是独立预后因素
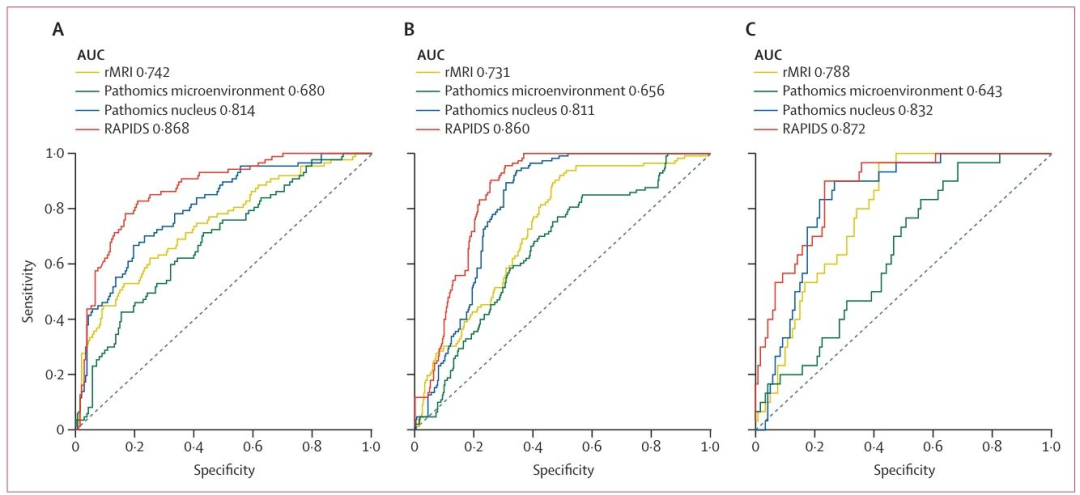
图 2:RAPIDS vs单模态模型在回顾性队列的预测性能(ROC曲线)
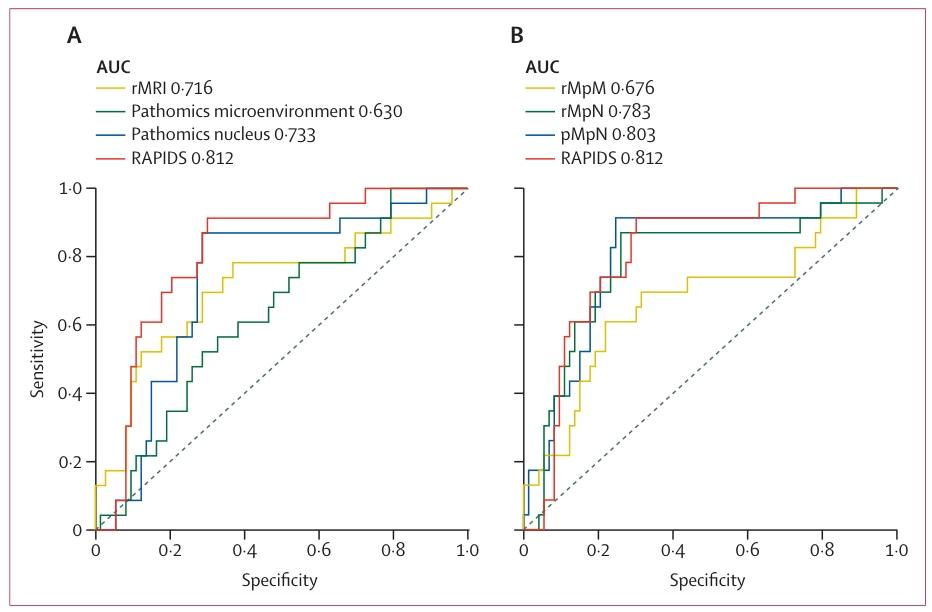
图 3:RAPIDS vs单/双模态模型在前瞻性队列的预测性能(ROC曲线)
05
研究结论
该研究成功开发并验证了一个名为 RAPIDS 的人工智能模型,该模型通过整合治疗前的 多参数MRI影像组学特征与 活检病理切片(H&E染色)的病理组学特征(包括细胞核与微环境特征),实现了对局部晚期直肠癌患者接受新辅助放化疗后能否达到 病理完全缓解的精准预测。在回顾性训练集与两个外部验证集中,模型均展现出良好的预测性能(AUC分别为0.868、0.860和0.872),并显著优于基于单一模态的预测模型。尤为重要的是,该研究通过一项多中心前瞻性观察研究进一步验证了模型的临床适用性与稳健性,AUC达0.812,敏感度高达0.888,阴性预测值达0.929,表明其在识别无法达到病理完全缓解的患者方面具有极高可靠性。研究结论指出,RAPIDS作为一种无创、高效、可重复的预测工具,能够在治疗前辅助临床决策,为不同敏感性的患者实现个体化治疗策略(如强化治疗、器官保留或降阶治疗)提供了重要依据,推动直肠癌精准医学的发展。
参考文献:Feng L, Liu Z, Li C, Li Z, Lou X, Shao L, Wang Y, Huang Y, Chen H, Pang X, Liu S, He F, Zheng J, Meng X, Xie P, Yang G, Ding Y, Wei M, Yun J, Hung MC, Zhou W, Wahl DR, Lan P, Tian J, Wan X. Development and validation of a radiopathomics model to predict pathological complete response to neoadjuvant chemoradiotherapy in locally advanced rectal cancer: a multicentre observational study. Lancet Digit Health. 2022 Jan;4(1):e8-e17. doi: 10.1016/S2589-7500(21)00215-6.

AtomGit 是由开放原子开源基金会联合 CSDN 等生态伙伴共同推出的新一代开源与人工智能协作平台。平台坚持“开放、中立、公益”的理念,把代码托管、模型共享、数据集托管、智能体开发体验和算力服务整合在一起,为开发者提供从开发、训练到部署的一站式体验。
更多推荐
 已为社区贡献20条内容
已为社区贡献20条内容






所有评论(0)