Lancet Digit Health(IF=24.1)南方医科大学南方医院等团队:基于多任务深度学习从CT影像预测胃癌腹膜复发与无病生存期
01
文献学习

今天分享的文献是由南方医科大学南方医院、斯坦福大学放射肿瘤科、中山大学肿瘤防治中心等团队于2022年5月在《The Lancet Digital Health》(中科院1区top,IF=24.1)上发表的研究“Predicting peritoneal recurrence and disease-free survival from CT images in gastric cancer with multitask deep learning: a retrospective study”即基于多任务深度学习从CT影像预测胃癌腹膜复发与无病生存期:一项回顾性研究,该研究开发并验证了一种基于术前CT影像的多任务深度学习模型,用于同时预测胃癌患者术后腹膜复发和无病生存期。研究纳入了2320名来自三家医院的患者,分为训练集、内部验证集和外部验证集。模型在预测腹膜复发方面表现出高准确性(AUC达0.84-0.86),并能独立于临床病理因素预测生存期。此外,模型还能识别哪些患者可能从辅助化疗中获益,为个性化治疗提供依据。
创新点:①首次应用多任务深度学习同步预测胃癌术后腹膜复发与生存期,多任务学习模型同时预测腹膜复发与无病生存期,提升数据效率与模型泛化能力。②结合监督对比学习与多尺度动态神经网络提取CT影像特征,采用对比学习与多尺度融合策略,显著提升模型对微小病灶的识别能力与预测精度。③AI辅助显著提升临床医生对腹膜复发的预测敏感性与一致性,AI模型辅助下,医生预测敏感性提升至90%以上,诊断一致性显著增强。
临床价值:①实现术前无创、个体化预测胃癌术后腹膜复发风险,基于常规CT影像无创预测复发风险,为高危患者早期干预提供依据。②精准筛选可从辅助化疗中获益的II/III期胃癌患者,模型识别出高风险患者化疗获益显著,低风险者无效,助力个体化治疗决策。③为腹腔热灌注等新型治疗提供患者筛选依据,识别腹膜复发高风险人群,支持腹腔热灌注等局部强化治疗的精准应用。
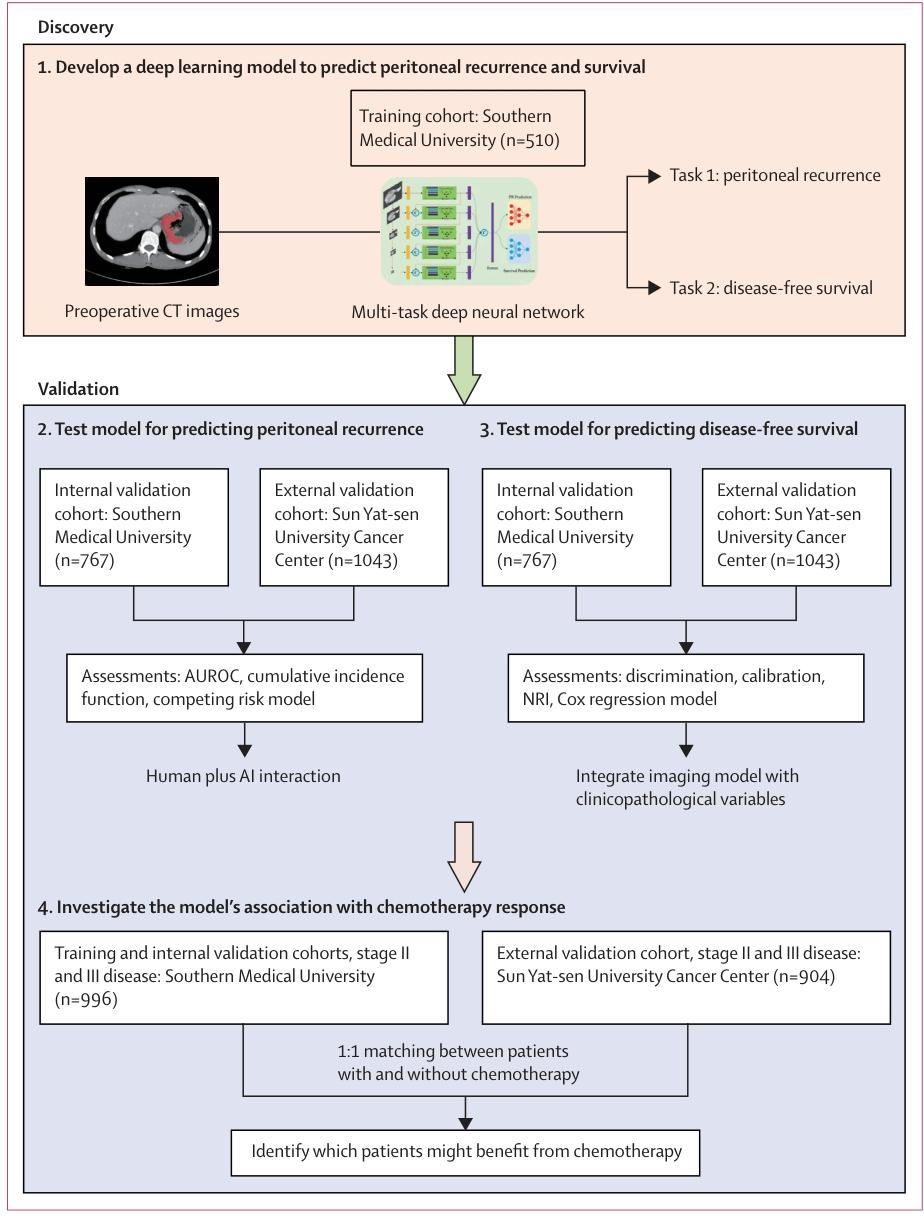
图 1:深度学习模型预测胃癌腹膜复发和无病生存期的开发与验证研究设计图
阶段1:模型开发
研究对象:训练队列(n=510);
输入数据:术前CT影像;
模型构建:多任务深度神经网络;
学习任务:同步预测任务1-腹膜复发、任务2-无病生存期。
阶段2:腹膜复发预测验证
研究对象:训练+内部+外部验证队列;
验证方法:受试者工作特征曲线(AUROC)、累积发生率函数、竞争风险模型;
评估指标:区分度、校准度。
阶段3:无病生存期预测验证
研究对象:训练+内部+外部验证队列;
验证方法:Cox回归模型、净重新分类改善指数(NRI);
核心指标:Harrell’sC指数。
阶段4:人机交互与化疗获益分析
人机交互:将影像模型与临床病理指标整合,评估AI对临床医生预测腹膜复发的辅助价值;
化疗获益分析:研究对象为II/III期患者(训练+内部验证n=996;外部验证n=904),采用1:1倾向评分匹配平衡化疗/非化疗组临床病理特征,核心目标是识别能从辅助化疗获益的患者亚组。
02
研究背景和目的
研究背景
胃癌是全球常见的恶性肿瘤,致死率高,即使接受根治性手术后,复发率依然较高,其中腹膜复发是最常见的复发模式,且预后极差,患者中位生存期仅为3至6个月。目前,全身化疗对腹膜转移的疗效有限,而新兴的治疗手段如腹腔热灌注化疗虽显示出一定的前景,但其长期生存获益尚不明确,且可能增加术后并发症风险。因此,亟需一种能够准确、个体化地预测胃癌患者术后腹膜复发风险的工具,以筛选出最可能从强化治疗中获益的高危人群,避免不必要的治疗带来的伤害。尽管深度学习在医学影像分析中已展现出潜力,但既往研究多集中于单一任务的预测(如总生存期),而针对腹膜复发这一特定且关键的临床终点,尚无基于术前CT影像的深度学习预测模型的研究报道。因此,开发一种能够同时预测腹膜复发和生存预后的非侵入性工具,对于指导临床决策具有重要的现实意义。
研究目的
基于术前CT影像,开发和验证一种多任务深度学习模型,用于同时且准确地预测胃癌患者根治术后的腹膜复发风险和无病生存期。具体目标包括:首先,在大型多中心回顾性队列中,评估该模型对腹膜复发的预测准确性,并探索其能否提升临床医生的判断能力;其次,评估模型对无病生存期和总生存期的预后价值,并验证其独立于传统临床病理因素的预测能力;最后,通过整合腹膜复发与生存风险,探索该模型在识别可从辅助化疗中获益的II期和III期胃癌患者方面的潜力,旨在为个体化治疗决策(如是否需加强全身化疗或考虑腹腔热灌注化疗)提供依据,从而推动精准医疗在胃癌治疗中的应用。
03
数据和方法
研究数据
总样本量:2320名胃癌患者
训练集:510例(2005–2012,南方医院)
内部验证集:767例(2012–2017,南方医院)
外部验证集:1043例(2007–2012,中山大学肿瘤防治中心)
所有患者均接受术前增强CT扫描和根治性胃切除术
技术方法
模型构建:采用多任务深度学习框架,结合监督对比学习与多尺度动态神经网络,同时预测腹膜复发概率与无病生存期。
模型评估:使用ROC曲线、AUC、C-index、校准曲线、NRI等指标评估模型性能。
临床应用评估:
与临床医生预测能力对比(有无AI辅助)
与临床病理指标联合建模(构建诺模图)
分析模型对化疗获益的预测能力(结合风险分层)
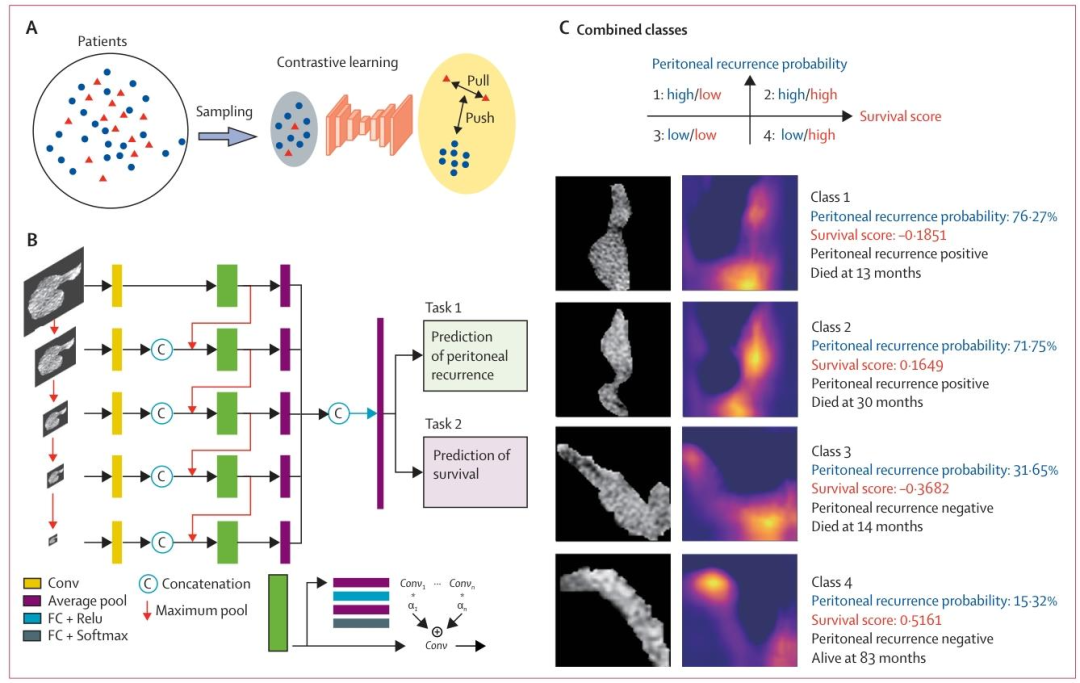
图 2:提出的多任务深度学习网络架构及预测结果可视化图
A:监督对比学习策略
B:多尺度动态神经网络架构
模型为端到端的卷积神经网络(CNN),同步完成两个任务的预测,核心结构为:
输入层:术前CT影像的多尺度特征;
卷积层(Conv):通过多轮卷积、平均池化(Average pool)、最大池化(Maximum pool)提取影像的浅层/深层特征;
全连接层(FC+Relu/Softmax):将提取的特征分别映射至任务1(腹膜复发)的概率输出(Softmax实现概率归一化)和任务2(无病生存期)**的生存评分输出;
输出层:同时给出每位患者的腹膜复发概率和生存评分,实现多任务同步预测。
C:CT影像预测结果典型案例(4类患者)
04
实验结果
腹膜复发预测:AUC在训练集、内部验证集、外部验证集分别为0.857、0.856、0.843,显著优于临床病理指标。
生存预测:C-index分别为0.654、0.668、0.610,模型独立于TNM分期等因素。
AI辅助临床决策:AI辅助下,临床医生的敏感性和一致性显著提升。
化疗获益分析:
高风险患者(高腹膜复发风险+低生存)从化疗中显著获益
低风险患者(低复发风险+高生存)未从化疗中获益
部分中风险患者(如III期)仍可从化疗中获益
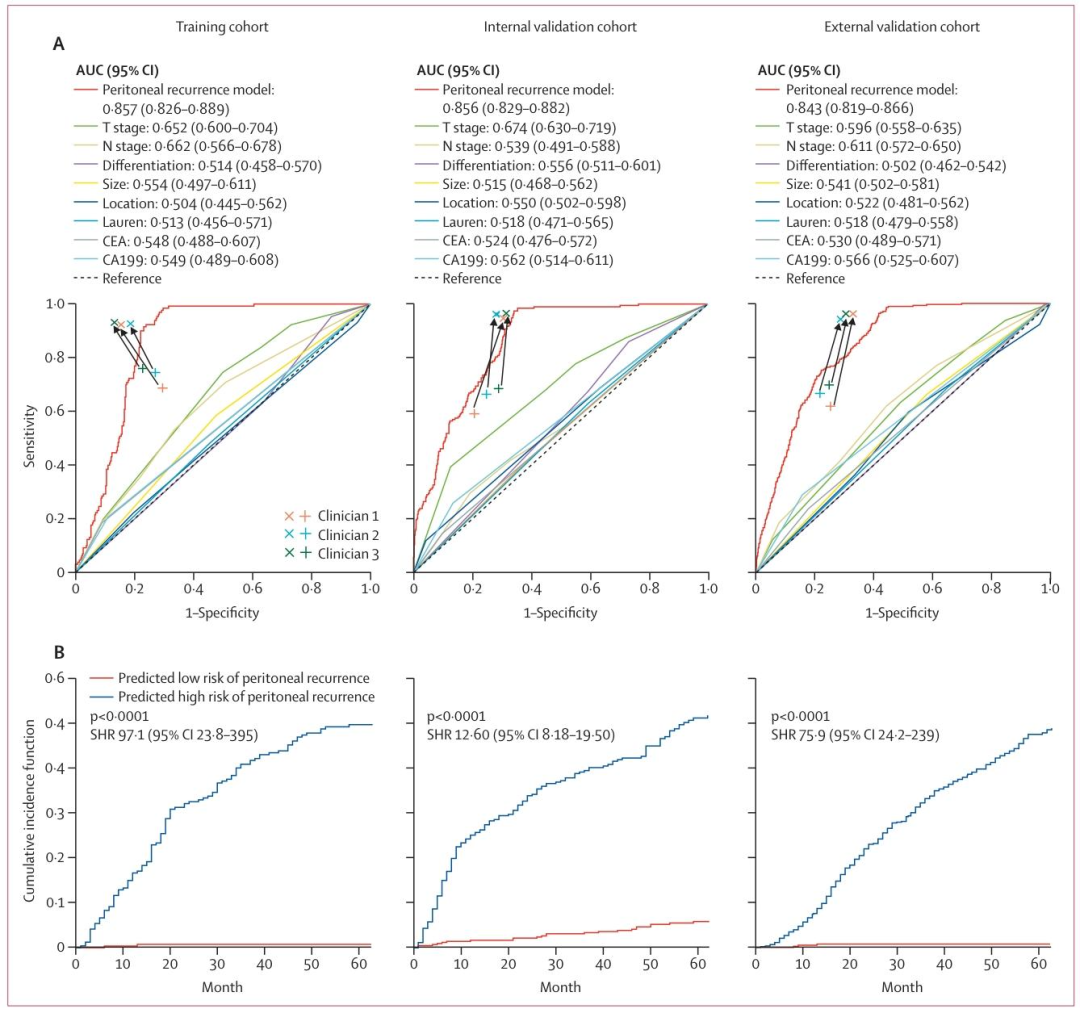
图 3:模型在训练、内部、外部验证队列中预测腹膜复发的准确性图
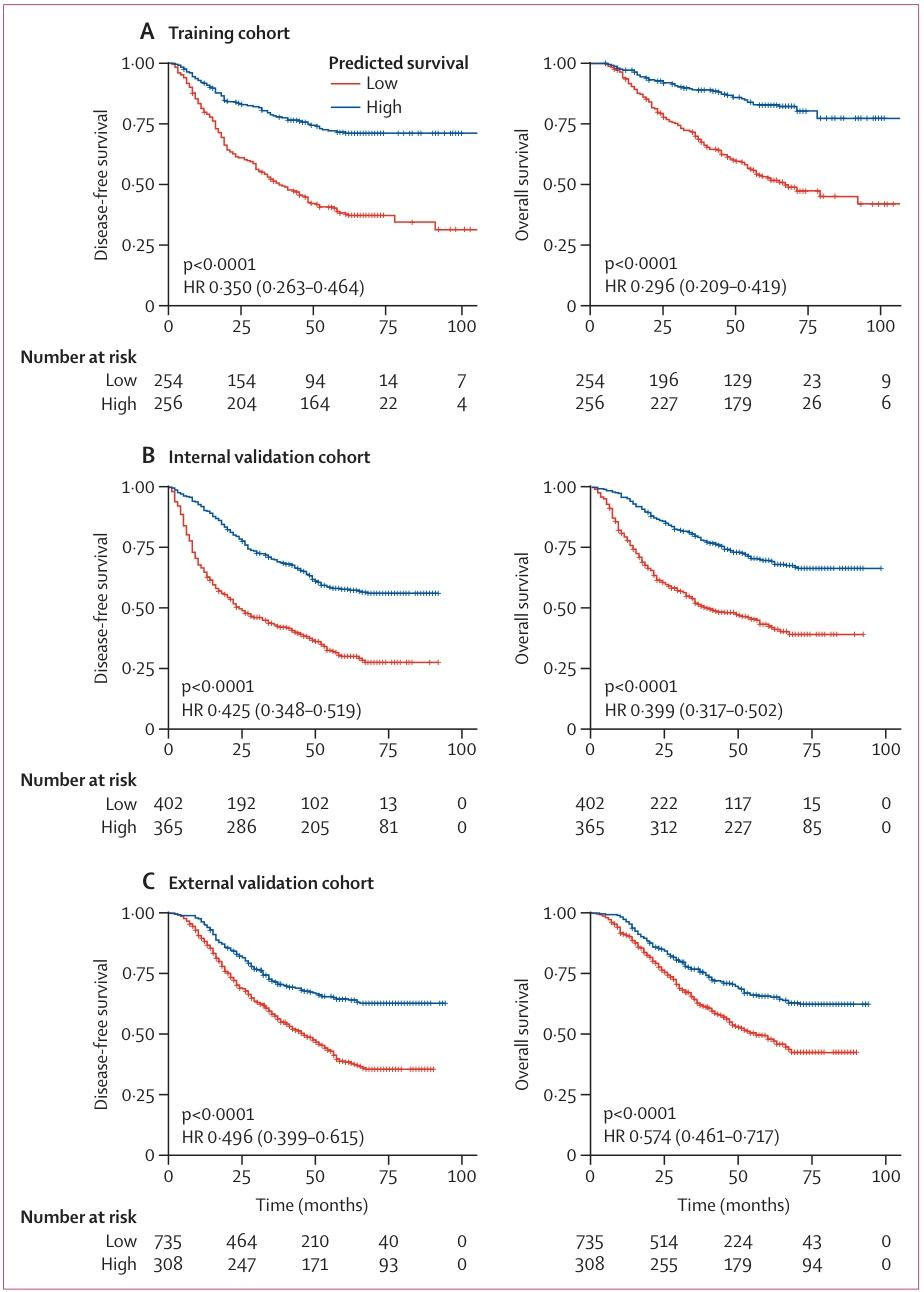
图 4:训练、内部、外部验证队列中模型分层的无病生存期(DFS)和总生存期(OS)Kaplan-Meier分析图
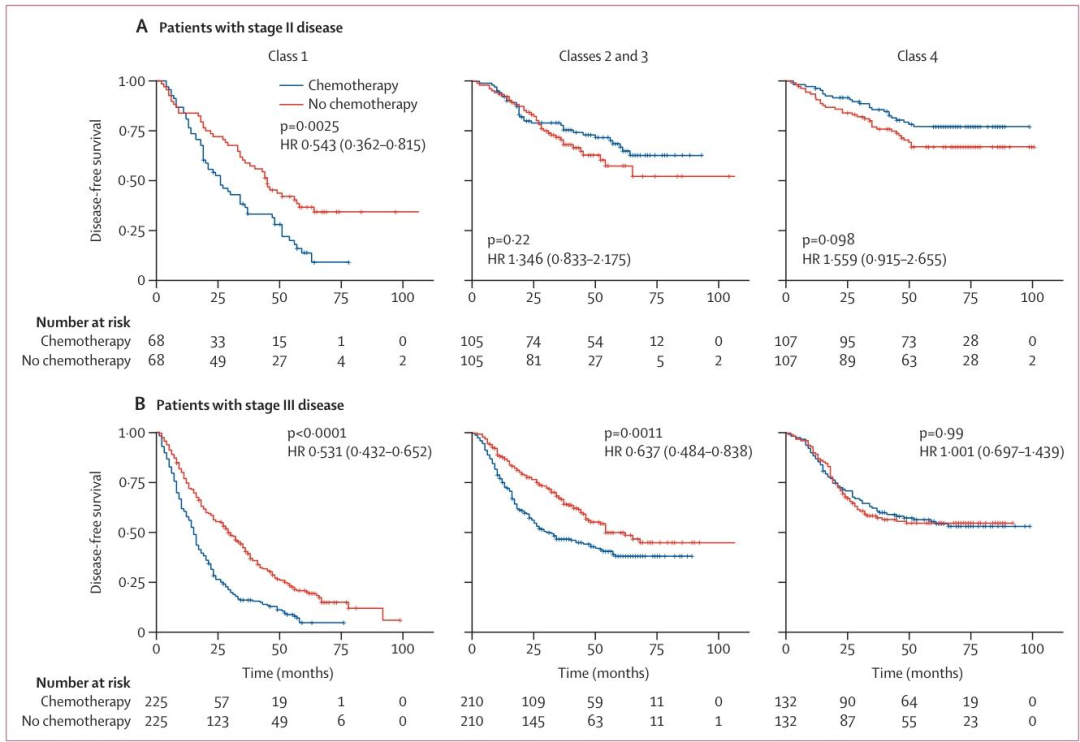
图 5:深度学习模型与II/III期胃癌患者辅助化疗获益的关系图
05
研究结论
本研究成功开发并验证了一种基于术前CT图像的多任务深度学习模型,能够同时准确预测胃癌患者的腹膜复发风险和無病生存期。该模型在包含2320例患者的多中心回顾性队列中表现出一致的高预测效能,腹膜复发的曲线下面积(AUC)在训练集、内部验证集和外部验证集分别达到0.857、0.856和0.843,且其预测能力独立于传统的临床病理因素(如TNM分期)。研究的关键结论在于,该模型不仅能有效进行风险分层,还能指导个体化治疗决策:对于模型预测为高腹膜复发风险且低生存期的II期和III期患者,辅助化疗显著改善了其无病生存期;而对于预测为低风险的患者,化疗则无明显获益。此外,当临床医生参考该AI模型的预测结果后,其对腹膜复发的判断敏感度和诊断一致性均得到显著提升。该研究首次证实了基于深度学习分析的CT影像在预测胃癌术后腹膜复发方面的巨大潜力,为筛选可能从强化治疗(如腹腔热灌注化疗)中获益的高危患者提供了无创、精准的新工具,但仍需前瞻性研究进一步验证其临床效用。
参考文献:Jiang Y, Zhang Z, Yuan Q, Wang W, Wang H, Li T, Huang W, Xie J, Chen C, Sun Z, Yu J, Xu Y, Poultsides GA, Xing L, Zhou Z, Li G, Li R. Predicting peritoneal recurrence and disease-free survival from CT images in gastric cancer with multitask deep learning: a retrospective study. Lancet Digit Health. 2022 May;4(5):e340-e350. doi: 10.1016/S2589-7500(22)00040-1.

AtomGit 是由开放原子开源基金会联合 CSDN 等生态伙伴共同推出的新一代开源与人工智能协作平台。平台坚持“开放、中立、公益”的理念,把代码托管、模型共享、数据集托管、智能体开发体验和算力服务整合在一起,为开发者提供从开发、训练到部署的一站式体验。
更多推荐
 已为社区贡献15条内容
已为社区贡献15条内容





所有评论(0)