从大海捞针到量身定制,科晶生物数字化引擎如何加速小分子发现?

在新药研发与生命科学研究的漫长征途中,寻找能够与特定靶标蛋白(诱饵蛋白)完美结合的小分子化合物,往往被形容为“大海捞针”。传统的盲筛模式不仅耗资巨大,且周期漫长,极易错失具有潜力的活性分子。
随着计算生物学与人工智能(AI)的飞速发展,CADD(计算机辅助药物设计)与AIDD(AI驱动药物发现)正以前所未有的速度重塑研发的底层逻辑。作为数字化生物领域的积极探索者,科晶生物为您提供两大核心数字引擎——【小分子化合物虚拟筛选】与【小分子化合物从头设计(De novo design)】,助力科研工作者精准锁定高潜力靶向分子!
今天,我们将通过两份真实的结题项目报告,为您硬核拆解这两大技术是如何高效运作的。
引擎一:小分子化合物虚拟筛选——在海量图谱中“漏斗式精准淘金”
面对动辄数万至数百万级别的已知化合物库,如何快速、准确地找出与目标蛋白具有强相互作用的“潜力股”?科晶生物摒弃了低效的粗筛,构建了一套“高通量初筛—虚拟复筛—精细化终筛”的三阶递进式漏斗体系。
1. 高精度地基:AlphaFold3三维建模与严苛预处理 靶点结构是筛选的基石。对于缺乏已知晶体结构的诱饵蛋白,我们引入前沿的AlphaFold3算法进行高精度的三维结构构建。同时,对海量化合物进行精细化标准处理:将2D转为3D结构,并进行加氢、计算Gasteiger电荷、能量最小化及添加MMFF94力场,确保分子以最符合物理化学规律的真实姿态进入对接池。
2. AutoDock Vina三重接力,层层过滤 我们利用业内权威的AutoDock Vina软件展开三轮计算把关:
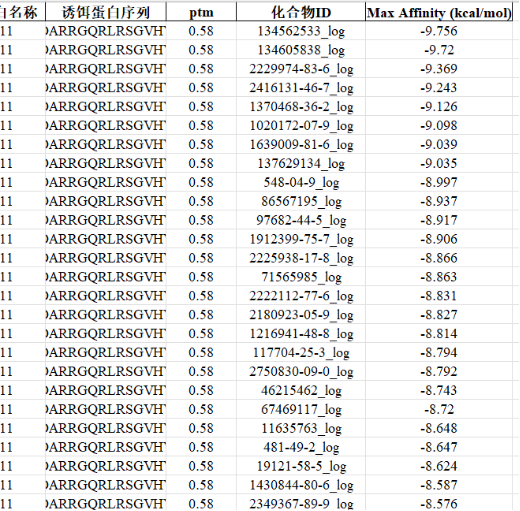
- 高通量筛选:极速扫掠化合物库,提取结合亲和力(Max Affinity)排名前5%的优选分子进入下一轮。
- 虚拟筛选:进一步提高对接精度,剔除假阳性,再次提取排名前 5% 的精英分子。
- 精细化筛选:采用极高精度的参数进行终极验证,得出最可靠的结合预测。
引擎二:小分子从头设计 (De novo) —— AI驱动的“量体裁衣”
如果现有的天然产物库或商业库中没有理想的候选者,或者您面对的是全新的孤儿靶点,想要获得具备全新骨架的分子怎么办?科晶生物的基于生成式AI的从头设计服务,能够真正实现分子的“量身定制”。
1. 智能锁定“靶心”:结合口袋定位 化合物设计的核心在于对症下药。无论您是有已知配体作为参考,还是毫无先验信息需要从零预测,科晶生物均能精准锁定诱饵蛋白的“结合口袋”,明确分子生长的空间坐标。
2. 扩散模型发力:MegaMolBART 智能生成 确定口袋后,我们引入强大的 MegaMolBART——一款基于等变扩散模型的结构驱动药物设计工具。系统能为每个靶标蛋白专属“生长”出数百个高亲和力分子,并通过进化算法兼顾化合物的药物可及性与合成易度,确保新分子不仅“算得出”,更“造得出”。
3. 强强联合验证:Vina + DiffDock 构象预测 新生成的化合物首先接受 AutoDock Vina 的高通量与前50名精细化双重把关。随后,我们引入基于深度学习的 DiffDock 算法。它突破了传统物理对接的空间搜索限制,能更精准地捕捉蛋白与配体间的复杂相互作用,生成符合物理约束的最优结合姿势。
拒绝“黑匣子”,交付出版级科研数据
科研数据的核心价值在于准确与可解释性。科晶生物交付的不仅仅是一份简单的打分Excel表格,更是一份包含详尽参数解析的“保姆级”结题报告,直接赋能您的论文发表与课题申报:
- 多维度能量剖析:深度解读 Output 文件,清晰标注总结合能、分子间作用能(INTER)、分子内应变能(INTRA)以及非结合状态能量(UNBOUND)。
- 微观构象与偏差解读:解析分子的活动扭转键(Active torsions)状态,以及不同对接模式间的均方根偏差(RMSD),确保结果不仅知其然,更知其所以然。
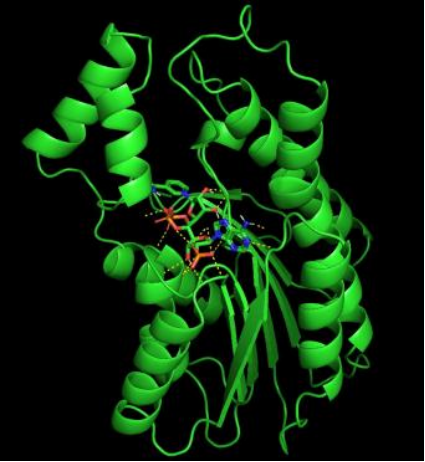
- 高质 3D 可视化:提供直观的受体-配体结合三维可视化展示(如氢键网络、疏水作用等),满足顶刊发文的图表严苛要求。
在这个数字化生物学的新纪元,无论您是正在寻找高效靶向分子的高校课题组,还是致力于创新药研发的医药企业,科晶生物都愿做您最坚实的数字化技术后盾。

AtomGit 是由开放原子开源基金会联合 CSDN 等生态伙伴共同推出的新一代开源与人工智能协作平台。平台坚持“开放、中立、公益”的理念,把代码托管、模型共享、数据集托管、智能体开发体验和算力服务整合在一起,为开发者提供从开发、训练到部署的一站式体验。
更多推荐
 已为社区贡献14条内容
已为社区贡献14条内容








所有评论(0)