如何将TotalSegmentator用于科研论文-案例思路分享
在医学影像分析中,解剖结构自动分割一直是一个基础而关键的任务。过去的做法往往是针对某几种器官(比如肝、肾、肺)训练单独网络。但随着数据和算力的提升,研究者越来越希望用一个“通用模型”一次性分割人体多器官/多结构。TotalSegmentator(TS) 就是在这种背景下应运而生:
- 它支持在 CT(最初版本)中一次性分割 100 多个解剖结构(器官 / 骨骼 / 血管 / 肌肉等)。
- 后来又扩展到 MRI 序列上的“序列无关”分割能力(TotalSegmentator MRI)版本,适配多种 MRI 序列(T1、T2、PD 等)。
- 它开源、用户友好(提供命令行 / Python 接口 / 3D Slicer 插件),因此很快被很多研究者拿来试验或嵌入自己的工作流程
那么,我们该怎么将它应用到科研论文里面呢?今天给大家列举一些已经使用TS发表论文的例子.大概分为以下几个类别:
在TS基础上再训练
TS虽然分割的器官很多,但对有的任务准确性并不是那么好,或者说有的器官没包括在内。就可以选择在此基础上再训练
比如论文:
- Automatic Segmentation of Cardiovascular Structures on Chest CT Data Sets: An Update of the TotalSegmentator
- 中文题目:基于胸部CT数据的心血管结构自动分割:TotalSegmentator的更新
- DOI: 10.1016/j.ejrad.2025.112006
使用方式:基于原有TotalSegmentator的训练集(1613例多中心胸部CT)对心血管系统结构进行再训练和扩展,将缺失的结构添加到标签中。研究者利用TotalSegmentator数据集迭代标注胸部CT,新增11个结构并增强6个已有结构的分割标签
研究目的及贡献:提高胸部CT中动脉、心房、心室等心血管结构的自动分割精度,促进动脉瘤等疾病的量化研究。TotalSegmentator提供的丰富多样训练数据和原有模型框架为新模型的训练奠定基础,使分割结果更准确
技术框架:采用与TotalSegmentator一致的nnU-Net框架进行模型训练和推理。
成果总结:更新后的模型在测试集中对心血管结构分割表现优异,中位DICE系数约0.967,与原模型相比5/6个结构显著提升(p<0.001),表明扩展后的TotalSegmentator模型准确性提高,可在常规电脑上高效运行。
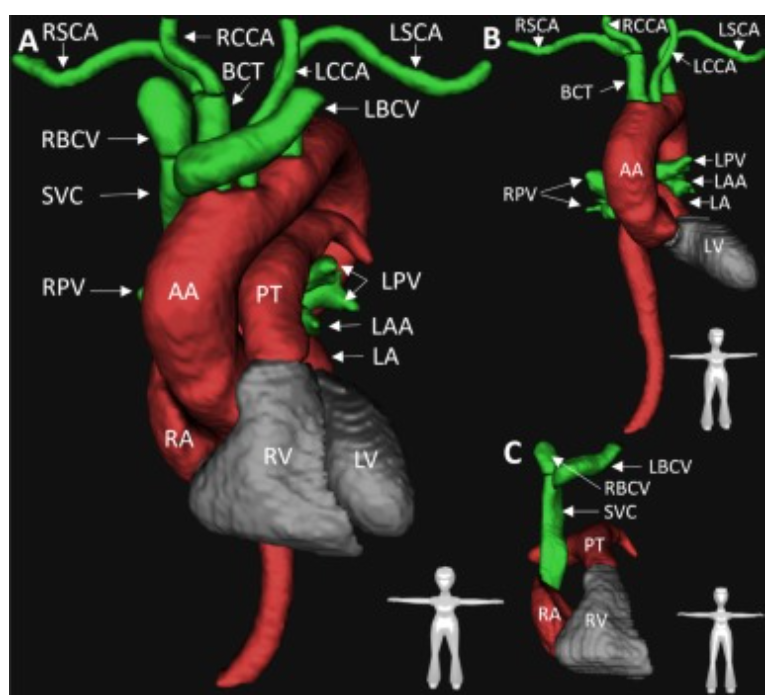
这篇文章训练方式类似TS,只是新增了几个结构,一样可以发ER。这种思路是可以借鉴的。遗憾的是它这篇文章没有公开代码以及新增结构的模型。
使用TS提取组学特征
TS可以分割几百个器官,用于提取影像组学特征再合适不过了。
论文:
- Assessing Patient Health Dynamics by Comparative CT Analysis: An Automatic Approach to Organ and Body Feature Evaluation
- 中文题目:通过比较 CT 分析评估患者健康动态:一种器官和身体特征评估的自动方法
- https://doi.org/10.3390/diagnostics14232760
- 开源代码:https://github.com/frankkramer-lab/RadTA
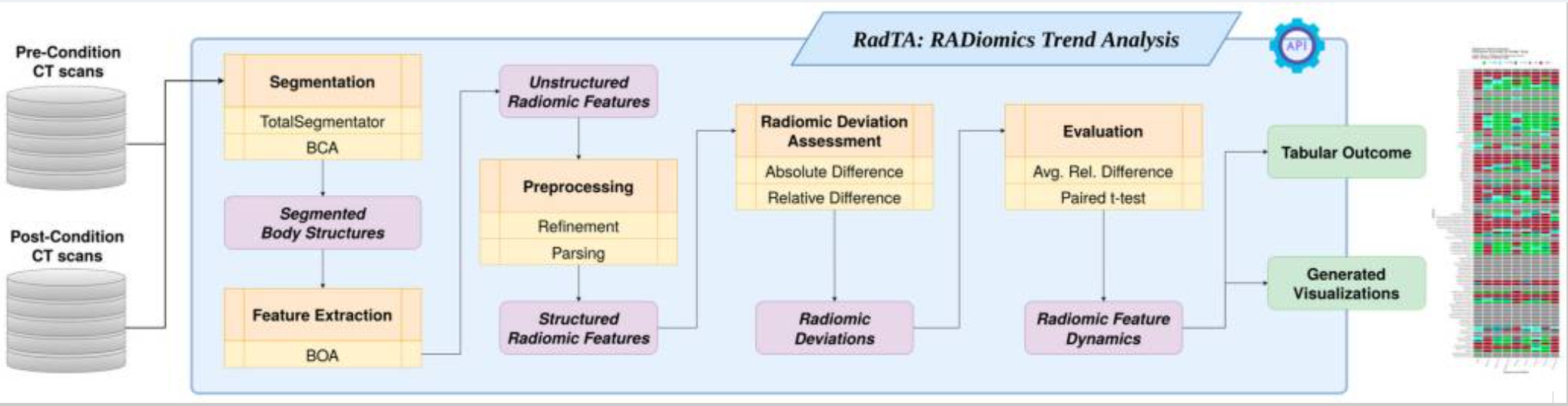
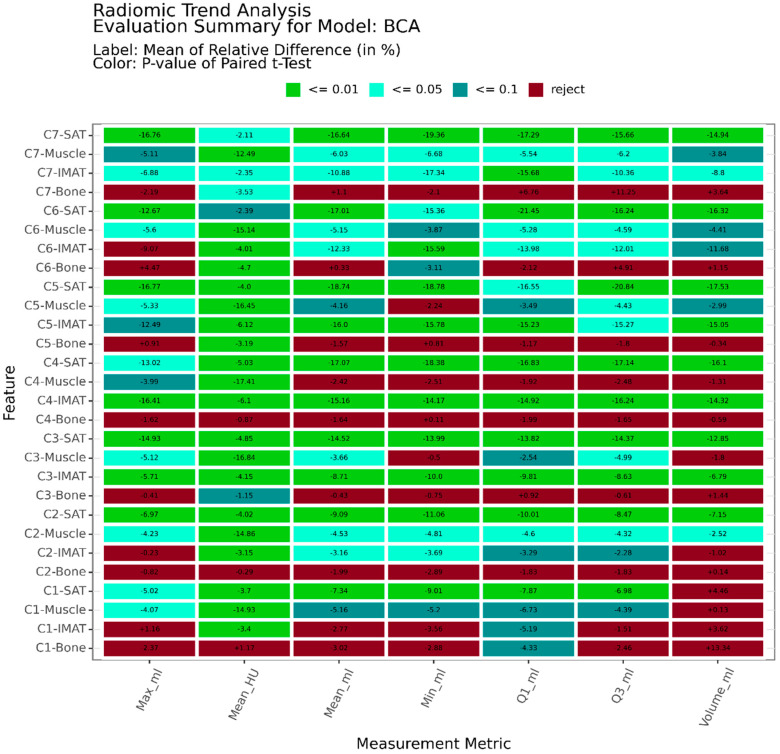
RadTA(RADiomics Trend Analysis)是一个开源的自动化放射组学趋势分析框架,通过整合TotalSegmentator(分割117个结构)和身体成分分析BCA(分割203个组织掩膜),从配对CT扫描中自动提取2560个放射组学特征覆盖320个身体结构,并通过统计检验评估治疗前后的定量成像生物标志物变化。在31例头颈鳞癌放疗患者的验证中,RadTA成功检测到皮下脂肪和肌肉间脂肪组织体积分别下降15.55%和11.68%,肌肉密度下降17.41%,平均处理时间为15分钟/患者。该框架设计为低技术门槛的命令行工具,通过透明的统计分析而非黑盒AI模型提供可解释的临床决策支持,适用于肿瘤学治疗反应监测及其他需要纵向身体成分评估的医学专科。
TS分割器官作为下游任务的基础
论文:
- AI-Enabled CT Cardiac Chamber Volumetry Predicts Atrial Fibrillation and Stroke Comparable to MRI
- 中文题目:人工智能 CT 心腔容积测定可预测心房颤动和中风,效果与 MRI 相当
- https://doi.org/10.1016/j.jacadv.2024.101300
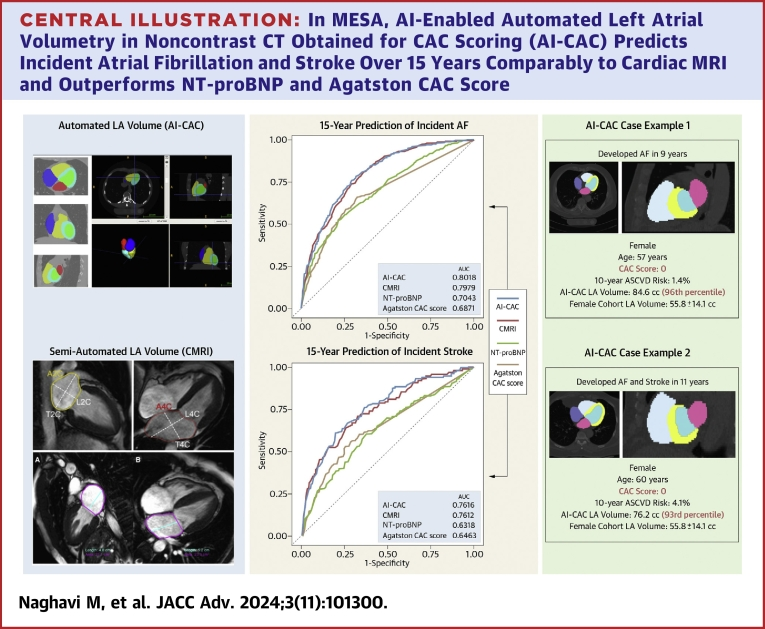
研究目的: 这项研究想解决一个临床难题:心脏核磁共振(MRI)是测量心房大小的金标准,能预测房颤和中风风险,但太贵、太耗时(30-45分钟),不适合大规模筛查。能否用便宜又普及的冠脉钙化CT扫描(每年美国就做1000多万次)来达到同样效果?
研究方法:研究团队开发了一个叫AI-CAC的人工智能工具:基于TotalSegmentator改编,能在21秒内自动测量CT图像中所有4个心腔的体积和左心室壁厚度。然后在美国MESA研究的3552名健康人群中测试,追踪他们15年,看谁得了房颤(562人)和中风(140人)。
核心发现
-
- AI的CT分析≈专家的MRI分析
AI分析CT预测房颤的准确率(AUC 0.802)与专家手工测量MRI(AUC 0.798)几乎一样,预测中风也相当(0.762 vs 0.751)
-
- 发现"漏网之鱼"
17.7%冠脉钙化评分为0(被认为低风险)的人实际上心房已经增大,这些高危患者传统方法会漏诊
-
- 优于传统指标
AI-CAC在1年内预测房颤的准确率(AUC 0.83)明显优于常用的CHARGE-AF风险评分(0.74)和血液指标NT-proBNP(0.74)
- 临床意义
这项研究证明:用AI分析常规CT扫描,可以"免费"获得额外的健康信息。医生可以在患者做冠脉钙化评分时,顺便用AI自动检测心腔是否增大,及早发现房颤和中风的高危人群,推荐他们做心脏超声进一步检查或预防性治疗。这就像给每台CT机装上了"智能预警系统",能挖掘出影像中原本被忽略的宝贵信息。
其实,利用TS做科研的太多了,结合你的方向你的领域来做。

AtomGit 是由开放原子开源基金会联合 CSDN 等生态伙伴共同推出的新一代开源与人工智能协作平台。平台坚持“开放、中立、公益”的理念,把代码托管、模型共享、数据集托管、智能体开发体验和算力服务整合在一起,为开发者提供从开发、训练到部署的一站式体验。
更多推荐
 已为社区贡献15条内容
已为社区贡献15条内容






所有评论(0)