组织切片基础形态学染色方法大全
很多科研新手拿到组织切片时,常常面对多种染色方法无从选择。今天,小橙子为大家系统梳理6种常见的基础形态学染色方法,帮你快速选对方法、避开误区,轻松搞定形态学观察!
基础形态学染色的核心目标是清晰显示组织和细胞的基本形态,区分细胞核、细胞质、细胞膜及不同组织成分。这类方法是组织学观察的基石,适用于常规病理筛查和基础形态观察,为后续的病理分析和实验验证提供依据。
1. 苏木素-伊红染色
苏木素-伊红染色(Hematoxylin-Eosin Staining,简称H&E染色)是组织形态学中最经典、应用最广泛的方法。几乎适用于所有组织切片(包括石蜡切片和冰冻切片),是病理诊断和基础科研的首选染色技术。
🧪 染色原理
H&E染色的核心在于两种染料与细胞成分的特异性结合,从而实现核质区分:
-
苏木素(碱性染料)与细胞内的酸性成分(主要是细胞核内的染色质)结合,使细胞核呈现深蓝色,清晰显示细胞核的形态和大小。
-
伊红(酸性染料)与细胞内的碱性成分(如细胞质、细胞膜和胞外基质蛋白)结合,使细胞质呈现淡红色,帮助分析细胞形态和组织结构。
🔍 结果观察
-
细胞核:深蓝色,核形态、大小和染色深浅一目了然。
-
细胞质:淡红色,可观察细胞质分布、组织边界及分层。
-
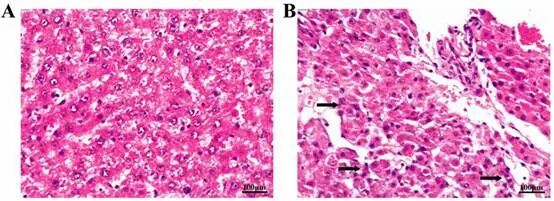
🔑 优缺点
-
优点:操作简便快速(全程30–60分钟),染色效果稳定,适用范围极广,成本低廉,切片可长期保存,对比清晰,满足绝大多数形态观察需求。
-
缺点:特异性较低,无法区分胶原、弹性纤维等特殊成分;不能检测细胞内特定物质(如糖原、脂肪),仅能观察基本形态。
📌 主要应用
适用于各类组织的形态学及病变观察,如肿瘤组织、肝脏、心脏、肾脏等,适配绝大多数基础形态观察需求。
2. 吉姆萨染色
吉姆萨染色(Giemsa Staining)是专用于血液系统和染色体的形态学染色方法,染色效果柔和,能清晰显示细胞核细节,尤其适合血细胞观察。
🧪 染色原理
目前主流方法包括瑞氏-吉姆萨染色或改良吉姆萨染色。染料由酸性染料(伊红、荧光桃红B)和碱性染料(亚甲基蓝、天青B等)组成:
-
酸性染料与嗜酸性颗粒(碱性蛋白)结合,使其呈粉红色。
-
碱性染料与嗜碱性物质(核蛋白、淋巴细胞胞浆)结合,使其呈紫蓝色。
-
中性颗粒同时与伊红和亚甲基蓝结合,呈现淡紫色。
🔍 结果观察
-
成熟红细胞:胞质粉红色,无细胞核,呈圆饼状。
-
中性粒细胞:胞质淡紫红色,细胞核蓝色,呈马蹄形或分叶状。
-
嗜酸性粒细胞:胞质深红色,细胞核蓝色,呈马蹄形或分叶状。
-
嗜碱性粒细胞:胞质蓝紫色,细胞核蓝色,呈马蹄形或分叶状。
-
淋巴细胞:胞质蓝紫色,细胞核蓝色,细胞和核较小。
-
单核细胞/巨噬细胞:胞质蓝紫色,细胞核蓝色,细胞和核较大。
-
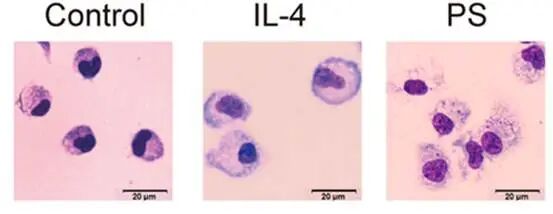
🔑 优缺点
-
优点:细胞核细节显示清晰,适合血细胞和染色体观察;染色效果稳定,能区分不同类型血细胞;可用于寄生虫检测。
-
缺点:操作相对复杂(需缓冲液调节pH),适用范围较窄,主要针对血液和染色体标本。
📌 主要应用
-
血液系统研究:血细胞涂片、骨髓切片的形态学观察,贫血、白血病等疾病初步筛查。
-
染色体核型分析:观察细胞分裂期染色体的形态和数量。
-
寄生虫检测:如疟原虫、弓形虫在组织或血液中的定位。
3. 台盼蓝染色
台盼蓝染色(Trypan Blue Staining)是一种快速、简单的细胞活性检测方法,属于“活体染色”,可快速区分活细胞与死细胞,适合细胞培养及组织切片中细胞存活状态的快速筛查。
🧪 染色原理
台盼蓝为酸性偶氮染料,具有亲水性,无法透过活细胞完整的细胞膜。死细胞由于细胞膜破损,通透性增加,染料进入细胞使其染成蓝色;活细胞因细胞膜完整,不被染色,呈无色或淡粉色。
🔍 检测指标
-
活细胞:无色或淡粉色。
-
死细胞:蓝色。
-
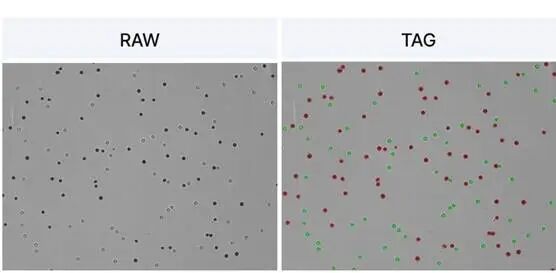
🔑 优缺点
-
优点:操作极简便,耗时短(5–10分钟),成本低,可批量检测,无需特殊仪器。
-
缺点:仅能区分活死细胞,无法判断细胞损伤类型(如凋亡、坏死);特异性低,部分早期凋亡细胞可能不被染色,导致结果偏差。
📌 主要应用
主要用于活细胞计数、细胞活力检测、组织切片中细胞存活状态的快速观察。
4. 甲苯胺蓝染色
甲苯胺蓝染色(Toluidine Blue Staining,简称TB染色)是一种快速、简便的碱性染色方法,属于“快速筛查型”染色,适合快速观察组织或特定细胞形态及特定成分,可作为H&E染色的补充。
🧪 染色原理
甲苯胺蓝为醌亚胺类碱性染料,可与细胞内黏多糖、肥大细胞颗粒中的肝素和组织胺等物质结合,呈现紫红色;同时可与细胞核内的核酸结合,使细胞核呈深蓝色,细胞质呈浅蓝色。
🔍 检测指标
-
黏多糖、肥大细胞:紫红色。
-
尼氏小体:蓝色块状。
-
嗜碱性粒细胞、软骨组织基质:蓝紫色。
-
幽门螺杆菌:蓝紫色。
-
细胞核:深蓝色;细胞质:浅蓝色。
-
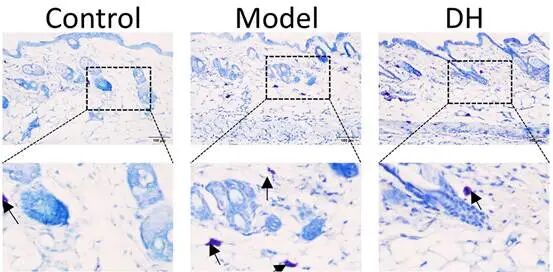
🔑 优缺点
-
优点:操作极简便,耗时短(10–15分钟),成本低;能快速显示肥大细胞,适合大批量样本筛查。
-
缺点:染色细节不如H&E染色清晰,无法精细区分细胞质与其他成分;特异性一般,仅适合快速筛查,不适合精准病理诊断。
📌 主要应用
适用于细胞涂片、血涂片、骨髓涂片以及不同动植物组织的石蜡切片和冰冻切片,常用于肥大细胞、软骨细胞及细胞核的快速染色。
5. 尼氏染色
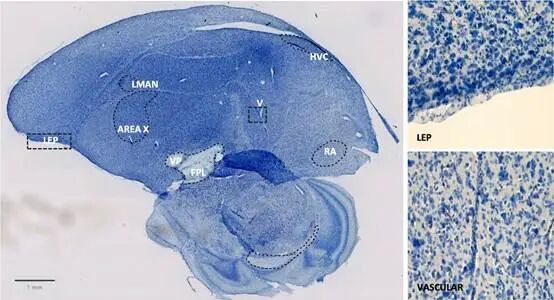
尼氏染色(Nissl Staining)是神经科学研究的“专属染色方法”,主要用于显示神经元的形态和尼氏小体,能清晰区分神经元与神经胶质细胞,是神经组织形态学观察的核心方法。
🧪 染色原理
尼氏体是神经元胞质内的嗜碱性物质(粗面内质网,蛋白质合成场所)。尼氏染色液中的碱性染料(如甲苯胺蓝、亚甲蓝、焦油紫、硫堇等)可特异性结合尼氏体并将其染色。
🔍 结果观察
-
尼氏小体:深蓝色或蓝紫色(焦油紫法呈紫色)。
-
神经元细胞核:淡蓝色(焦油紫法呈淡紫色)。
-
神经胶质细胞:染色较浅,呈淡蓝色。
-
背景:焦油紫法背景呈淡紫色或蓝色。
-
🔑 优缺点
-
优点:特异性强,能精准区分神经元与神经胶质细胞;尼氏小体显示清晰,可快速判断神经元功能状态;操作相对简便。
-
缺点:仅适用于神经组织,不能用于其他组织;无法显示髓鞘和轴突细节,需结合其他染色方法。
📌 主要应用
-
神经科学研究:大脑、脊髓组织形态学观察,神经元分布、数量统计。
-
神经系统疾病研究:评价神经元损伤情况(如尼氏小体变化)。
6. Luxol Fast Blue染色
Luxol Fast Blue染色(简称LFB染色)是神经组织形态学的重要染色方法,专门用于显示神经髓鞘,能清晰区分髓鞘与神经元、神经胶质细胞,是研究髓鞘损伤和修复的核心技术。
🧪 染色原理
LFB(坚牢蓝)为脂溶性铜-酚箐染料,在乙醇溶液中可特异性结合神经髓鞘中的脂质(如髓磷脂),使其呈现亮蓝色。随后可用苏木素复染细胞核(呈蓝黑色),或与焦油紫配合使尼氏体呈粉红色或紫红色。
🔍 结果观察
-
髓鞘:亮蓝色。
-
细胞核:蓝黑色。
-
神经元胞体:淡蓝色(苏木素复染)或尼氏体呈粉红色/紫红色(焦油紫复染)。
🔑 优缺点
-
优点:特异性强,能精准显示神经髓鞘,髓鞘脱失区域清晰可辨;染色效果稳定,切片可长期保存。
-
缺点:仅适用于神经组织;操作较复杂(需梯度酒精脱水、分化),耗时较长(全程1–2小时)。
📌 主要应用
用于神经髓鞘的分布观察,以及神经损伤中的髓鞘脱失、修复情况检测,适用于神经髓鞘损伤和神经退行性疾病相关研究。
以上六种染色方法涵盖了从基础组织形态到特定细胞结构(如血细胞、神经元、髓鞘)的观察需求。在实际应用中,可根据研究目的、样本类型和观察目标灵活选择,必要时也可联合使用多种染色以获得更全面的信息。

AtomGit 是由开放原子开源基金会联合 CSDN 等生态伙伴共同推出的新一代开源与人工智能协作平台。平台坚持“开放、中立、公益”的理念,把代码托管、模型共享、数据集托管、智能体开发体验和算力服务整合在一起,为开发者提供从开发、训练到部署的一站式体验。
更多推荐
 已为社区贡献6条内容
已为社区贡献6条内容






所有评论(0)