NPJ Precis Oncol(IF=8)山西医科大学第一医院双卫兵教授等团队:基于多尺度影像组学与深度学习的肾透明细胞癌Ki-67表达预测研究
01
文献学习
今天分享的文献是由山西医科大学第一医院双卫兵教授等团队于2025年12月在肿瘤学领域顶刊《npj Precision Oncology》(中科院1区top,IF=8)上发表的研究“Integration of multi-scale radiomics and deep learning for Ki-67 prediction in clear cell renal carcinoma”即多尺度放射组学与深度学习融合预测透明细胞肾细胞癌的Ki-67表达水平,该研究基于627例肾透明细胞癌患者的多中心回顾性数据,构建并验证了一个融合多尺度影像组学、深度学习和临床特征的多模态机器学习模型,用于术前无创预测Ki-67表达水平。该模型在外部测试集中AUC达0.756,显著优于单一模态模型,具有良好的校准性和临床净收益。SHAP分析显示,肿瘤内部异质性(habitat影像)是模型最重要的预测因素。
创新点:①突破传统单区域分析,首次整合瘤内、瘤周及栖息地多尺度影像组学特征②融合多模态影像组学与深度学习特征,构建基于堆叠集成策略的预测模型③首次证实影像组学与深度学习特征的互补协同,挖掘肿瘤表型多维信息
临床价值:①实现Ki-67表达的术前无创预测,替代术后免疫组化,避免病理延迟与取样偏倚②精准识别高危患者,指导个体化手术与随访方案,避免过度治疗或干预不足③决策曲线分析显示广泛的临床净收益,模型校准度优异,实用性强
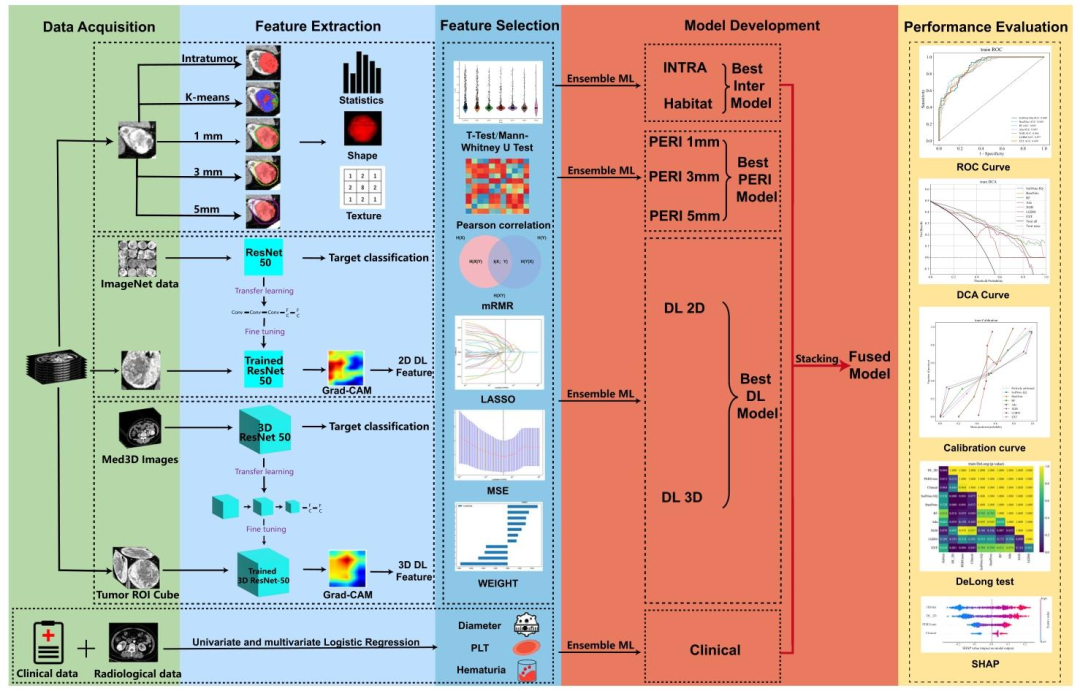
图 6:研究整体工作流
数据获取:多中心收集临床数据、影像学CT数据(皮质髓质期、肾实质期);
特征提取:并行提取三类特征——放射组学特征(瘤内、栖息地、瘤周1/3/5mm)、深度学习特征(2D/3DResNet50)、临床特征(Table1筛选的独立因子);
特征选择:通过ICC/CCC验证特征稳定性,mRMR算法降维,LASSO回归确定最终特征集;
模型构建:先构建单模态模型并筛选最优算法,再通过投票融合、堆叠融合构建多模态融合模型;
性能评估:采用ROC、DCA、校准曲线、DeLong检验评估模型,SHAP分析实现可解释性。
02
研究背景和目的
研究背景
肾透明细胞癌(ccRCC)是肾癌中最常见的病理类型,约占所有肾癌病例的70%至80%,其全球发病率和死亡率持续上升,已成为重要的公共卫生问题。尽管早期局限性ccRCC可通过手术切除获得良好预后,但约20%至30%的患者术后仍会出现局部复发或远处转移,显著影响5年生存率。Ki-67是一种反映细胞增殖活性的核抗原,已被广泛证实为ccRCC中重要的预后生物标志物,其高表达与肿瘤侵袭性、恶性进展及不良预后密切相关。目前,Ki-67的评估依赖于术后免疫组化染色,存在侵入性、采样偏差和诊断延迟等固有局限。因此,开发一种术前、无创、可靠的Ki-67表达预测方法,对于精准评估肿瘤生物学行为、早期识别高危患者、制定个体化治疗策略具有重要临床意义。医学影像作为宏观水平的生物学过程替代指标,结合人工智能技术,尤其是放射组学与深度学习,为无创预测肿瘤分子表型提供了新路径。然而,既往研究多局限于单一影像区域或单一特征来源,未能充分利用肿瘤内异质性、微环境信息及高阶语义特征,限制了模型的预测性能和泛化能力。
研究目的
本研究旨在构建并验证一种多模态机器学习模型,通过整合多尺度放射组学特征(包括瘤内、瘤周及基于“影像组学亚区”分析的异质性区域)、二维与三维深度学习特征以及临床实验室指标,实现对ccRCC患者术前Ki-67表达水平的精准预测。研究团队基于627例来自多中心回顾性队列的患者数据,首先通过ICC、CCC等方法筛选稳定特征,分别构建了多个单模态模型(如瘤内、瘤周、亚区、DL2D/DL3D及临床模型),并在验证集上比较五种集成学习算法(RF、Ada、XGB、LGBM、EXT)的表现。在此基础上,进一步采用堆叠集成策略融合表现最优的单模态模型,构建最终的多模态融合模型。研究不仅评估了模型的区分度、校准度和临床净收益,还通过SHAP分析揭示了各模态对预测结果的贡献程度。最终目标是开发一种可解释、高泛化能力的术前预测工具,为ccRCC患者的个性化手术决策、术后监测策略制定及高风险人群早期干预提供影像学支持。
03
数据和方法
研究数据:
样本量:627例ccRCC患者
数据来源:三家中国医院(山西医科大学第一医院、山西白求恩医院、山西省人民医院)
分组:训练集(n=290)、验证集(n=125)、外部测试集(n=212)
Ki-67阈值:5%(≥5%为高表达)
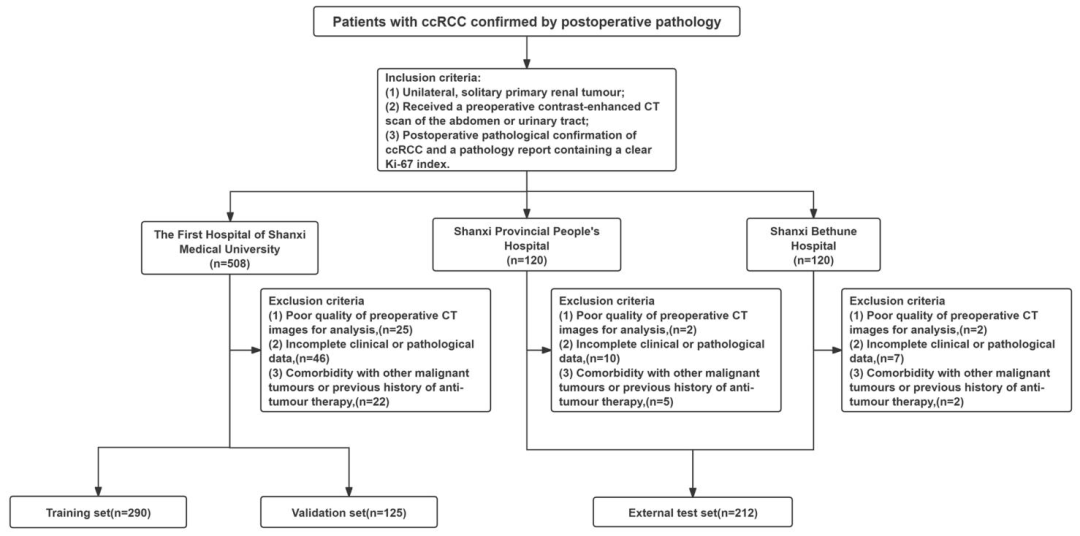
图 5:患者选择流程图
技术方法:
影像分割与特征提取:
手动分割肿瘤区域,提取影像组学特征(intratumoral, peritumoral, habitat)
使用2D/3D ResNet50提取深度学习特征
临床特征通过回归分析筛选
特征筛选:
ICC、CCC评估特征稳定性
t检验、Pearson相关、mRMR、LASSO逐步筛选
模型构建:
构建五大类单模态模型(intratumoral, habitat, peritumoral, DL, clinical)
使用五种集成学习算法(RF, Ada, XGB, LGBM, EXT)
融合策略:投票法 + Stacking
模型评估:
ROC、AUC、校准曲线、DCA、DeLong检验、SHAP可解释性分析
04
实验结果
最佳单模态模型:Habitat模型(AUC=0.835)表现最佳
最佳融合模型:EXT-Stacking模型,验证集AUC=0.848,外部测试集AUC=0.756
SHAP分析:Habitat、DL_2D、PERI1mm为最主要贡献因素
临床价值:DCA显示融合模型在20%~85%阈值范围内净收益最高
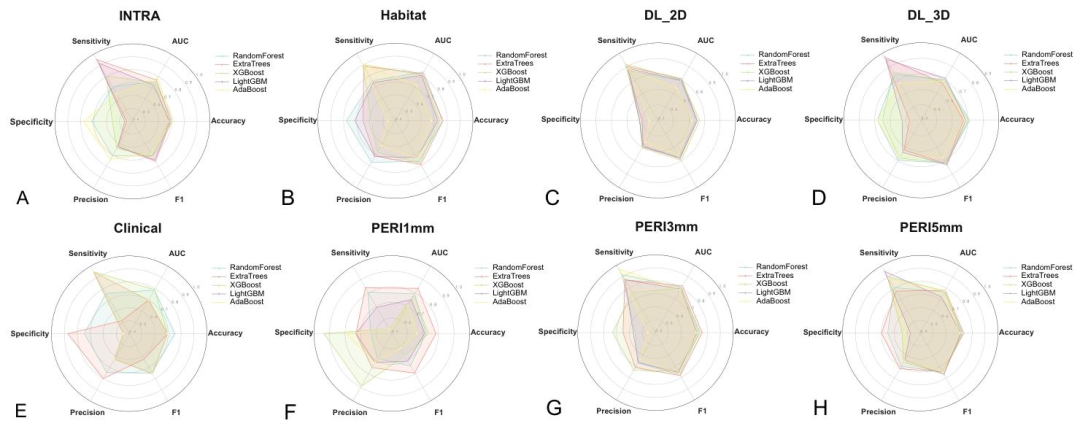
图 1:验证集上单模态模型的性能对比
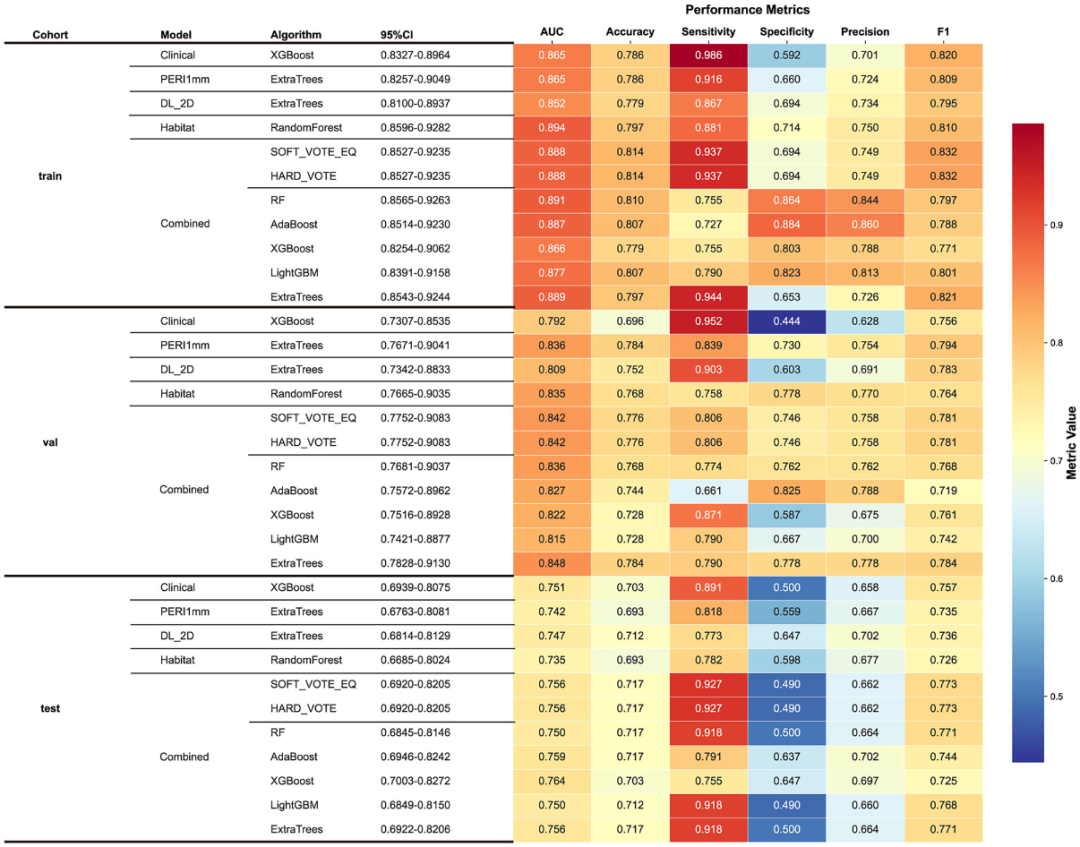
图 2:单模态和融合模型在各队列的性能热图
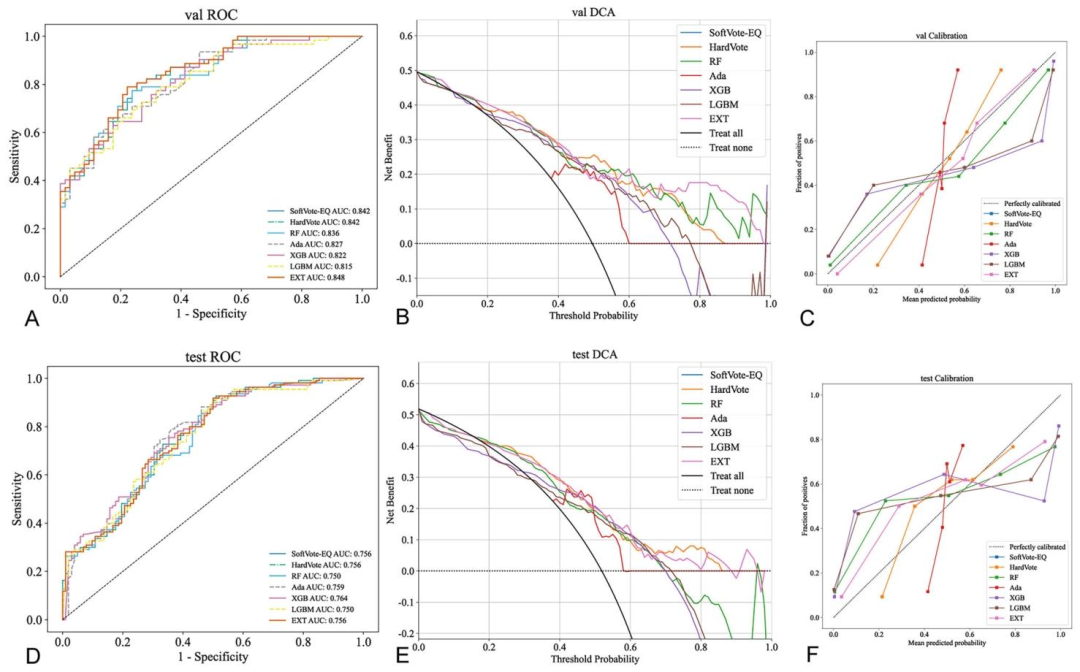
图 3:集成融合策略的性能对比
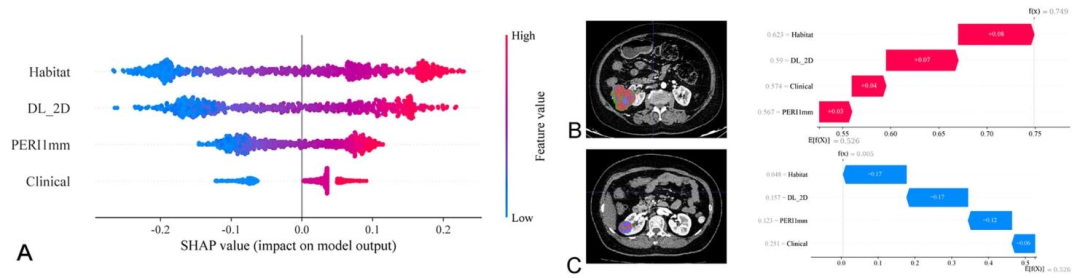
图 4:EXT-stacking模型的SHAP可解释性分析
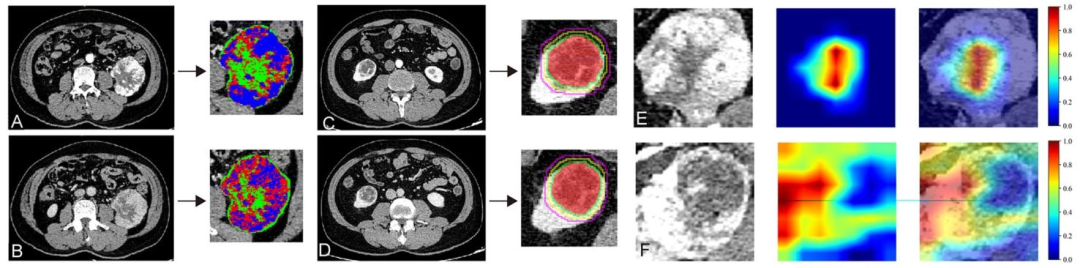
图 7:生境成像、瘤周分割和DL模型可解释性的可视化
05
研究结论
该研究成功开发并验证了一种整合多尺度影像组学与深度学习特征的多模态融合模型,用于术前无创预测透明细胞肾细胞癌(ccRCC)的Ki-67表达水平。研究纳入了627例患者,构建了基于CT影像的瘤内、瘤周(1mm/3mm/5mm)、“影像亚区”(habitat)及2D/3D深度学习的单模态模型,并通过堆叠集成策略(EXT-stacking)融合最优模型。结果显示,融合模型在验证集和外部测试集中均表现出最优的预测性能(AUC分别为0.848和0.756),显著优于临床模型及单一模态模型。Habitat影像特征贡献最大,揭示了肿瘤异质性与Ki-67表达之间的病理关联;瘤周1mm区域也被证实为关键预测区域。模型具备良好的校准能力和临床净收益,SHAP分析进一步增强了其可解释性。该研究为ccRCC的术前风险分层、个体化手术决策及随访策略提供了强有力的无创工具,具有重要的临床转化潜力。
参考文献:Li J, Lv D, Guo Z, Zhou H, Yao X, Rong Y, Bian X, Pang L, Zhao T, Qiao Y, Shuang W. Integration of multi-scale radiomics and deep learning for Ki-67 prediction in clear cell renal carcinoma. NPJ Precis Oncol. 2025 Dec 6;10(1):12. doi: 10.1038/s41698-025-01214-y.

AtomGit 是由开放原子开源基金会联合 CSDN 等生态伙伴共同推出的新一代开源与人工智能协作平台。平台坚持“开放、中立、公益”的理念,把代码托管、模型共享、数据集托管、智能体开发体验和算力服务整合在一起,为开发者提供从开发、训练到部署的一站式体验。
更多推荐
 已为社区贡献107条内容
已为社区贡献107条内容






所有评论(0)