体液 “信号” 解锁 PD 认知密码 —— 帕金森病认知障碍生物标志物研究综述
引言
帕金森病认知功能障碍(PDCI)是帕金森病(PD)最主要的非运动症状之一,多达 80% 的 PD 患者随疾病进展会发展为帕金森病痴呆(PDD),严重影响患者生活质量且与早期死亡风险相关。PDCI 的病理机制复杂,涉及 α- 突触核蛋白异常聚集、神经炎症、氧化应激、神经退行性变等多过程。体液生物标志物因取样便捷、可动态监测等优势,成为 PDCI 早期诊断、病程预测及治疗靶点开发的研究热点。
一、帕金森病认知功能障碍核心体液生物标志物
(一)与蛋白质错误折叠相关的生物标志物
蛋白质错误折叠及异常聚集是PDCI的核心病理特征,以α-突触核蛋白、Aβ、Tau蛋白为代表的标志物成为研究重点,其表达水平及修饰状态与PDCI的严重程度密切相关。
1. α-突触核蛋白:作为Lewy小体的主要组成成分,病理性α-突触核蛋白的神经元间扩散是导致皮层认知功能障碍的关键。脑脊液中寡聚体或总α-突触核蛋白与PD患者认知能力的相关性尚未明确,但超敏免疫分析法证实,PDD患者血浆α-突触核蛋白水平显著高于PD-MCI患者和认知正常的PD患者,且与简易精神状态检查(MMSE)得分呈负相关。α-突触核蛋白的磷酸化、泛素化、硝化等翻译后修饰形式,可能更精准地反映PD认知衰退进程,而血浆α-突触核蛋白/Aβ40比率可显著提高PD认知衰退的预测准确性。
2. 淀粉样β蛋白:Aβ虽为阿尔茨海默病的核心标志物,但其与PDCI的关联已被证实。脑脊液中Aβ42水平降低与PD患者认知功能下降密切相关,尤其在PD-MCI向PDD转化过程中表现出显著的预测价值。外周血中Aβ40和Aβ42的检测结果存在异质性,血浆Aβ42水平并非PDCI的可靠标志物,但血浆Aβ40水平与PD认知下降相关,且Aβ42/Aβ40比率可作为早期筛查标志物——PD-MCI患者该比率显著降低,而比率升高与更好的执行功能评分相关。
3. Tau蛋白:Tau蛋白过度磷酸化形成的神经纤维缠结会损害神经元功能,引发认知衰退。脑脊液中总Tau蛋白无法预测PD认知衰退,但磷酸化Tau181(p-tau181)水平升高与PD患者认知衰退加速相关,且PDCI患者脑脊液p-tau181水平显著高于无认知障碍的PD患者。血浆p-tau181可区分PD认知正常与认知障碍患者,与注意力、执行功能下降相关,而p-tau181/Aβ42比率则与记忆和执行功能损害密切相关。此外,p-tau231、p-tau217等新兴标志物在阿尔茨海默病中具有高度特异性,但其在PDCI中的预测价值仍需进一步验证。
(二)神经退行性相关生物标志物
神经丝轻链蛋白(NFL)是轴突胞质的核心结构蛋白,当轴突受损或神经元死亡时,NFL会释放至脑脊液和血液中,成为反映神经退行性变的特异性标志物。PDCI患者基线脑脊液NFL水平显著升高,且其水平与认知表现差、皮层结构改变密切相关,高NFL水平可有效预测随访期内PDD的发生。外周血NFL同样具有预测价值,但由于其易受年龄等因素影响,特异性不足,需结合其他标志物或临床指标进行解读。血浆α-突触核蛋白与NFL的联合检测,结合神经影像学指标构建的综合模型,可全面评估PD严重程度并提高PDD风险预测的准确性。
(三)炎症与氧化应激相关生物标志物
神经炎症和氧化应激是PDCI病理进程的重要环节,星形胶质细胞激活、炎症因子释放、自由基蓄积等过程共同参与神经元损伤,相关标志物为PDCI的机制研究和治疗靶点开发提供了新方向。
1. 胶质纤维酸性蛋白(GFAP):作为星形胶质细胞激活的特异性标志物,GFAP与PD患者认知功能衰退密切相关,可有效预测PDD及PD-MCI向PDD的转化,是评估PDCI严重程度的重要指标。
2. 氧化应激相关标志物:尿酸具有清除自由基的神经保护作用,低尿酸水平与PD患者认知表现差相关;SIRT1蛋白可调节α-突触核蛋白降解、抑制氧化应激和炎症反应,是PDCI潜在的生物标志物和治疗靶点。同型半胱氨酸、维生素D的水平与PDCI的关联尚存争议,部分研究证实高同型半胱氨酸通过影响脂质代谢和氧化应激参与PDCI进程,而维生素D的神经保护作用仍需大样本研究验证。
3. 炎症因子:C反应蛋白、肿瘤坏死因子α、白介素-6、干扰素γ诱导蛋白10等炎症因子在PD患者体液中表达异常,其水平升高与认知衰退相关,提示神经炎症途径可能成为PDCI干预的重要靶点。
(四)代谢相关生物标志物
代谢紊乱是PDCI的重要病理特征之一,脂质、氨基酸等代谢物的表达异常与认知功能损害密切相关,为PDCI的早期筛查提供了新的标志物类别。甘油三酯升高与PD-MCI相关,尤其影响视空间和执行功能;PD-MCI患者载脂蛋白A1、总胆固醇、高密度脂蛋白水平显著升高,提示脂质代谢物可能成为PD-MCI的潜在标志物,且存在性别差异。神经酰胺代谢紊乱与PDCI相关,无GBA基因突变的PD患者神经酰胺水平升高与认知功能下降显著相关,但其作用机制仍需深入研究。此外,脂肪酸氧化途径的20种代谢物与PD-MCI相关,其中9种对早期认知功能恶化具有较高的预测准确性;血清1-油酰-sn-甘油-3-磷酸胆碱水平与PD患者认知功能呈负相关,具有潜在的临床诊断价值。
(五)其他潜在生物标志物
1. 神经营养因子:脑源性神经营养因子(BDNF)、胶质细胞源性神经营养因子(GDNF)参与神经元的生长、存活和突触可塑性调节,其水平降低与PDCI认知功能下降相关;表皮生长因子、胰岛素样生长因子-1等也被证实与PD患者认知功能相关。
2. 酶与microRNA:泛素羧基末端水解酶、芳基磺酸酯酶A参与蛋白质降解和α-突触核蛋白清除,其失调会加速PDCI病理进程;microRNA可通过调控神经退行性相关蛋白表达、调节突触可塑性和记忆形成,成为PDCI的潜在标志物。
3. 突触功能与细胞外囊泡标志物:神经粒蛋白(Ng)可反映突触损伤,在PDCI的早期检测中显示出潜力;神经元来源的细胞外囊泡携带α-突触核蛋白、Tau蛋白、细胞因子等标志物,为PDCI的无创诊断和预后评估提供了新途径。
(六)唾液与尿液中的微创生物标志物
唾液与尿液作为无创取材的体液样本,在帕金森病认知功能障碍(PDCI)生物标志物研究中具有独特优势,尽管相关研究仍较有限,但其临床应用潜力已初步显现。 唾液中总α突触核蛋白水平升高与MoCA评分降低呈负相关;口腔微生物组分析显示,PDCI患者唾液中奈瑟菌属与乳杆菌属存在显著关联,提示口腔微生态可能参与PDCI病理过程;而唾液总Tau(ttau)与认知评分无明显相关性,诊断价值有待进一步验证。 尿液中犬尿氨酸水平与MMSE评分呈负相关,可用于PDCI病程监测;尿液外泌体中Ser(P)1292 LRRK2升高与MoCA评分降低相关,有助于识别认知损害较重的PD患者。 唾液与尿液标志物为PDCI无创筛查提供了新方向,但其诊断特异性及检测方法的标准化仍需深入优化。
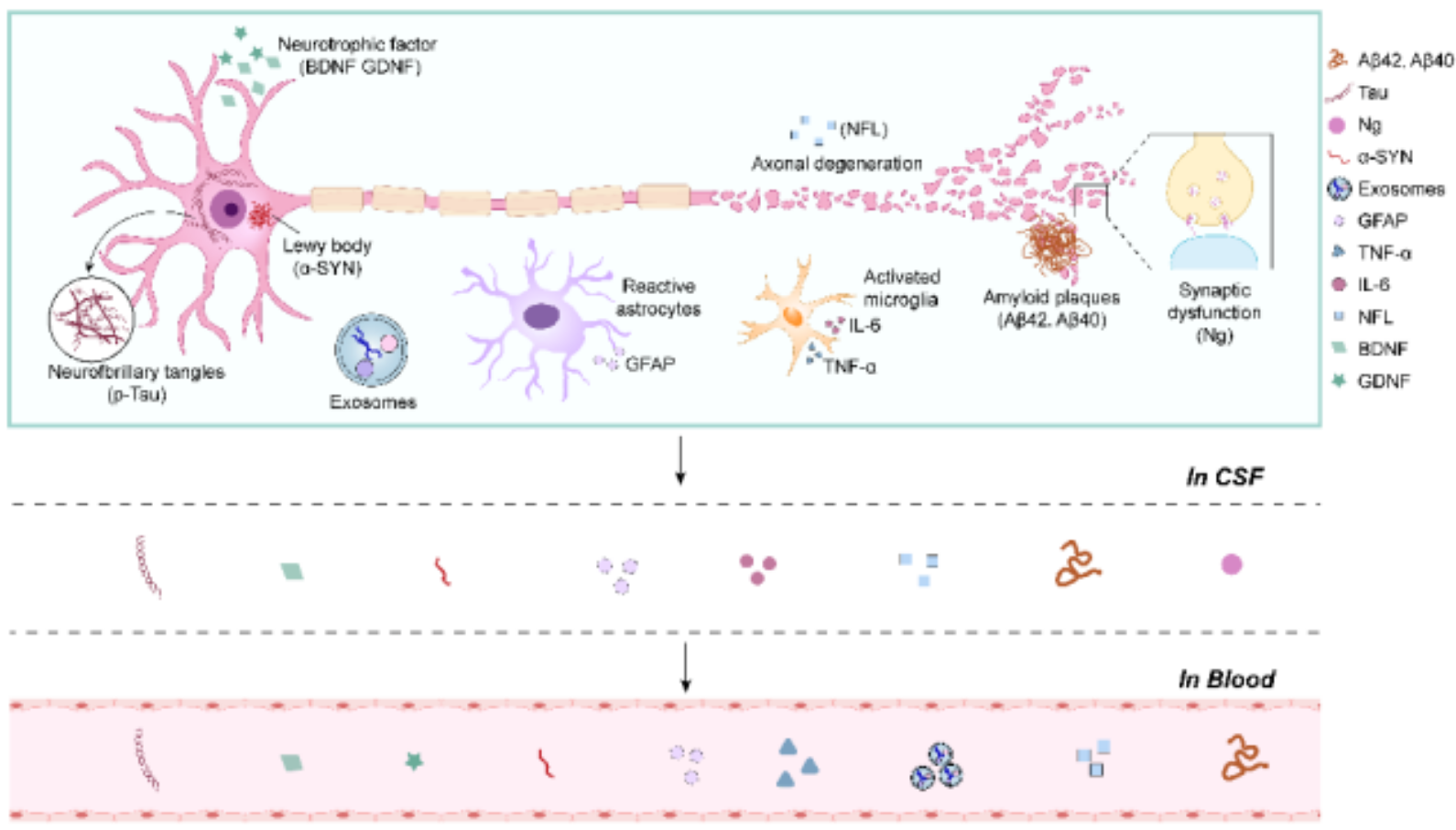
帕金森病认知障碍相关的病理机制及基于生物体液的生物标志物
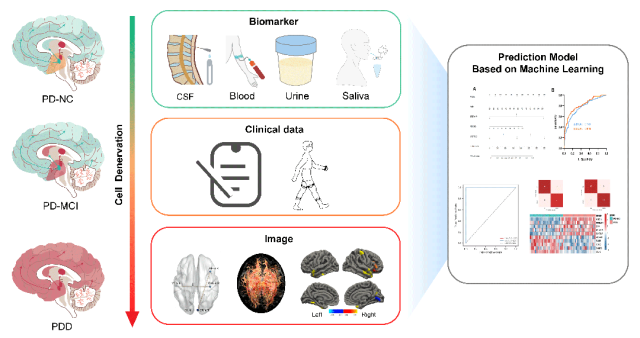
建立帕金森病认知障碍的预测模型
二、多组学技术在帕金森病认知功能障碍标志物研究中的应用
蛋白质组学和代谢组学技术的快速发展,为PDCI标志物的高通量筛选提供了技术支撑,实现了从单一标志物到多标志物联合的研究转变。高通量抗体蛋白质组学发现,脑脊液中激肽原1水平升高与PD患者认知功能测试评分降低相关,是预测PD认知下降的潜在标志物;优化的蛋白质组学方法识别的不同唾液酸化Serpin A1异构体,可100%准确识别PDD患者,显示出极高的诊断价值。
代谢组学研究证实,脂肪酸、卵磷脂、长链脂肪酸、鞘脂类的代谢改变显著促进PDCI的发展,而多组学整合分析可深入解析PDCI的分子通路,为标志物筛选和治疗靶点开发提供更全面的视角。
多组学技术与机器学习的结合,成为PDCI精准诊断的重要发展方向。通过整合血液、脑脊液、唾液、尿液等体液标志物,结合神经影像学和临床数据,利用机器学习算法构建的预测模型,可显著提高PDCI的早期诊断准确性和病程预测能力。该模型可实现PD认知正常(PD-NC)、PD-MCI、PDD的精准分层,为个性化治疗策略的制定提供依据。
三、结论
帕金森病认知功能障碍是严重影响患者预后的核心非运动症状,体液生物标志物在其早期诊断、病程预测和治疗靶点开发中具有不可替代的价值。目前已在血液、脑脊液、唾液、尿液等体液中发现多种与PDCI相关的标志物,涵盖蛋白质、代谢物、炎症因子、microRNA等多个类别,其中α-突触核蛋白、Aβ42/Aβ40、p-tau181、NFL、GFAP等标志物显示出较高的临床应用潜力。多组学技术与机器学习的结合,为PDCI精准诊断模型的构建提供了新途径,而微创标志物的研究则为疾病的无创筛查奠定了基础。 尽管目前PDCI体液生物标志物的研究仍存在诸多挑战,但随着检测技术的进步和研究的深入,通过标志物的联合应用和多学科技术的整合,有望建立标准化的PDCI生物标志物诊断框架,实现疾病的早期识别和精准干预,最终改善PDCI患者的生活质量并延缓疾病进展。

AtomGit 是由开放原子开源基金会联合 CSDN 等生态伙伴共同推出的新一代开源与人工智能协作平台。平台坚持“开放、中立、公益”的理念,把代码托管、模型共享、数据集托管、智能体开发体验和算力服务整合在一起,为开发者提供从开发、训练到部署的一站式体验。
更多推荐
 已为社区贡献7条内容
已为社区贡献7条内容






所有评论(0)